Prawidłowa odpowiedź:
5. Rak gruczołowy (adenocarcinoma)
Komentarz
Polipy jelita grubego pod względem histopatologicznym dzielą się na polipy nowotworowe (gruczolaki, raki) oraz nienowotworowe (polipy hiperplastyczne, polipy zapalne, polipy hamartomatyczne). Rozróżnienie to jest niezwykle ważne z klinicznego punktu widzenia. Na podłożu nowotworowych, lecz łagodnych, polipów gruczolakowatych dochodzi do rozwoju raka jelita grubego, natomiast transformacji złośliwej w przypadku polipów nienowotworowych praktycznie się nie spotyka. Nowoczesna endoskopia pozwala nie tylko na wykrywanie polipów w jelicie grubym, ale również na przewidywanie typu histologicznego na podstawie obrazu ich powierzchni i układu naczyniowego. Taka bezpośrednia charakterystyka polipów pozwala na szybkie podejmowanie decyzji terapeutycznych podczas badania endoskopowego. Na przykład drobne polipy odbytnicy (o średnicy <5 mm) o wyglądzie polipów hiperplastycznych można pozostawić, natomiast takie same polipy o wyglądzie gruczolaków powinny być usunięte na drodze polipektomii.
Ocena powierzchni polipa uwzględnia przede wszystkim analizę tzw. układu dołeczkowego (ang. pit pattern), który tworzą ujścia drobnych krypt gruczołowych wnikających do blaszki właściwej błony śluzowej jelita grubego. Ujścia tych krypt mają różne kształty i układ względem siebie, jednak cechy wspólne układów dołeczkowych na poszczególnych podtypach histologicznych polipów umożliwiły stworzenie klasyfikacji, na podstawie której przewiduje się budowę histopatologiczną polipów, zwaną klasyfikacją Kudo.
Polipy hiperplastyczne mają na swojej powierzchni drobne, okrągłe lub gwiazdkowate ujścia krypt (Kudo I i II) i charakteryzują się słabo widoczną siatką naczyniową z bardzo wąskimi i symetrycznie ułożonymi naczyniami. Dla gruczolaków charakterystyczne są ujścia krypt gruczołowych w kształcie okrągłym, podłużnym lub rozgałęzionym (Kudo III i IV). Naczynia na ich powierzchni mają regularny układ, jednak są szersze niż w przypadku polipów hiperplastycznych i nie są symetryczne ułożone. Dla raków natomiast charakterystyczny jest nieregularny układ różnokształtnych ujść krypt gruczołowych (Kudo V). Podobnie układ naczyniowy ma chaotyczny przebieg, a naczynia są nieregularne („przecinkowate”) i poszerzone. W obrębie raka mogą również występować obszary nieobecnej siatki naczyniowej. Uproszczoną klasyfikację Kudo przedstawia poniższa rycina (patrz piśmiennictwo poz. 1).
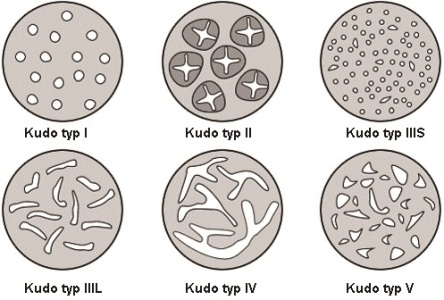
Należy podkreślić, że ocena układu dołeczkowego i naczyniowego w standardowej endoskopii (w świetle białym) jest mało precyzyjna i wskazana jest dodatkowa analiza za pomocą tzw. technik zaawansowanego obrazowania, do których zalicza się obrazowanie wąskopasmowe (and. narrow band imaging – NBI). Celem NBI jest zwiększenie kontrastu i poprawa szczegółowej oceny powierzchni błony śluzowej, dzięki wzmocnieniu wiązek światła o płytkiej penetracji w głąb ciał stałych – są nimi wiązki światła zielonego i niebieskiego. Naczynia krwionośne w obrazowaniu NBI przyjmują kolor ciemnobrązowy. Ocena układu dołeczkowego i drobnych naczyń w obrazowaniu wąskopasmowym może być dodatkowo poprawiona dzięki powiększeniu obrazu (zoom-endoscopy), choć nie jest ona konieczna (ryc. 2).
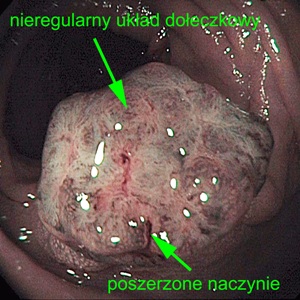
Polip u przedstawionego pacjenta ma nieregularny układ dołeczkowy odpowiadający klasyfikacji Kudo V, a naczynia, zwłaszcza u podstawy polipa, są skrócone i poszerzone. Wstępne rozpoznanie raka pozwoliło zastosować dodatkowe techniki zwiększające szansę na bezpieczne i doszczętne usunięcie polipa. Przede wszystkim tego typu zmiany należy usuwać w jednym fragmencie, ze zwiększonym marginesem zdrowej tkanki, optymalnie po uprzednim podstrzyknięciu zmiany roztworem soli fizjologicznej. Po skutecznej resekcji endoskopowej tego typu zmian należy pamiętać o zaznaczeniu miejsca po polipektomii za pomocą tatuażu endoskopowego – najlepiej dwoma – proksymalnie i dystalnie wobec zmiany. Tatuaż ma na celu ułatwienie znalezienia miejsca po polipektomii w kolejnych badaniach kontrolnych lub podczas zabiegu chirurgicznego, gdy konieczna będzie radykalizacja leczenia w przypadku braku doszczętności leczenia endoskopowego w ocenie histopatologicznej (ryc. 3).
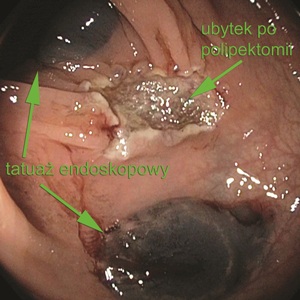
W przedstawionym przypadku badanie mikroskopowe usuniętej zmiany potwierdziło obecność średnio zróżnicowanego raka gruczołowego na podłożu gruczolaka cewkowego (adenocarcinoma G2 ex adenomate tubulari ordinis ortum intestini crassi), jednak zachowane zostały kryteria doszczętności resekcji, ponieważ margines zdrowej tkanki wyniósł 2 mm i nie stwierdzono zatorów raka w naczyniach krwionośnych w ocenianym preparacie (pT1Nx, R0). Rak naciekał głowę polipa i ogniskowo jego szypułę (Haggit 2/3). Pacjent pozostaje zatem pod dalszym nadzorem endoskopowym i nie wymaga dodatkowego leczenia.
Piśmiennictwo:
1. Kudo S., Tamura S., Nakajima T. i wsp.: Diagnosis of colorectal tumorous lesions by magnifying endoscopy. Gastrointest. Endosc. 1996; 44: 8–14
2. Hirata M., Tanaka S., Oka S. i wsp.: Magnifying endoscopy with narrow band imaging for diagnosis of colorectal tumors. Gastrointest. Endosc. 2007; 65: 988–995
3. Rastogi A., Keighley J., Singh V. i wsp.: High accuracy of narrow band imaging without magnification for the real-time characterization of polyp histology and its comparison with high-definition white light colonoscopy: a prospective study. Am. J. Gastroenterol. 2009; 104: 2422–2430
4. Kamiński M.F., Reguła J., Bartnik W. i wsp.: Wytyczne Polskiego Towarzystwa Gastroenterologii dotyczące nadzoru kolonoskopowego po polipektomii — adaptacja wytycznych europejskich. Gastroenterol. Klin. 2011; 2: 55–62









