Czy szczepić przeciwko pneumokokom dzieci po przebyciu chemioterapii lub przeszczepieniu komórek hematopoetycznych szpiku (HSCT)? Jaki schemat zastosować?
Skróty: HSCT – przeszczepienie komórek hematopoetycznych szpiku, PCV – skoniugowana szczepionka przeciwko pneumokokom, PCV-13 – 13-walentna skoniugowana szczepionka przeciwko pneumokokom, PPSV-23 – 23-walentna polisacharydowa szczepionka przeciwko pneumokokom
Szczepienie przeciwko pneumokokom zaleca się wszystkim pacjentom po leczeniu onkohematologicznym – zarówno przyjmującym chemioterapię klasyczną, jak i po HSCT (p. pyt. Czy szczepienie pacjentów z niedoborem odporności przeciwko pneumokokom jest skuteczne? – przyp. red.).
Pacjentom z niedawno rozpoznaną chorobą nowotworową szczepionkę przeciwko pneumokokom należy podać 2 tygodnie przed rozpoczęciem chemioterapii (o ile nie zrealizowano go wcześniej). Jednak w większości przypadków realizacja tego założenia jest niemożliwa, ponieważ priorytetem w chorobach onkohematologicznych jest jak najszybsze rozpoczęcie leczenia przeciwnowotworowego i jego długie opóźnienie jest niedopuszczalne.
W przypadku pacjentów poddawanych standardowej chemioterapii szczepienie odbywa się więc dopiero co najmniej 3 miesiące po zakończeniu leczenia. Zgodnie z zaleceniami po zakończeniu leczenia przeciwnowotworowego podaje się pojedynczą dawkę przypominającą szczepienia PCV (u pacjentów, którzy zrealizowali pełny schemat szczepienia przed zachorowaniem na nowotwór) lub stosuje się więcej dawek PCV (u chorych, którzy nie zrealizowali pełnego schematu przed zachorowaniem na nowotwór – liczba dawek do uzupełnienia jest zależna od liczby dawek przyjętych przed zachorowaniem), a następnie uzupełnia – w miarę dostępności – szczepieniem PPSV-23 (p. pyt. Czy u dzieci >2. roku życia można stosować szczepionki polisacharydowe przeciwko pneumokokom? – przyp. red.). Niektóre wyniki badań wskazują na częściową skuteczność serologiczną szczepionek PCV podawanych u dzieci w trakcie chemioterapii przeciwnowotworowej (Te-Yu Hung i wsp., 2017). Być może obserwacja ta doprowadzi w przyszłości do zmiany zaleceń i wprowadzenia zalecenia szczepienia przeciw pneumokokom nawet w trakcie intensywnej fazy leczenia przeciwnowotworowego, ale na razie dane są zbyt skąpe na zmianę zasad postępowania.
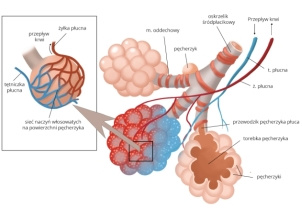
Dzieci po HSCT należą do grupy zwiększonego ryzyka rozwoju zagrażających życiu zakażeń pneumokokowych z powodu czynnościowego hiposplenizmu (wywołanego megachemioterapią i napromienianiem całego ciała [total body irradiation – TBI]) oraz przewlekłej choroby przeszczep przeciwko gospodarzowi (cGvHD). Potwierdzono zadowalającą immunogenność „wczesnego” (>3 mies. po HSCT) szczepienia szczepionką skoniugowaną biorców przeszczepu. Natomiast PPSV-23, która zawiera jedynie czyste polisacharydy i do wywołania optymalnej odpowiedzi odpornościowej wymaga dojrzałego, w pełni sprawnego układu immunologicznego, charakteryzuje się małą immunogennością u biorców przeszczepu. Wykazano, że wczesne szczepienie PPSV-23 (<12 mies. po HSCT) jest nieskuteczne, dlatego można ją podać dopiero po upływie roku od HSCT. Szczepionka polisacharydowa nie przynosi natomiast pożądanych efektów u pacjentów z cGvHD.
Zgodnie z zaleceniami biorcom HSCT podaje się 3 dawki PCV-13, począwszy od 3.–6. miesiąca po przeszczepieniu, niezależnie od wieku pacjenta. Po upływie co najmniej 12 miesięcy od HSCT należy podać kolejne szczepionki:
- u pacjentów bez cech cGvHD – pojedynczą dawkę PPSV-23
- u pacjentów z cechami cGvHD – kolejną (czwartą) dawkę PCV-13.
Piśmiennictwo:
1. Johnston B.L., Conly J.M.: Immunization for bone marrow transplant recipients. Can. J. Infect. Dis., 2002; 13: 353–3572. Parkkali T., Käyhty H., Ruutu T. i wsp.: A comparison of early and late vaccination with Haemophilus influenzae type b conjugate and pneumococcal polysaccharide vaccines after BMT. Bone Marrow Transplant., 1996; 18: 961–967
3. Shigayeva A., Rudnick W., Green K.: Invasive pneumococcal disease among immunocompromised persons: implications for vaccination programs. Clin. Infect. Dis., 2016; 62: 139–147
4. Cordonnier C., Averbuch D., Maury S., Engelhard D.: Pneumococcal immunization in immunocompromised hosts: where do we stand? Expert Rev. Vaccines, 2014; 13: 59–74
5. Halasa N.B., Shankar S.M., Talbot T.R. i wsp.: Incidence of invasive pneumococcal disease among individuals with sickle cell disease before and after the introduction of the pneumococcal conjugate vaccine. Clin. Infect. Dis., 2007; 44: 1428–1433
6. Madhi S.A., Koen A., Jose L. i wsp.: Vaccination with 10 valent pneumococcal conjugate vaccine in infants according to HIV status. Medicine (Baltimore), 2017; 96: e588
7. French N., Gordon S.B., Mwalukomo T. i wsp.: A trial of a 7 valent pneumococcal conjugate vaccine in HIV infected adults. N. Engl. J. Med., 2010; 362: 812–822
8. Torre G., Mannocci A., Colamest V. i wsp.: Influenza and pneumococcal vaccination in hematological malignancies: a systematic review of efficacy, effectiveness, and safety. Mediterr. J. Hematol. Infect. Dis., 2016; 8: e2 016 044
9. Esposito S., Cecinati V., Brescia L. i wsp.: Vaccinations in children with cancer. 2010; 28: 3278–3284
10. Rubin L.G., Levin M.J., Ljungman P. i wsp.: 2013 IDSA clinical practice guideline for vaccination of the immunocompromised host. Clin. Infect. Dis., 2014; 58: 309–318
11. Hung T.S., Kotecha R.S., Blyth C.C. i wsp.: Immunogenicity and safety of single-dose, 13-valent pneumococcal conjugate vaccine in pediatric and adolescent oncology patients. Cancer, 2017; 123: 4215–4223