Źródło:
"Ból i cierpienie." Red. G. Makiełło-Jarża. Acta Academiae Modrevianae, Kraków 2012:105-115
Funkcjonalne zespoły bólowe obejmują szereg schorzeń o niewyjaśnionej dokładnie etiologii. Do grupy tej zaliczane są wszelkie objawy lub dyskomfort fizyczny zgłaszane przez pacjenta, a niemające uzasadnienia fizjologicznego lub organicznej przyczyny, pomimo przeprowadzenia pełnej i dokładnej diagnostyki klinicznej, łącznie z badaniami obrazowymi. Większość pacjentów, u których występują funkcjonalne zespoły bólowe, to kobiety, stąd też częste jest zjawisko niedoceniania tych objawów przez lekarzy i składanie ich na karb nerwicy. Jest to postępowanie błędne, gdyż na obecnym etapie wiedzy istnieją dowody, iż takie zespoły bólowe nie odzwierciedlają konkretnej patologii narządowej, ale są związane z istotnymi zmianami neurobiologicznymi, fizjologicznymi oraz niekiedy anatomicznymi w obrębie ośrodkowego układu nerwowego. Istniejące zaburzenia w obrębie OUN skutkują także zmianami czynnościowymi na obwodzie – zmienionymi właściwościami nocyceptorów i komórek układu immunologicznego, nie wiadomo jednak, jaka jest dokładna rola patologii na obwodzie, szczególnie w podtrzymywaniu zaburzonych relacji neuroendokrynnych OUN – narząd obwodowy.
W etiologii funkcjonalnych zespołów bólowych mogą odgrywać rolę zaburzenia funkcji autonomicznego układu nerwowego, osi podwzgórze–przysadka–nadnercza, zaburzenia funkcji układu immunologicznego i komórek glejowych, zaburzenia mikroflory bakteryjnej jelit, nadwrażliwość nocyceptorów układu trzewnego, a także wzmacnianie doznań bólowych na poziomie OUN, jednakże jak dotąd etiologia ta nie jest dokładnie poznana ani potwierdzona. U pacjentów w przebiegu funkcjonalnych zespołów bólowych w badaniach eksperymentalnych wykazano obecność nadwrażliwości na eksperymentalne bodźce bólowe, a także na bodźce niebolesne – słuchowe, zapachowe i smakowe. W badaniach fMRI oraz testach psychofizycznych wykazano także zaburzoną funkcję zstępujących układów antynocyceptywnych DNIC – diffuse noxious inhibitory control, a w fMRI także nasiloną odpowiedź neuronalną na bodźce bólowe. Badania obrazowe wykazały także zmniejszoną gęstość i grubość korowej substancji szarej w obrębie miejsc związanych z afektywną i poznawczą reakcją na ból. Dodatkowo stwierdzano także w przeprowadzanych testach psychologicznych zaburzenia poznawcze.
W powstawaniu funkcjonalnych zespołów bólowych istotną rolę może odgrywać polimorfizm genetyczny, płeć żeńska, trauma okresu wczesnodziecięcego, np. przemoc w rodzinie, a czynnikiem wyzwalającym może być infekcja, uraz, inne stresory psychologiczne i fizyczne.
Do funkcjonalnych zespołów bólowych zaliczamy:
W badaniach klinicznych wykazano, że zespoły te posiadają wspólną etiologię, podobne czynniki ryzyka, a także wykazano częstsze współwystępowanie i wzajemne nakładanie się tych schorzeń u pacjentów.
Choć nie są to zwykle schorzenia zagrażające życiu, to jednak w istotny sposób obniżają jego jakość, prowadząc niekiedy do trwałej niesprawności. Szacuje się, że w USA około 15% pacjentów otrzymuje rentę z powodu objawów fibromialgii.
Fibromialgia (FM) jest jednym z częściej występujących zespołów funkcjonalnych i jest definiowana jako uogólniony, rozlany, przewlekły ból w układzie mięśniowo-szkieletowym z tkliwością uciskową mięśni szkieletowych i struktur przystawowych, z współwystępującymi objawami, wśród których najczęściej spotykane są zaburzenia snu, zaburzenia wegetatywne, zmęczenie i zaburzenia afektywne. U chorych z FM obserwuje się występowanie nadwrażliwości na bolesne bodźce, zarówno w miejscach bolesnych, jak i niebolesnych, obniżony próg bólu na bodźce termiczne, mechaniczne, elektryczne, akustyczne oraz nasilone czasowe sumowanie bólu. Fibromialgia ma stopniowy samoistny lub pourazowy początek. Ból jest opisywany jako uporczywe, rozlane, głębokie, tępe, tętniące odczucie w mięśniach, najczęściej o charakterze stałym.
Częstość występowania w populacji ogólnej ocenia się na 0,7–3,3%, do siedmiu razy częściej u kobiet niż mężczyzn, choć opisywano również 21-krotnie częstsze występowanie u kobiet. Większość pacjentów to osoby w wieku średnim: 40–60 lat.
Podobnie jak w przypadku innych zespołów funkcjonalnych, u pacjentów z FM stwierdza się częstsze niż w ogólnej populacji współwystępowanie innych schorzeń funkcjonalnych, takich jak depresja, lęk, zespół jelita drażliwego, zmęczenie i zespół przewlekłego zmęczenia, zaburzenia snu, bolesne miesiączkowanie, śródmiąższowe zapalenie pęcherza, przewlekłe bóle krzyża i zespół bólowo-dysfunkcyjny stawu skroniowo-żuchwowego, co może sugerować wspólny mechanizm patofizjologiczny, leżący u podłoża tych chorób.
Kryteria diagnostyczne rozpoznawania FM zostały zaproponowane i opublikowane przez American College of Rheumatology w 2010 roku, eliminując z poprzednich kryteriów z 1990 roku konieczność badania palpacyjnego punktów tkliwych, a podkreślając dla rozpoznania FM znaczenie takich objawów jak:
1. Wskaźnik rozległości bólu (widespread pain index – WPI) ≥7 i stopień natężenia objawów (symptom severity score) ≥5 lub WPI 3–6 i stopień natężenia objawów ≥9.
Ocena WPI polega na oznaczeniu obszarów (maksymalnie 19), w których pacjent odczuwał ból w ciągu ostatniego tygodnia: obustronnie obręcz barkowa, ramiona, przedramiona, pośladki, uda, podudzia, żuchwa, klatka piersiowa brzuch, kark, grzbiet.
Oceniane objawy to zmęczenie, zaburzenia snu i zaburzenia poznawcze, także oceniane są ogólnie inne objawy somatyczne. Każdy z tych elementów oceniany jest w skali 0–3, gdzie 0 – brak, a 3 – wysokie natężenie danego objawu, a suma punktacji stanowi o stopniu natężenia objawów – symptom severity score i wynosi maksymalnie 12. Inne objawy somatyczne występujące w FM i podlegające ocenie obejmują: bóle i osłabienie mięśni, zaburzenia pamięci, obecność zespołu jelita drażliwego, bóle głowy, skurcze w obrębie jamy brzusznej, zawroty głowy, bezsenność, zaparcia lub biegunki, bóle brzucha i klatki piersiowej, suchość w ustach i spojówek, szumy uszne i zaburzenia słuchu, zgaga, zaburzenia smaku i apetytu, duszność, pokrzywka, wypadanie włosów, bolesne i częste oddawanie moczu, objaw Raynauda.
2. Obecność rozlanego bólu na podobnym poziomie przez co najmniej 3 miesięcy.
3. Pacjent nie ma innych schorzeń, które mogłyby w jakikolwiek sposób tłumaczyć występowanie bólu.
Kwestionariusze zalecane w procesie diagnostycznym to Brief Pain Inventory, Fibromyalgia Impact Questionnaire. Badania laboratoryjne zalecane standardowo to OB, morfologia krwi, poziom białka C-reaktywnego, kinazy kreatyninowej, wapnia, TSH. Badania obrazowe nie są zalecane, podobnie jak rutynowe oznaczanie poziomu przeciwciał. Rozpoczynając leczenie pacjenta z FM, należy wykluczyć inne choroby, które mogą przebiegać pod maską fibromialgii (choroby autoimmunologiczne tkanki łącznej, choroby nowotworowe).
Leczenie:
Do metod o mocno udowodnionej skuteczności według Evidence Based Medicine zaliczamy leczenie farmakologiczne – leki przeciwdepresyjne (TCA – amitryptylina, SNRI – duloksetyna, milnacipran, SSRI – fluoksetyna, paroksetyna), ligandy podjednostki α2δ kanału wapniowego – gabapentyna, pregabalina, leki obniżające napięcie mięśni –cyklobenzapryna; oraz metody niefarmakologiczne – ćwiczenia aerobowe, balneo- i spa-terapia, terapia poznawczo-behawioralna, programy leczenia multimodalnego.
Do metod o udowodnionej skuteczności (przynajmniej 2 randomizowane badania kliniczne) zaliczono homeopatię, hipnoterapię, medytacje, dietę wegetariańską, termoterapię całego ciała, a z metod farmakologicznych stosowanie tramadolu i tropisetronu. Podkreślić należy, że brak jest wystarczających dowodów na skuteczność powszechnie stosowanych metod w leczeniu objawów FM jak paracetamol, metamizol, opioidy inne niż tramadol, leki zmniejszające napięcie mięśniowe inne niż cyklobenzapryna, dożylne wlewy lidokainy oraz metody niefarmakologiczne jak ostrzykiwanie punktów tkliwych, masaż, osteopatia, drenaż limfatyczny, Qi-gong, fizjoterapia. Dane dotyczące skuteczności akupunktury są niejednoznaczne, chociaż obiecujące. Natomiast metody nieskuteczne w leczeniu FM obejmują stosowanie leków jak NLPZ, steroidy, neuroleptyki, anksjolityki, podobnie metody takie jak biofeedback, relaksacja i edukacja pacjenta stosowane jako pojedyncze metody terapeutyczne.
Obecnie eksperci zalecają trójstopniowy model postępowania w fibromialgii w zależności od występujących dolegliwości, ograniczenia aktywności pacjenta, odpowiedzi na różne formy terapii. W pierwszym etapie American Pain Society (APS), German Interdisciplinary Guideline Group (GIGG) oraz European League Against Rheumatism zalecają dokładne postawienie rozpoznania, edukację pacjenta, omówienie dostępnych opcji leczenia, a następnie jako terapia pierwszego rzutu wprowadzenie indywidualnych ćwiczeń aerobowych, terapii poznawczo-behawioralnej oraz trójcyklicznych leków przeciwdepresyjnych (amitryptylina w dawce 25–50 mg/d).
W przypadku braku skuteczności powyższych metod w drugim etapie zalecane jest przez APS ostrzykiwanie punktów tkliwych, terapia manualna, akupunktura oraz leczenie farmakologiczne – inhibitory zwrotnego wychwytu serotoniny i noradrenaliny (duloksetyna 60–120 mg/d, milnacipran 100–200 mg/d), selektywne inhibitory zwrotnego wychwytu serotoniny (fluoksetyna 20–40 mg/d, paroksetyna 20–40 mg/d), leki przeciwpadaczkowe (gabapentyna, pregabalina w dawce 150–300 mg/d), tramadol. Leczenie farmakologiczne powinno trwać do 6 miesięcy, a ocena skuteczności powinna się odbywać po 3 miesiącach stosowania amitryptyliny, w przypadku pozostałych leków po 6 miesiącach stosowania. Oczywiście, jeżeli leczenie farmakologiczne jest skuteczne w zmniejszeniu objawów FM można rozważyć kontynuację i długotrwałą farmakoterapię. Leczenie niefarmakologiczne powinno być stosowane do 24 miesięcy.
Trzeci stopień postępowania w fibromialgii, gdy mimo ww. leczenia objawy nadal się utrzymują, obejmuje wielodyscyplinarne podejście do chorego – multimodalne programy terapeutyczne, psychoterapię, farmakoterapię, opioidy, terapie niekonwencjonalne (homeopatia, leczenie dietetyczne) i ich połączenie. Stosowanie odpowiednich metod powinno odbywać się na podstawie świadomej zgody i preferencji pacjenta, chorób współistniejących i dostępności metod terapeutycznych. Leczenie długoterminowe powinno obejmować głównie stosowanie metod niefarmakologicznych, takich jak ćwiczenia aerobowe, terapia poznawczo-behawioralna, multimodalne programy terapeutyczne. Ocena efektów leczenia powinna się odbywać po zakończeniu terapii i potem co 6 miesięcy.
Ogólne zasady postępowania w FM kładą nacisk na samoleczenie pacjenta i jego maksymalne zaangażowanie w proces terapeutyczny, co ma polegać na zaakceptowaniu objawów i ograniczeń, jak np. zakaz ciężkiej pracy fizycznej, a także zachowaniu aktywności fizycznej i radzeniu sobie ze stresem. Celem leczenia jest zachowanie lub poprawa codziennego funkcjonowania i niesprawności pacjenta.
Bóle twarzy
Pomimo opracowanych i dostępnych kryteriów diagnostycznych pozwalających właściwie rozpoznawać bóle w obrębie głowy i twarzy zarówno ich rozpoznawalność, ocena kliniczna, a także leczenie przysparza problemów wielu specjalistom. Powszechnie akceptowana jest klasyfikacja bólów głowy i twarzy opracowana przez International Headache Society – International Classification of Headache Disorders (2004). Opisano w niej liczne zespoły bólowe w obrębie głowy i twarzy, ale jak wynika z doświadczeń klinicznych, wciąż pojawiają się doniesienia o nowych zespołach bólowych nieujętych w tej klasyfikacji bądź będących niewyodrębnioną odmianą już opisanych zespołów bólowych. Ból w obrębie twarzy nie jest rzadkim zjawiskiem, a większość dolegliwości, zwłaszcza ból ostry, związana jest z dolegliwościami ze strony zębów i może być skutecznie leczona przez stomatologów. Problem pojawia się, jeśli ból ma charakter przewlekły i ma swą lokalizację zewnątrzustnie. Ból w obrębie twarzy może powstawać w różnych strukturach: opony mózgowe, rogówka, miazga zęba, śluzówka jamy ustnej czy nosa, staw skroniowo-żuchwowy, tym samym posiada kilka odmiennych cech fizjologicznych w porównaniu z rdzeniowym systemem nocyceptywnym. Badania z ostatnich lat wykazują różnice w elektrofizjologicznych, anatomicznych i farmakologicznych właściwościach aferentnych włókien trójdzielnych odpowiedzialnych za unerwienie struktur twarzy.
Trudno jest jednoznacznie określić częstotliwość występowania bólu twarzy w ogólnej populacji. Z analizy elektronicznych baz danych Integrated Primary Care Information (IPCI) database zebranych przez Koopmana (2009) wynika, że całkowita zachorowalność na bóle twarzy wynosi 38,7 [95% CI: 34.9–42.9]/ 100 000/rok, z czego największy odsetek stanowią neuralgia trójdzielna (32,6%) i klasterowe bóle głowy (32,3%), w dalszej kolejności neuralgia popółpaścowa (9,9%), neuralgia nerwu potylicznego (8,3%), zlokalizowana neuralgia (4,7%), neuralgia nerwu językowo-gardłowego (0,6%), nietypowy ból twarzy (11,3%).
Rzadkie występowanie bólów twarzy, brak obiektywnych testów diagnostycznych i szeroki zakres przyczyn i objawów sprawiają, że postawienie właściwego rozpoznania jest trudne dla niespecjalisty. Z tego względu wiedza na temat przewlekłych bólów twarzy jest niezbędna nie tylko dla lekarzy zajmujących się leczeniem bólu w specjalistycznych poradniach leczenia bólu, ale także dla lekarzy pierwszego kontaktu, jak i innych specjalności medycznych (stomatologów, okulistów, laryngologów, neurologów).
Na rysunku 1 przedstawiono propozycję diagnostyki różnicowej bólów twarzy.
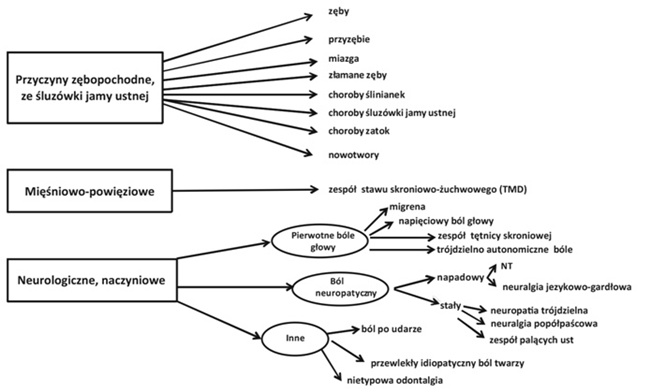
Ryc. 1. Diagnostyka różnicowa bólów twarzy.
Przewlekły idiopatyczny ból twarzy (PIBT)/przetrwały ból twarzy/nietypowy ból twarzy
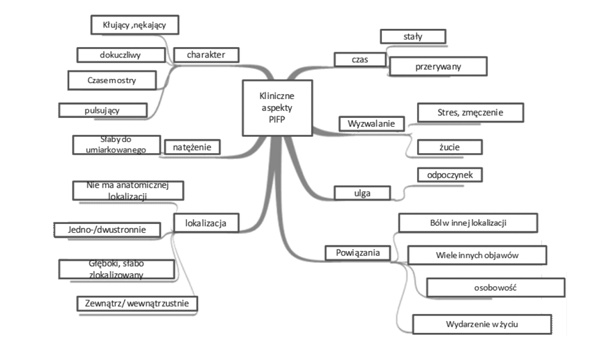
Ryc. 2. Kliniczne aspekty przewlekłego idiopatycznego bólu twarzy.
Rozpoznanie przewlekłego idiopatycznego bólu twarzy zazwyczaj stawia się, jeśli wykluczono inne organiczne przyczyny dolegliwości w jego lokalizacji, stąd też zaliczany jest do funkcjonalnych somatycznych zespołów bólowych. Ten rodzaj dolegliwości charakteryzuje się stałym, palącym, parzącym lub piekącym bólem występującym głównie u chorych w młodym wieku. Ból ma charakter stały, zdarzają się okresy ulgi w dolegliwościach. Ból może być zmienny w swoim nasileniu i pojawia się zwykle w zakresie unerwienia nerwu V, ale czasami obejmuje obszar górnej części karku i potylicę. Czynniki nasilające: jedzenie, mówienie, stres, ale nie „drażnienie punktów spustowych”. Czynniki przynoszące ulgę: odpoczynek, relaks.
Przyczyna występowania nie jest do końca wyjaśniona, rozważa się ten zespół bólowy jako twarzową postać migreny, z dużym udziałem komponenty psychogennej. Ostatnio w patogenezie przewlekłego idiopatycznego bólu twarzy podkreśla się również rolę substancji wazoaktywnych, uwalnianych na drodze antydromowej stymulacji z zakończeń nerwu V. Może pojawić się u chorych z neuralgią nerwu V, u których wykonywano zabiegi neurodestrukcyjne.
U pacjentów z przewlekłym idiopatycznym bólem twarzy zmiany osobowości są utrwalone i mają odzwierciedlenie w pasywnym trybie życia i depresji prowadzącej do nadużycia leków, co komplikuje proces prawidłowej diagnozy i skutecznego leczenia. Występowanie tej dolegliwości w 80% dotyczy kobiet, szczyt zachorowania przypada między 40 a 50 rokiem życia. Czynniki potencjalizujące występowanie dolegliwości: płeć żeńska, wysoki stopień troski o własne zdrowie, zachowania bólowe w celu uzyskania środków finansowych, inne objawy somatyczne, ostatnio występujące zdarzenia niepożądane.
Kryteria diagnostyczne przewlekłego idiopatycznego bólu twarzy według International Headache Society:
Ból twarzy codzienny, trwający od 1 miesiąca, utrzymujący się
przez większość dnia, o przynajmniej czterech cechach z grupy kryteriów B i C.
1. Ból jest ograniczony i powstaje w ograniczonym obszarze po jednej stronie twarzy;
2. Ból jest głęboki i trudny do zlokalizowania;
3. Stopień nasilenia: umiarkowany do silnego, ale nie „nie do zniesienia”;
4. Napadowy ból nie występuje;
5. Ból nie nasila się przy dotyku i aktywności.
Obydwa z poniższych kryteriów:
1. Brak objawów autonomicznych;
2. Brak ubytków czucia i innych objawów neurologicznych, może być dyzestezja.
Badania dodatkowe nie wykazują patologii (łącznie z RTG twarzy i stawów skroniowo-żuchwowych).
Rozpoznanie wymaga zatem dokładnej analizy badania przedmiotowego, objawów zespołu bólowego oraz diagnostykę radiologiczną czaszki i zatok ze szczególnym uwzględnieniem oceny podstawy czaszki w tomografii komputerowej.
Leczenie pacjentów z przewlekłym idiopatycznym bólem twarzy stanowi duży problem. Zwykle wymaga postępowania wielodyscyplinarnego, ale przede wszystkim zaangażowania pacjenta. Dokładna ocena i badanie wykluczające inne przyczyny dolegliwości bólowych może wpłynąć na efektywność terapii. W badaniach randomizowanych wykazano skuteczność amitryptyliny w dawce 50–150mg/dobę, fluoksetyny w dawce 20mg/dobę, dosulepiny: 25–150mg/dobę, fenelzyny: 45mg/dobę. Terapia poznawczo-behawioralna może być przydatna w leczeniu PIBT, choć rola psychoterapii w leczeniu tego schorzenia jest szeroko dyskutowana i chociaż kontrolowane badania niejednoznacznie potwierdzają zasadność jej stosowania. Wydaje się jednak, że gdy chory wykazuje ewidentne zaburzenia osobowości skojarzone z wystąpieniem PIBT, to należy wdrożyć postępowanie psychoterapeutyczne. Ponadto w terapii PIBT stosuje się również TENS oraz elektrostymulację za pomocą elektrod zaimplantowanych do zwoju Gassera lub do wzgórza.
Uważa się, że wczesne rozpoznanie i rozpoczęcie leczenia warunkuje znacznie lepszy efekt terapeutyczny.
Rzadką postacią PIBT jest obustronny, nietypowy, stały, palący ból twarzy o nieznanej etiologii, występujący prawie wyłącznie u kobiet (ale w każdym wieku). Bólowi temu towarzyszyć mogą zaburzenia czucia (dysestezja, hipoestezja, parestezje) oraz zaburzenia osobowości (wskazana psychoterapia), jak również nie jest on wyzwalany przez nienocyceptywną stymulację w zakresie obszaru bólowego. Brak jest skutecznej terapii dla tej postaci PIBT i najważniejszym zadaniem do spełnienia dla terapeuty jest ochrona chorego przed nieadekwatnym postępowaniem terapeutycznym.
W podsumowaniu należy stwierdzić, że funkcjonalne zespoły bólowe są jednym z częściej występujących rodzajów bólu przewlekłego i jako takie należy je traktować jak chorobę samą w sobie, wymagającą wielokierunkowego postępowania. Wnikliwa ocena objawów klinicznych oraz charakteru bólu pozwala u większości pacjentów na dobór optymalnego leczenia. U wielu pacjentów z bólem przewlekłym etiologia jest złożona, stąd też leczenie powinno być ukierunkowane nie tylko na przyczynę bólu, ale również powinien być wdrożony program leczenia wielokierunkowego z uwzględnieniem także psychologicznego i emocjonalnego komponentu bólu.
Piśmiennictwo
1. Burckhardt C.S. i in., Guideline for the management of fibromyalgia syndrome pain in adults and children, „American Pain Society” (APS) 2005, s. 109.
2. Carville S.F. i in., EULAR evidence based recommendations for the management of fibromyalgia syndrome, „Ann Rheum Dis” 2008, Vol. 67, s. 536–541.
3. Eich W., Häuser W., Friedel E. i in., Definition, classification and diagnosis of fibromyalgia syndrome, „Schmerz” 2008, Vol. 22, s. 256–266.
4. Evidence-Based Chronic Pain Management, red. C.F. Stannard, E. Kalso, J. Ballantyne, BMJ books 2010.
5. Fietta P., Manganelli P., Fibromyalgia and psychiatric disorders, „Acta Biomed” 2007, Vol. 78, s. 88–95.
6. Gran J.T., The epidemiology of chronic generalized musculoskeletal pain, „Best Pract Res Clin Rheumatol” 2003, Vol. 17, s. 547–561.
7. Hargreaves K.M., Orofacial Pain, „Pain” 2011, Vol. 152 (3S), s. 25–33.
8. Häuser W. i in., Efficacy of multicomponent treatment in fibromyalgia syndrome – a meta-analysis of randomized controlled clinical trials, „Arthritis Rheum” 2009, Vol. 61 (2), s. 216–224.
9. Häuser W., Bernardy K., Üceyler N., Sommer C., Treatment of fibromyalgia syndrome with gabapentin and pregabalin – a meta-analysis of randomized controlled trails, „Pain” 2009, June 16 epub.
10. Häuser W., Bernardy K., Üçeyler N., Treatment of fibromyalgia syndrome with antidepressants – a meta-analysis, JAMA 2009, Vol. 301 (2), s. 198–209.
11. Häuser W. i in., Fibromyalgia Syndrome Classification, Diagnosis, and Treatment, „Deutsches Ärzteblatt International Dtsch Arztebl Int” 2009, Vol. 106 (23), s. 383–391.
12. Häuser W., Thieme K., Petzke F., Sommer C., Fibromyalgia, [w:] Evidence-Based Chronic Pain Management, red. C. Stannard, E. Kalso, J. Ballantyne, Blackwell Publishing Ltd 2010, s. 121–133.
13. Häuser W., Zimmer C., Felde E., Köllner V., What are the key symptoms of fibromyalgia? Results of a survey of the German Fibromyalgia Association, „Schmerz” 2008, Vol. 22, s. 176–183.
14. Headache Classification Committee of The International Headache Society. The International Classification of Headache Disorders, „Cephalgia” 2004, Vol. 24 (Suppl 1), s. 1–160.
15. Jorns T.P., Zakrzewska J.M., Evidence-based approach to the medical management of trigeminal neuralgia, „Br J Neurosurg” 2007 Jun, Vol. 21 (3), s. 253–261.
16. Koopman J.S. i in., Incidence of facial pain in the general population, „Pain” 2009, Dec 15, Vol. 147 (1–3), s. 122.
17. Loeser J.D., Cranial neuralgias, „In Bonica’s Management of Pain” 2001, s. 855–886.
18. Medycyna bólu, red. J. Dobrogowski, J. Wordliczek, PZWL, Warszawa 2011.
19. Przeklasa-Muszyńska A., Wiatr M., Dobrogowski J., Bóle twarzy – metody leczenia według medycyny opartej na dowodach naukowych, aktualny stan wiedzy, „Ból” 2012, t. 13, nr 1, s. 28–34.
20. Smith B., Peterson K., Fu R., McDonagh M., Thakurta S., Drug Class Review: Drugs for Fibromyalgia: Final Original Report. Oregon Evidence-based Practice Center, Oregon Health & Science University, April 2011.
21. Sommer C., Häuser W., Berliner M. i in., Pharmacological therapy of fibromyalgia syndrome, „Schmerz” 2008, Vol. 22, 313–323.
22. Sommer C., Häuser W., Gerhold K. et al., Etiology and pathophysiology of fibromyalgia syndrome and chronic widespread pain, „Schmerz” 2008, Vol. 22, s. 267–282.
23. Stępień A., Ostre bóle głowy – diagnostyka i leczenie. Acute headache – diagnosis and treatment, „Przewodnik Lekarza” 2006, Vol. 9, s. 28–38.
24. Thieme K., Häuser W., Batra A. et al., Psychotherapy in patients with fibromyalgia syndrome, „Schmerz” 2008, Vol. 22, s. 295–302.
25. Wolfe F. i in., Preliminary Diagnostic Criteria for Fibromyalgia and Measurement of Symptom Severity, „The American College of Rheumatology, Arthritis Care & Research” May 2010, Vol. 62, No. 5, s. 600–610.
26. Wolfe F., Smythe H.A., Yunus M.B. i in., The American College of Rheumatology criteria for the classification of fibromyalgia: report of the Multicenter Criteria Committee, „Arthritis Rheum” 1990, Vol. 33, s. 160–172.
27. Zakrzewska J.M., Facial pain: an update, „Curr Opin SupportPalliat Care” 2009, Vol. 3, s. 125–130.