Leczenie substytucyjne wydłuża przeżycie pacjentów z postacią niemowlęcą choroby, zmniejsza kardiomegalię, wpływa korzystnie na funkcję serca i mięśni szkieletowych. Pomimo hipotonii mięśniowej większość dzieci uczy się chodzić i osiąga zadowalającą sprawność ruchową. Należy jednak zaznaczyć, że mimo leczenia enzymatycznego choroba ma charakter postępujący. Ciągły postęp choroby widoczny jest między innymi w wynikach badań biochemicznych – stężenia transaminaz we krwi (zwłaszcza AspAT) nierzadko przekraczają 500 U/µl, a stężenie kinazy kreatynowej (CK) – 2000 U/µl.
Pacjenci CRIM– gorzej odpowiadają na enzymatyczne leczenie substytucyjne ze względu na rozwój przeciwciał, które neutralizują skuteczność rekombinowanego enzymu.
U pacjentów z postacią późną leczenie enzymatyczne poprawia sprawność fizyczną, zmniejsza progresję niewydolności oddechowej i ryzyko konieczności stosowania wentylacji mechanicznej. Poprawę sprawności obserwuje się zwykle w 1. roku leczenia, a uzyskany efekt zazwyczaj utrzymuje się w następnych latach. Progresja choroby ulega znacznemu spowolnieniu.
Chorzy wymagają również terapii wspomagającej, przede wszystkim fizjoterapii, ze względu na słaby odruch kaszlowy oraz upośledzenie klirensu śluzowo-rzęskowego. Szczególny nacisk należy położyć na profilaktykę chorób infekcyjnych (szczepienia ochronne pacjentów oraz osób z bliskiego kontaktu, coroczne szczepienia przeciw grypie).
Niektórzy pacjenci ostatecznie wymagają wentylacji mechanicznej. Najchętniej stosowana jest wentylacja nieinwazyjna (non-invasive ventilation – NIV), która skutecznie koryguje hipowentylację pęcherzyków płucnych oraz hiperkapnię. Ponadto przerywana (nocna) NIV poprawia wytrzymałość mięśni oddechowych oraz wspomaga rozszerzanie klatki piersiowej i płuc, co może zapobiegać wystąpieniu niedodmy i infekcji.
U pacjentów, u których występują trudności w karmieniu, może być konieczne odżywianie przez zgłębnik żołądkowy lub gastrostomię.
Istotne znaczenie dla optymalnej opieki nad pacjentem z chorobą Pompego ma multidyscyplinarne podejście, w którym łączy się wiedzę pediatrów, neurologów, pulmonologów i specjalistów intensywnej terapii.
| Objawy kliniczne choroby Pompego postaci niemowlęcej | |
|---|---|
| Układ sercowo-naczyniowy | kardiomegalia
kardiomiopatia przerostowa zwężenie drogi odpływu z lewej komory zaburzenia rytmu serca niewydolność krążenia |
| Układ nerwowo-mięśniowy | zmniejszone napięcie mięśniowe
brak odruchów ścięgnistych lub ich osłabienie opóźniony rozwój motoryczny |
| Układ oddechowy | zaburzenia oddychania
niewydolność oddechowa |
| Układ pokarmowy | słaby przyrost masy ciała
powiększenie języka trudności w karmieniu powiększenie wątroby |
| Inne | niedosłuch
podwyższona kinaza kreatynowa hipertransaminazemia |
| Objawy kliniczne choroby Pompego postaci o późnym początku | |
|---|---|
| Układ sercowo-naczyniowy | zaburzenia rytmu serca
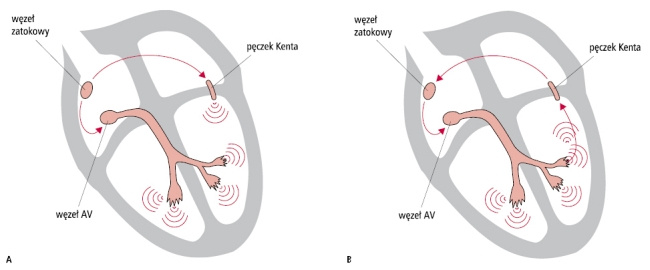
zespół preekscytacji tętniaki aorty/mózgu (szczególnie tętnicy podstawnej) |
| Układ nerwowo-mięśniowy | postępujący niedowład proksymalny (obręczowo-kończynowy)
zaburzenia chodu (chód „kaczkowaty”) objaw Gowersa osłabione/zniesione odruchy ścięgniste bóle mięśni słaba tolerancja wysiłku (wczesne zmęczenie) ptoza jedno- lub obuoczna zespół sztywnego kręgosłupa (rigid spine syndrome – RSS) hiperlordoza i skolioza (dzieci) opóźnienie rozwoju motorycznego (dzieci) |
| Układ oddechowy zaburzenia oddychania niewydolność oddechowa |
duszność wysiłkowa
orthopnoë problemy z oddychaniem podczas snu, bezdech senny senność w ciągu dnia, zawroty głowy słaby kaszel częste infekcje dróg oddechowych |
| Układ pokarmowy | trudności z żuciem
dysfagia powiększenie języka objawy zespołu jelita drażliwego powiększenie wątroby (dzieci) |
| Inne | niedosłuch
ptoza jedno- lub obuoczna podwyższona kinaza kreatynowa hipertransaminazemia |
| Diagnostyka różnicowa choroby Pompego | |
|---|---|
| Dystrofie | dystrofia mięśniowa obręczy kończyn
dystrofia mięśniowa Duchenne’a lub Beckera miopatia mięśniowo-włóknista dystrofia miotoniczna typu 2 |
| Miopatie zapalne | zapalenie wielomięśniowe
wtrętowe zapalenie mięśni |
| Miopatie wrodzone | miopatia nemalinowa
miopatia typu central core (central core disease – CCD) miopatia typu MmD (multi mini cores) choroba Danona |
| Miopatie metaboliczne | miopatie mitochondrialne
glikogenoza typu IIIa glikogenoza typu IV choroba McArdle’a |
| Zaburzenia neuronu ruchowego | rdzeniowy zanik mięśni
stwardnienie zanikowe boczne choroba Kennedy’ego |
| Zaburzenia łącza nerwowo-mięśniowego | miastenia
wrodzone zespoły miasteniczne |
| Inne | idiopatyczna kardiomiopatia przerostowa
zapalenie mięśnia sercowego fibroelastoza wsierdzia wrodzona niedoczynność tarczycy |
Piśmiennictwo:
1. Pompe Disease Diagnostic Working Group, Winchester B., Bali D., Bodamer O.A. i wsp.: Methods for a prompt and reliable laboratory diagnosis of Pompe disease: report from an international consensus meeting. Mol. Genet. Metab. 2008; 93 (3): 275–281.2. Boentert M., Prigent H., Várdi K. i wsp.: Practical Recommendations for Diagnosis and Management of Respiratory Muscle Weakness in Late-Onset Pompe Disease. Int. J. Mol. Sci. 2016; 17 (10): 1735.
3. Toscano A., Schoser B.: Enzyme replacement therapy in late-onset Pompe disease: A systematic literature review. J. Neurol. 2013; 260: 951–959.
4. Bembi B., Cerini E., Danesino C. i wsp.: Management and treatment of glycogenosis type II. Neurology 2008; 71 (Suppl. 2): S12–S36.
5. Kishnani P.S., Corzo D., Nicolino M. i wsp.: Recombinant human acid ?-glucosidase: Major clinical benefits in infantile-onset Pompe disease. Neurology 2007; 68: 99–109.
6. Tarnopolsky M., Katzberg H., Petrof B.J. i wsp.: Pompe Disease: Diagnosis and Management. Evidence-Based Guidelines from a Canadian Expert Panel. Can. J. Neurol. Sci. 2016; 43 (4): 472–485.