Tłumaczył lek. Kamil Polok
Konsultował prof. dr hab. n. med. Roman J. Nowicki, Katedra i Klinika Dermatologii, Wenerologii i Alergologii, Gdański Uniwersytet Medyczny
Jak cytować: Bernstein J.A., Cremonesi P., Hoffmann T.K., Hollingsworth J.: Obrzęk naczynioruchowy na oddziale ratunkowym – praktyczny przewodnik po diagnostyce różnicowej i leczeniu. Med. Prakt., 2018; 7-8: 37–49
Skróty: ACEI – inhibitor konwertazy angiotensyny, AE (angioedema) – obrzęk naczynioruchowy, ARB – bloker receptora angiotensynowego, C1-INH – inhibitor esterazy C1, FFP – świeżo mrożone osocze, GKS – glikokortykosteroid(y), HAE (hereditary angioedema) – wrodzony obrzęk naczynioruchowy, NSLPZ – niesteroidowy lek przeciwzapalny, SOR – szpitalny oddział ratunkowy
Translated from International Journal of Emergency Medicine 10:15, Jonathan A. Bernstein, Paolo Cremonesi, Thomas K. Hoffmann and John Hollingsworth, Angioedema in the emergency department: a practical guide to differential diagnosis and management, https://doi.org/10.1186/s12245-017-0141-z © The Authors. 2017. This article is distributed under the terms of the Creative Commons Attribution 4.0 International License (http://creativecommons.org/licenses/by/4.0/).
Streszczenie
Wprowadzenie: Obrzęk naczynioruchowy (AE) jest częstą przyczyną zgłaszania się na szpitalny oddział ratunkowy (SOR). AE dróg oddechowych może prowadzić do zgonu, dlatego szybkie ustalenie rozpoznania i odpowiednie leczenie mają zasadnicze znaczenie.
Cel przeglądu: Przegląd ten ma na celu dostarczenie praktycznych wskazówek dotyczących diagnostyki, różnicowania i leczenia na SOR AE zależnego od histaminy lub bradykininy. Został on przygotowany na podstawie
wniosków 2 międzynarodowych zespołów ekspertów w dziedzinach AE i medycyny ratunkowej.
Wyniki: AE najczęściej ma charakter histaminergiczny, jednak personel SOR musi też pamiętać o rzadziej występującej postaci AE zależnej od bradykininy. Co ważne, AE zależny od bradykininy nie odpowiada na to samo
leczenie co AE histaminergiczny. AE zależny od bradykininy ma wiele przyczyn, w tym wrodzone defekty inhibitora
esterazy C1 (C1-INH), skutki uboczne inhibitorów konwertazy angiotensyny (ACEI) i nabyty niedobór C1-INH.
Rosnące stosowanie ACEI w ostatnich dekadach doprowadziło do tego, że na SOR częściej trafiają chorzy z AE
związanym z ACEI. Badania ankietowe wykazały jednak, że wielu pracowników SOR może nie wiedzieć, jak
rozpoznawać i leczyć AE zależny od bradykininy, a szpitale mogą nie mieć odpowiednich leków lub protokołów
postępowania w takich przypadkach.
Wnioski: Lekarze pracujący na SOR muszą mieć świadomość istnienia różnych szlaków patofizjologicznych prowadzących do AE, aby w tych potencjalnie śmiertelnych stanach chorobowych postępować sprawnie i skutecznie.
Wprowadzenie
Obrzęk naczynioruchowy (AE) jest stosunkowo częstą przyczyną zgłaszania się pacjentów na szpitalny oddział ratunkowy (SOR). W Stanach Zjednoczonych AE i/lub pokrzywka w ciągu całego życia wystąpi u około 25% osób i odpowiada za ponad milion wizyt na SOR rocznie.1,2 W rozwoju AE bierze udział kilka mechanizmów, w tym histamina i bradykinina (ryc. 1). Do odpowiedniego leczenia niezbędne jest rozpoznanie konkretnego typu AE,3 jednak wielu lekarzy pracujących na SOR może nie wiedzieć, jak odróżnić poszczególne typy AE oraz jak skutecznie leczyć rzadsze postacie kliniczne tej choroby.4
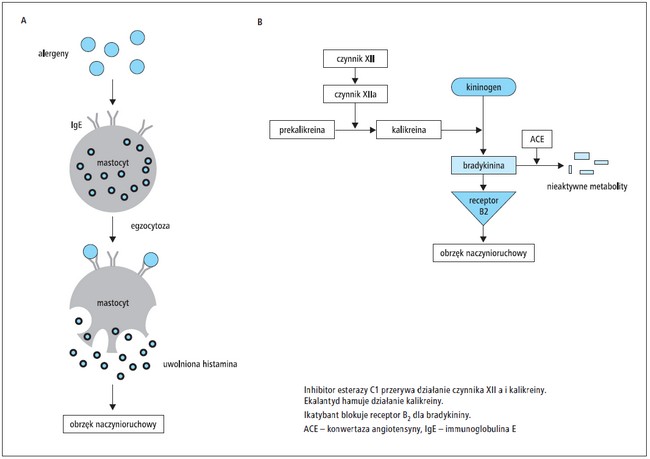
Ryc. 1. Schemat szlaków biochemicznychh odpowiadających za obrzęk naczynioruchowy histaminergiczny (A)62 i zależny od bradykininy (B)26
Każdego roku w Stanach Zjednoczonych AE
lub reakcje alergiczne są przyczyną ponad miliona
zgłoszeń na SOR.2 Spośród nich około 110 000
przypadków zostaje zakwalifikowanych jako AE
(dziedziczny lub nabyty), a 979 400 – jako reakcje
alergiczne.2 Około 42,5% wizyt zakwalifikowanych
jako reakcje alergiczne zawiera również kod
pokrzywki.2 Między 2280 a 5000 wizyt na amerykańskich
SOR każdego roku można przypisać wrodzonemu
AE (hereditary angioedema – HAE),5,6
co oznacza 1,87 na 100 000 wizyt na SOR,5 ale
liczby te mogą nie doszacowywać rzeczywistego
obciążenia SOR przez AE.2,5,6 Podobne dane z Włoch sugerują, że 0,37% zgłoszeń na SOR jest związanych z AE,7 a w opublikowanym niedawno
badaniu kanadyjskim oszacowano, że AE był przyczyną 1 na 1000 wizyt na SOR.8 W końcu badanie
ankietowe przeprowadzone w Wielkiej Brytanii
wykazało, że 30% chorych na wrodzony lub nabyty
AE zgłosiło się w przeszłości na SOR.9 W związku z tym, że ACEI przepisuje się coraz
powszechniej, częstość występowania AE związanego z ACEI (ACEI-AAE) znacząco wzrosła10-14 i w Stanach Zjednoczonych stanowi obecnie 30%
zgłoszeń na SOR z powodu AE (0,7/10 000 wizyt
na SOR), a na Karaibach nawet 60%.10,11,14
Hospitalizacja może być wykorzystana jako
wskaźnik ciężkości AE. Chorzy z niezróżnicowanym
AE (tzn. z AE zależnym od histaminy
lub z AE zależnym od bradykininy) zgłaszający
się na SOR są przyjmowani do szpitala (11% wizyt na SOR) częściej niż chorzy z reakcjami alergicznymi
(2,2% wizyt na SOR).2,5 Większy jest
odsetek hospitalizacji zgłaszających się na SOR z powodu HAE (45–50%) i ACEI-AAE (42–66%).5,6,10,12 Liczba hospitalizacji z powodu AE
wzrosła w ostatnich 15 latach z 3,3–3,4/100 000
przyjęć w latach 1998–2000 do 4,0/100 000 w 2005 roku i 5,4/100 000 w 2009 roku.15,16 Uważa
się, że wzrost ten ma związek z coraz częstszym
przepisywaniem ACEI w tym okresie.15,16
Niestety nie ma danych dotyczących śmiertelności u chorych na AE, aczkolwiek w jednym badaniu
wykazano niewielkie ryzyko zgonu przez
uduszenie u chorych z HAE, u których doszło
do obrzęku krtani, w ciągu zaledwie 15 minut.17
Co istotne, ryzyko zgonu jest 3–9-krotnie większe u chorych bez potwierdzonego rozpoznania HAE,
co podkreśla znaczenie odpowiedniego przygotowania
oraz świadomości w zapobieganiu zdarzeniom
niepożądanym.17 Chociaż AE z dobrze udokumentowaną
patogenetyczną rolą bradykininy
występuje stosunkowo rzadko, większość personelu
SOR prawdopodobnie spotka taki przypadek w swojej pracy. W związku z tym świadomość
możliwości występowania AE zależnego od bradykininy u pacjenta SOR jest ważna.
Ponieważ AE zależny od bradykininy jest rzadki,
na SOR zazwyczaj nie ma odpowiednich protokołów
postępowania w takich przypadkach ani
natychmiastowego dostępu do właściwych leków.
Na przykład niedawne badanie ankietowe przeprowadzone
na brytyjskich SOR ujawniło, że leki konieczne
do leczenia AE zależnego od bradykininy
były dostępne w większości szpitali udzielających
specjalistycznych świadczeń także z zakresu immunologii,
ale nie były dostępne na SOR (np. przechowywano
je w głównej aptece szpitalnej). Ponadto w zaledwie połowie szpitali objętych badaniem
ustalono wytyczne stosowania tych leków.18
Brak protokołów i dostępu do leków może prowadzić
do błędów w leczeniu i jego nieskuteczności u pacjentów SOR zgłaszających się z powodu AE
zależnego od bradykininy.19,20 Niniejszy artykuł
przedstawia wnioski i zalecenia sformułowane w 2013 roku przez 2 międzynarodowe zespoły,
składające się z 16 specjalistów w dziedzinach
AE i medycyny ratunkowej.21,22 Celem tej publikacji
jest dostarczenie praktycznych wskazówek dotyczących wczesnej identyfikacji AE zależnego
od bradykininy na SOR, co umożliwi poprawę diagnostyki i wyników leczenia napadów AE.
Przegląd
Typy i charakterystyka AE
AE to przejściowy, nieciastowaty obrzęk tkanki podskórnej lub podśluzówkowej.1 Różni się od obrzęku wywołanego nagromadzeniem płynu w tkance śródmiąższowej, charakteryzującego się powstawaniem dołków pod wpływem ucisku. W rozwoju AE mogą uczestniczyć histamina, bradykinina i inne mechanizmy.1
AE histaminergiczny
AE histaminergiczny często wiąże się z wystąpieniem pokrzywki i obrzęku, który zwykle ustępuje w ciągu 24–37 godzin. AE histaminergiczny, zwany również alergicznym, jest związaną z degranulacją mastocytów reakcją nadwrażliwości typu I z udziałem immunoglobuliny E. Do reakcji tej dochodzi w wyniku wcześniejszego uczulenia na alergeny, takie jak jady owadów, pokarmy i leki.1
AE niehistaminergiczny
AE zależny od bradykininy jest najczęstszą przyczyną niehistaminergicznego AE. W patomechanizmie AE rzekomoalergicznego i AE idiopatycznego nie uczestniczy ani histamina, ani bradykinina. AE zależny od bradykininy dzieli się na 3 odrębne typy: HAE, AE nabyty oraz ACEI-AAE.1
HAE
Większość przypadków HAE jest spowodowana mutacjami genu kodującego inhibitor esterazy C1 (C1-INH), których efektem jest małe stężenie C1-INH w osoczu (HAE typu I) lub prawidłowe stężenie C1-INH o upośledzonej czynności (HAE typu II).1 HAE występuje u około 1/50 000 osób w populacji ogólnej.22 Mechanizm HAE typu III – z prawidłowym stężeniem i prawidłową aktywnością C1-INH1 – nie został dotychczas w pełni wyjaśniony.24 Napady AE u chorych na HAE typu III są podobne do napadów u chorych z HAE typu I i II.
Nabyty AE
AE zależny od bradykininy może się rozwinąć w późniejszym okresie życia i jest nazywany nabytym AE. Występuje bardzo rzadko; chorobowość w populacji ogólnej szacuje się na 1/500 000–1/100 000.25 Objawy nabytego AE są takie same jak w przypadku HAE. Charakteryzuje się on tym, że niemal we wszystkich przypadkach rozpoznanie zostaje ustalone w 4. dekadzie życia lub później oraz często obserwuje się związek AE z towarzyszącą chorobą limfoproliferacyjną i/lub przeciwciałami skierowanymi przeciwko C1-INH.25
ACEI-AAE
Kolejną przyczyną AE zależnego od bradykininy są ACEI.26 Konwertaza angiotensyny jest jednym z 2 enzymów rozkładających bradykininę. ACEI mogą powodować nagromadzenie bradykininy, skutkujące AE – ACEI-AAE.26 Objawy ACEI-AAE występują zwykle w obrębie twarzy lub górnych odcinków dróg oddechowych i pokarmowych. Główną cechą charakterystyczną jest rumień (nieswędzący) utrzymujący się przez 24–72 godziny, z następczą samoistną remisją.27 Opublikowano pojedyncze doniesienia o rzadkiej manifestacji brzusznej.28 ACEI-AAE jako skutek uboczny stosowania ACEI występuje z częstością 0,1–0,7%, a w niektórych badaniach do 1,6%;29 w dużym badaniu amerykańskim stwierdzono zapadalność 0,2%30. Jako że częstość występowania chorób sercowo-naczyniowych rośnie z wiekiem, prawdopodobieństwo pojawienia się ACEI-AAE u chorych w wieku >40 lat jest większe.11 Wykazano, że ACEI-AAE występuje częściej u kobiet i osób rasy czarnej.30,31
AE związany z innymi lekami
Rzadszą przyczyną zwiększonego ryzyka wystąpienia
niehistaminergicznego AE są inne grupy
leków, w tym niesteroidowe leki przeciwzapalne
(NSLPZ), antybiotyki i blokery receptora angiotensynowego
(ARB).7,32 Szacuje się, że obrzęk
naczynioruchowy związany z NSLPZ występuje u 0,1–0,3% chorych przyjmujących te leki.33,34
Chorzy na astmę lub pokrzywkę przewlekłą są
znacznie bardziej narażeni i nawet u 35% z nich
dojdzie do rozwoju AE po przyjęciu NSLPZ. Istnieją liczne mechanizmy rozwoju AE wywołanego
przez NSLPZ, w tym hamowanie COX-1 prowadzące
do produkcji mediatorów zapalnych (leukotrienów
cysteinylowych) oraz nadwrażliwości IgE-zależnej.35 W przypadku AE wywołanego przez
NSLPZ odstawia się NSLPZ i stosuje leczenie
podobne jak w AE histaminergicznym. Zapadalność
na AE wywołany przez ARB na 1000 osobolat
wyniosła 1,66 (95% CI: 1,47–1,86).32
Wystąpienie niesymetrycznego AE w związku z podaniem rekombinowanego tkankowego aktywatora
plazminogenu (rtPA) w niedokrwiennym
udarze mózgu jest znanym zjawiskiem, opisywanym
już od czasu pierwszych doniesień dotyczących
tej metody leczenia.36 W zależności od ośrodka
częstość występowania AE wywołanego przez
rtPA u chorych z udarem niedokrwiennym mózgu
wynosi 1,2–5,1%.36-40 Co więcej, wydaje się, że jednoczesne
stosowanie ACEI zwiększa to ryzyko.36,37
Podanie rtPA nie tylko aktywuje składowe układu
dopełniacza, w tym histaminę, ale również prowadzi
do uwolnienia bradykininy za pośrednictwem
plazminy.40,41 AE wywołany przez rtPA zwykle
przebiega łagodnie i ustępuje w ciągu 24 godzin,
ale część przypadków ma charakter gwałtownie
postępujący i stanowi zagrożenie dla życia.
Rozróżnianie AE zależnego od histaminy i AE zależnego od bradykininy
W celu zapewnienia chorym właściwego leczenia niezbędne jest ustalenie przy przyjęciu przyczyny AE. Niestety nie ma obecnie zwalidowanych, szybkich przyłóżkowych testów diagnostycznych umożliwiających odróżnienie napadu histaminergicznego od AE zależnego od bradykininy. Istnieje jednak kilka cech różnicujących, które mogą ukierunkować na właściwe rozpoznanie (ryc. 221,42 oraz ryc. 3).
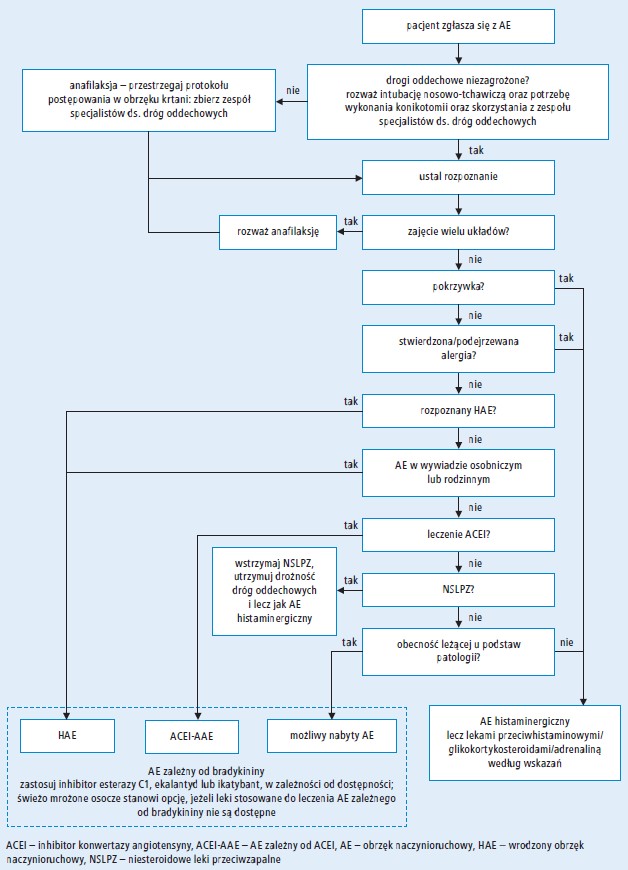
Ryc. 2. Schemat procesu diagnostycznego w obrzęku naczynioruchowym na szpitalnym oddziale ratunkowym21,42
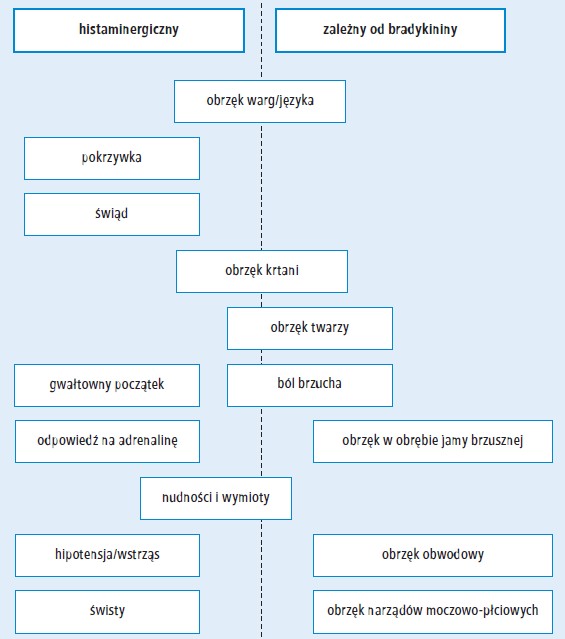
Ryc. 3. Różnicowanie obrzęku naczynioruchowego histaminergicznego i zależnego
od bradykininy
W AE histaminergicznym często występuje
pokrzywka. Niedawno opublikowane badanie
kanadyjskie wykazało, że u 29,8% chorych zgłaszających
się z AE wystąpiła również pokrzywka,
co miało istotny związek z czynnikiem wywołującym,
takim jak ukąszenia komarów oraz niektóre
pokarmy i leki (inne niż NSLPZ i ACEI).8
W AE zależnym od bradykininy (dziedzicznym ani ACEI-AAE; ryc. 3) pokrzywka nie występuje, zwykle
nie ma też świądu.
Szybkość rozwijania się obrzęku również może
stanowić czynnik różnicujący (ryc. 421). AE histaminergiczny
może się pojawiać szybko (≤1 h od narażenia
na alergen). Objawy wrodzonego lub nabytego
AE zwykle rozwijają się wolniej, w ciągu
kilku godzin, ale niekiedy mogą się pojawić szybko
albo sprawiać takie wrażenie (np. gdy napad zaczyna
się, kiedy chory śpi).
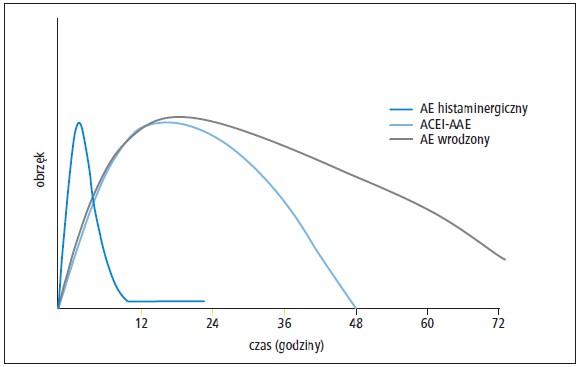
Ryc. 4. Schematyczny wykres przedstawiający początek i czas trwania napadu obrzęku
naczynioruchowego (AE). Napad AE histaminergicznego zwykle charakteryzuje się szybkim
początkiem i ustąpieniem. AE zależny od bradykininy zwykle rozwija się wolniej i może się
utrzymywać przez ≤5 dni, jednak AE zależny od ACEI (ACEI-AAE) zwykle ustępuje w ciągu
48 godzin po zaprzestaniu podawania leku
Nieleczony napad wrodzonego lub nabytego
AE jest zwykle cięższy i dłuższy niż napady
AE histaminergicznego; typowo utrzymuje się
przez 48–72 godzin, a czasem nawet do 5 dni.43
Co więcej, napady zależne od bradykininy wiążą
się z większym prawdopodobieństwem zajęcia
narządów jamy brzusznej (ryc. 3)21 – dotyczy jej
co najmniej 50% napadów.44 Jeżeli chory z wcześniej
rozpoznanym HAE zgłasza się z bólem i/lub
obrzękiem brzucha, w diagnostyce różnicowej należy
wziąć pod uwagę AE przewodu pokarmowego,
nawet jeżeli chory wcześniej nie przebył podobnych
napadów.45 Diagnostyka różnicowa jest znacznie
trudniejsza, jeśli wcześniej nie rozpoznano HAE.
Wywiad ma zasadnicze znaczenie u chorych zgłaszających
się z bólem brzucha. Nawracający ból i obrzęk brzucha, zwłaszcza z dodatnim wywiadem
rodzinnym w kierunku podobnych objawów, może
sugerować HAE.46
Odpowiedź na leczenie lekami przeciwhistaminowymi,
glikokortykosteroidami (GKS) i adrenaliną
może pomóc w odróżnieniu AE histaminergicznego
od AE zależnego od bradykininy.
AE histaminergiczny odpowiada na leczenie lekami
przeciwhistaminowymi, GKS i adrenaliną, w przeciwieństwie do AE zależnego od bradykininy
(w tym wrodzonego, nabytego i ACEI-AAE).
Chociaż odpowiedź na zastosowane leczenie lub jej
brak nie jest odpowiednią metodą diagnostyczną
na SOR, to efekt leczenia może stanowić cenną
wskazówkę kliniczną w dalszej obserwacji i diagnostyce.
Badania potwierdzające
Rozpoznanie wrodzonego lub nabytego AE można potwierdzić za pomocą badań krwi, lecz obecnie dostępne testy nie potwierdzą ACEI-AAE (tab. 1).1,21,47,48 U chorego zgłaszającego się z pierwszym w życiu izolowanym AE, z dodatnim wywiadem rodzinnym lub bez, należy rozważyć wykonanie przesiewowego pomiaru stężenia C4 w osoczu. Około 25% przypadków HAE może wynikać ze spontanicznej mutacji i w takich przypadkach wywiad rodzinny będzie ujemny. Wyniki badań krwi pobranej podczas napadu najprawdopodobniej nie będą dostępne odpowiednio wcześnie, by wspomóc podejmowanie decyzji na SOR, lecz mogą być użyteczne w dalszej obserwacji i późniejszym postępowaniu.
| Tabela 1. Wyniki testów diagnostycznych pomagających rozróżnić typy obrzęku naczynioruchowego1,21,47,48 | ||||
|---|---|---|---|---|
| Stężenie C1-INH | Aktywność C1-INH | Stężenie C4 | Stężenie tryptazya | |
| HAE typu 1 | małe | mała | małe | prawidłowe |
| HAE typu 2 | prawidłowe lub duże | mała | małe | prawidłowe |
| HAE z prawidłowym C1-INH | prawidłowe | prawidłowa | prawidłowe | prawidłowe |
| AE nabyty | małe | mała | małe | prawidłowe |
| ACEI-AAE | prawidłowe | prawidłowa | prawidłowe | prawidłowe |
| anafilaksja wywołana histaminą | prawidłowe | prawidłowa | prawidłowe | prawidłowe lub zwiększone |
| a we krwi pobranej w ciągu 4–6 h od początku napadu
ACEI-AAE – obrzęk naczynioruchowy zależny od inhibitora konwertazy angiotensyny, AE – obrzęk naczynioruchowy, C1-INH – inhibitor esterazy C1, HAE – wrodzony obrzęk naczynioruchowy | ||||
AE – postępowanie na SOR
Obraz kliniczny AE na SOR będzie się prawdopodobnie
mieścił w jednej z 4 kategorii:
1) obrzęk twarzy (w tym połowiczy) lub warg (ryc. 5A)
2) obrzęk języka (ryc. 5B)
3) obrzęk krtani
4) obrzęk, ból lub dyskomfort brzucha, który może być nasilony.
Obwodowy skórny AE również jest częsty,
jednak chorzy mogą nie przypisywać mu tego
samego poziomu ryzyka, co AE o innej lokalizacji, w związku z czym mogą się rzadziej zgłaszać
na SOR. Powyższe kategorie AE nie wykluczają
się wzajemnie; może dochodzić do jednoczesnego
obrzęku wielu miejsc.
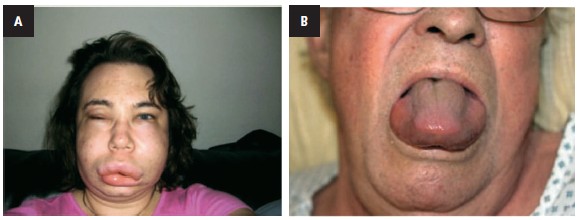
Ryc. 5. Obraz kliniczny obrzęku naczynioruchowego na oddziale ratunkowym. A – obrzęk
twarzy/warg (stopień 1 wg Ishoo). B – obrzęk języka (stopień 3 wg Ishoo). Zdjęcie A pochodzi z www.haeimages.com
Postępowanie z górnymi drogami oddechowymi
AE może postępować gwałtownie. W pierwszej
kolejności należy odpowiedzieć na pytanie, czy drożność dróg oddechowych nie jest zagrożona.
Jeżeli nie ma pewności co do tego i nie ma też
czasu na dalszą ocenę, należy postępować zgodnie z lokalnym protokołem postępowania w anafilaksji.
Może się okazać, że konieczna będzie intubacja
lub konikotomia/tracheotomia.42 U chorych ze świstem
krtaniowym (stridorem) lub chrypką należy
rozważyć badanie wziernikowe, optymalnie za pomocą
laryngoskopii nosowo-gardłowej, w celu oceny
stopnia obrzęku krtani.21 Intubacja jest konieczna
znacznie częściej w przypadku obrzęku krtani
lub gardła niż obrzęku warg i twarzy. Ogólnie się
przyjmuje, że jeśli obrzęk występuje do przodu
od zębów, wówczas najprawdopodobniej wystarczy
farmakoterapia, natomiast w przypadku obrzęku
tkanek za zębami należy rozważyć mechaniczne
zabezpieczenie dróg oddechowych.49 Częstość stosowania
intubacji zwiększa się z wiekiem.50
Jeżeli konieczna jest intubacja, w pierwszej kolejności
należy rozważyć drogę nosowo-gardłową
lub dotchawiczą.21 AE zależny od bradykininy często zajmuje wargi i język, co może spowodować
obturację odcinka ustno-gardłowego, a droga nosowa z dużym prawdopodobieństwem nie zostanie
zablokowana. W takich przypadkach przyrządy
nadgłośniowe (np. maski krtaniowe) nie są właściwe.
Złotym standardem zabezpieczania dróg oddechowych u przytomnego chorego z AE zależnym
od bradykininy jest intubacja nosowo-gardłowa.
AE zależny od bradykininy (wrodzony, nabyty,
ACEI-AAE) może być wyzwolony niewielkim
urazem, więc obrzęk jamy ustnej i krtani może
się nasilić po próbach wziernikowania i intubacji.
Zabezpieczenie dróg oddechowych u chorego z obrzękiem krtani wiąże się z ryzykiem. Przed
podjęciem próby intubacji należy wezwać zespół
doświadczony w intubacji nosowo-gardłowej oraz
ratunkowym, chirurgicznym udrażnianiu dróg
oddechowych.
Chociaż zapewnienie drożności dróg oddechowych
stanowi najwyższy priorytet, należy dążyć
do ustalenia przyczyny napadu AE (stwierdzona
wcześniej alergia na leki lub pokarmy, wrodzony
lub nabyty AE, stosowanie ACEI, wywiad rodzinny
itp.) w celu zapewnienia prawidłowego leczenia.
Leki stosowane w AE histaminergicznym
W przypadku AE histaminergicznego lub o nieokreślonej etiologii standardowe leczenie obejmuje stosowanie antagonistów receptorów H1 i H2 oraz GKS doustnych.21 Obrzęk dróg oddechowych lub hipotensja stanowią wskazania do domięśniowego podania adrenaliny w dawce 0,2–0,5 mg.51 W przypadkach innych niż anafilaksja adrenalina nie jest wskazana, jeśli nie ma objawów ze strony dróg oddechowych świadczących o potencjalnym zagrożeniu życia.
Leki stosowane w AE zależnym od bradykininy
W leczeniu ostrych napadów HAE można wybierać spośród kilku dostępnych leków (tab. 2). Chociaż nie zostały one zarejestrowane przez amerykański Urząd ds. Żywności i Leków (FDA) do leczenia AE nabytego lub wywołanego przez ACEI, to zakończone i trwające badania kliniczne wskazują na ich szerszą rolę w leczeniu napadów zależnych od bradykininy u chorych bez HAE.21,40 Dostępne są koncentraty C1-INH, pochodzące z gromadzonego osocza dawców. Hamują one aktywność czynnika XII i kalikreiny, co powoduje zmniejszenie wytwarzania bradykininy.21 Berinert® (CSL Behring, LLC, Kankakee, USA) został zarejestrowany w USA do leczenia ostrych brzusznych, twarzowych (obejmujących język i część ustną gardła) lub krtaniowych napadów HAE u dorosłych i dzieci. Cinryze® (Shire, Lexington, USA) został dopuszczony do stosowania w profilaktyce HAE u dorosłych i jest stosowany poza wskazaniami rejestracyjnymi w leczeniu napadów HAE. Ruconest ® (Salix Pharmaceuticals, Inc., Raleigh, USA) jest rekombinowanym C1-INH zarejestrowanym do leczenia ostrych napadów HAE u dorosłych i młodzieży.
| Tabela 2. Leczenie celowane wrodzonego obrzęku naczynioruchowego (HAE)21,63-66 | |||||
|---|---|---|---|---|---|
| Lek | Wskazanie zatwierdzone przez FDA | Mechanizm działania | Dawka/droga podania/cenaa | Czas do początku ustępowania objawów (mediana) | Działania niepożądane |
| osoczowy C1-INH (Berinert) | ostre napady HAE obejmujące brzuch, twarz lub krtań u dorosłych i dzieci (nie określono dolnej granicy wieku) | uzupełnienie białka C1-INH | 20 j./kg i.v. 8991 USD (1500 j.) | 48 min | częste: dysgeuzja rzadkie: anafilaksja, zakrzepica teoretyczne: zakażenia krwiopochodne |
| osoczowy C1-INH (Cinryze) | profilaktyka napadów HAE u dorosłych i dzieci w wieku ≥11 lat | uzupełnienie białka C1-INH | 1000 j. i.v. 5704 USD (1000 j.) | 30 min | częste: dysgeuzja rzadkie: anafilaksja, zakrzepica teoretyczne: zakażenia krwiopochodne |
| rekombinowany C1-INH (Ruconest) | ostre napady HAE u dorosłych i dzieci w wieku ≥11 lat; skuteczność niepotwierdzona w napadach krtaniowych | uzupełnienie białka C1-INH | 50 jedn./kg i.v.
12 142 USD (4200 IU) | 90 min | częste: zapalenie zatok przynosowych,
osutka, świąd rzadkie: anafilaksja |
| ekalantyd (Kalbitor)* | ostre napady HAE u chorych w wieku ≥12 lat | inhibitor kalikreiny osoczowej | 30 mg s.c. 14 090 USD (30 mg) | 67 min | częste: ból głowy, nudności, gorączka, reakcje w miejscu podania rzadkie: anafilaksja (konieczność podania przez personel medyczny) |
| ikatybant (Firazyr) | ostre napady HAE u osób w wieku ≥18 lat | antagonista receptora bradykininy typu 2 | 30 mg s.c. 10 037 USD (30 mg) | 2 h | częste: reakcje w miejscu podania, gorączka, zwiększona aktywność aminotransferaz, zawroty głowy
teoretyczne: pogorszenie trwającego napadu niedokrwienia |
| a ceny detaliczne w USA, na podstawie www.drugs.com z 05.04.2017 r.
* niezarejestrowany w Polsce – przyp. red. C1-INH – inhibitor esterazy C1, FDA – (amerykański) Urząd ds. Żywności i Leków | |||||
Kalbitor® (ekalantyd; Shire, Lexington, USA; niezarejestrowany w Polsce – przyp. red.) to rekombinowany osoczowy inhibitor kalikreiny, zmodyfikowany genetycznie tak, by wpływać na wytwarzanie bradykininy przez kalikreinę. Lek ten dopuszczono do stosowania w ostrych napadach HAE u chorych w wieku >12 lat. Podczas badań klinicznych u 3% chorych otrzymujących ten lek rozwinęła się anafilaksja, stąd uznano za konieczne podawanie go przez personel medyczny wyszkolony w postępowaniu w reakcjach nadwrażliwości, a także obserwację chorego przez co najmniej 1 godzinę po podaniu.21 Ikatybant to syntetyczny, selektywny antagonista receptora bradykininy typu 2, który hamuje działanie naczyniowe bradykininy i został zarejestrowany do leczenia napadów HAE. Może być podawany podskórnie przez samych chorych albo przez lekarza.21 Nie przeprowadzono badań bezpośrednio porównujących wyżej wymienione leki. Około 10% chorych może wymagać drugiej dawki z powodu niepełnej odpowiedzi lub nawrotu objawów.21,40,41,52 Niedawno opublikowano wyniki badań, w których stosowano ekalantyd lub ikatybant w ACEI-AAE. Lewis i wsp. porównali dołączenie ekalantydu do standardowego leczenia u chorych z lekkim lub umiarkowanym ACEI-AAE, a punkt końcowy stanowiła możliwość wypisania chorego w ciągu pierwszych 6 godzin od zastosowania leczenia. Nie stwierdzono znamiennej różnicy pod tym względem między grupą otrzymującą ekalantyd i grupą placebo.53 Bernstein i wsp. przyjęli krótszy czas do wypisu jako punkt końcowy: w ich badaniu do 4 godzin od zastosowania leczenia zostało wypisanych 8 z 26 (31%) chorych otrzymujących ekalantyd i 5 z 24 (21%) chorych otrzymujących placebo (95% CI: od –14 do 34%).52 Bas i wsp. wykazali istotnie krótszy czas do ustąpienia objawów u chorych, którym podano ikatybant, w porównaniu z chorymi leczonymi standardowo GKS i lekami przeciwhistaminowymi (odpowiednio 2,0 vs 11,7 h; p = 0,03),40 co potwierdziło wyniki serii przypadków.54 Choć niezarejestrowane przez FDA do leczenia ostrych objawów, świeżo mrożone osocze (FFP) również można zastosować w leczeniu ACEI-AAE i innych postaci AE zależnego od bradykininy. FFP zapewnia uzupełnienie objętości wewnątrznaczyniowej i jest skuteczne w większości przypadków AE zależnego od bradykininy. Objawy zaczynają ustępować w ciągu 30–90 minut od podania FFP.55 Ponadto FFP jest tańsze niż leczenie celowane, ale może wywołać reakcję nadwrażliwości oraz – rzadko – nasilenie objawów AE.21,22 Stosowanie antagonistów receptorów H1 i H2, GKS doustnych oraz adrenaliny wiąże się z małym prawdopodobieństwem uzyskania poprawy w przypadku AE zależnego od bradykininy.21 W AE wywołanym przez tPA podstawą leczenia pozostawało do tej pory dożylne podawanie GKS i leków przeciwhistaminowych. Wobec skuteczności nowych terapii, takich jak ikatybant i ekalantyd, u chorych z HAE lub ACEI-AAE, leki te mogą się też okazać przydatne w AE związanym z leczeniem trombolitycznym.
Wypis
Chorych bez obrzęku języka lub krtani i bez innych
zagrożeń drożności dróg oddechowych (stopień 1 wg Ishoo; klasyfikacja Ishoo nie została
zwalidowana, lecz może stanowić wskazówkę)
można wypisać po kilku godzinach obserwacji
(≥2–6 h lub dłużej w razie potrzeby), która jest
konieczna dla upewnienia się, że objawy zaczęły
ustępować i nic nie wskazuje na rozwój obturacji dróg oddechowych. Nie należy natomiast wypisywać
chorego ze szpitala, jeżeli stan dróg oddechowych
oceniono na stopień >1 według Ishoo.
Chorych z lekkim AE warg można wypisać z zaleceniem
swoistego leczenia, jeżeli objawy się nie nasilają.21,49 Przy wypisie, o ile to możliwe, chorym
należy przepisać odpowiednie leki umożliwiające
kontrolę nawracających objawów oraz wydać skierowanie
na wizytę kontrolną.21
W przypadku chorych z AE histaminergicznym
lub nieokreślonym zalecenia wypisowe
powinny obejmować adrenalinę i dalszą obserwację
przez specjalistę w dziedzinie AE w celu
ustalenia właściwego leczenia.21 Chorzy z HAE
powinni mieć dostęp do leczenia celowanego,
które można zastosować poza placówkami opieki
zdrowotnej, np. ikatybantu lub inhibitora C1-INH. U chorych z niehistaminergicznym AE należy niezwłocznie
zaprzestać stosowania ACEI i zastąpić
je alternatywnym lekiem o innym mechanizmie
działania. Chorych należy poinformować, że AE
może wystąpić lub nawrócić w ciągu kilku tygodni
po odstawieniu ACEI.56 U chorych, u których
wystąpił zagrażający życiu napad AE, należy
unikać stosowania zarówno ACEI, jak i ARB. U chorych ze słabszą reakcją po przyjęciu ACEI
można zastosować jako lek alternatywny ARB
(pod warunkiem ścisłej obserwacji, jeżeli współistnieje
choroba, w której zahamowanie układu
renina–angiotensyna–aldosteron jest szczególnie
korzystne, jak na przykład w przewlekłej niewydolności
serca.36,39
Obserwacja
Chorych bez wcześniej ustalonego rozpoznania powinno się przy wypisie skierować do lekarza podstawowej opieki zdrowotnej, specjalisty w dziedzinie immunologii lub do poradni alergologicznej w zależności od podejrzewanej przyczyny AE. Jeżeli istnieje podejrzenie HAE, chorego należy skierować do immunologa mającego doświadczenie w postępowaniu w HAE, w celu potwierdzenia rozpoznania i omówienia możliwości leczenia profilaktycznego i doraźnego.21 Wyniki badań krwi pobranej na SOR podczas napadu AE, chociaż zwykle nie ułatwiają doraźnego leczenia, mogą być wartościowe dla dalszego postępowania ambulatoryjnego.
Przygotowanie SOR
Dla zapewnienia optymalnego leczenia chorych zgłaszających się z AE w każdym SOR powinny się znaleźć – w widocznym lub łatwo dostępnym miejscu – ustalony protokół oraz algorytm lub plan postępowania. Niedawno opublikowane krajowe i międzynarodowe wytyczne mogą stanowić dobrą podstawę takiego planu.18,21,22,42,43,47,48,57-61 Poza szkoleniem personelu w rozpoznawaniu, różnicowaniu i leczeniu AE na SOR zasadnicze znaczenie ma dostęp do skutecznych i dobrze tolerowanych leków stosowanych w AE zależnym od bradykininy.
Wnioski
AE jest stosunkowo częstą przyczyną zgłaszania się na SOR i może prowadzić do zgonu. Postępowanie w AE na SOR rozpoczyna się od oceny i zabezpieczenia dróg oddechowych z jednoczesnym włączeniem swoistego leczenia. Dla zapewnienia właściwego leczenia i dalszego postępowania konieczne jest określenie, czy mamy do czynienia z AE histaminergicznym czy z AE zależnym od bradykininy. Ponieważ nie ma wiarygodnych testów przyłóżkowych, lekarze SOR powinni znać cechy różnicujące te 2 choroby, co może ułatwić podejmowanie decyzji terapeutycznych. W leczeniu AE histaminergicznego powinno się stosować antagonistów receptorów H1 i H2 i GKS doustne oraz – w razie potrzeby – adrenalinę. Chorzy z HAE powinni otrzymać lek wskazany w leczeniu HAE, na przykład inhibitor C1-INH, ekalantyd lub ikatybant. W pozostałych postaciach AE zależnego od bradykininy można stosować FFP. Szpitale powinny zapewnić dostępność odpowiednich procedur i leków w miejscu leczenia AE.
Piśmiennictwo:
1. Bernstein J.A., Moellman J.: Emerging concepts in the diagnosis and treatment of patients with undifferentiated angioedema. Int. J. Emerg. Med., 2012; 5: 392. Kelly M., Donnelly J.P., McAnnally J.R., Wang H.E.: National estimates of emergency department visits for angioedema and allergic reactions in the United States. Allergy Asthma Proc., 2013; 34: 150–154
3. Bernstein J.A.: HAE update: epidemiology and burden of disease. Allergy Asthma Proc., 2013; 34: 3–6
4. Lombardi C., Crivellaro M., Dama A., Senna G., Gargioni S., Passalacqua G.: Are physicians aware of the side effects of angiotensin-converting enzyme inhibitors? A questionnaire survey in different medical categories. Chest, 2005; 128: 976–979
5. Zilberberg M.D., Jacobsen T., Tillotson G.: The burden of hospitalizations and emergency department visits with hereditary angioedema and angioedema in the United States, 2007. Allergy Asthma Proc., 2010; 31: 511–519
6. Zilberberg M.D., Nathanson B.H., Jacobsen T., Tillotson G.: Descriptive epidemiology of hereditary angioedema emergency department visits in the United States, 2006–2007. Allergy Asthma Proc., 2011; 32: 390–394
7. Bertazzoni G., Spina M.T., Scarpellini M.G., Buccelletti F., De Simone M., Gregori M., et al.: Drug-induced angioedema: experience of Italian emergency departments. Intern. Emerg. Med., 2014; 9: 455–462
8. Felder S., Curtis R.M., Ball I., Borici-Mazi R.: Prognostic factors in outcome of angioedema in the emergency department. Allergy Asthma Proc., 2014; 35: 362–370
9. Jolles S., Williams P., Carne E., Mian H., Huissoon A., Wong G., et al.: A UK national audit of hereditary and acquired angioedema. Clin. Exp. Immunol., 2014; 175: 59–67
10. Banerji A., Clark S., Blanda M., LoVecchio F., Snyder B., Camargo Jr C.A.: Multicenter study of patients with angiotensin-converting enzyme inhibitor-induced angioedema who present to the emergency department. Ann. Allergy Asthma Immunol., 2008; 100: 327–332
11. Bluestein H.M., Hoover T.A., Banerji A.S., Camargo Jr C.A., Reshef A., Herscu P.: Angiotensin-converting enzyme inhibitor-induced angioedema in a community hospital emergency department. Ann. Allergy Asthma Immunol., 2009; 103: 502–507
12. Gang C., Lindsell C.J., Moellman J., Sublett W., Hart K., Collins S., et al.: Factors associated with hospitalization of patients with angiotensin-converting enzyme inhibitor-induced angioedema. Allergy Asthma Proc., 2013; 34: 267–273
13. Holm J.P., Ovesen T.: Increasing rate of angiotensin-converting enzyme inhibitor-related upper airway angio-oedema. Dan. Med. J., 2012; 59: A4449
14. Williams-Johnson J.A., Hemmings S., Williams E.W., Channer G., McDonald A.H.: Six years experience of angioedema at the University Hospital of the West Indies. West Indian. Med. J., 2007; 56: 278–281
15. Lin R.Y., Levine R.J., Lin H.: Adverse drug effects and angioedema hospitalizations in the United States from 2000 to 2009. Allergy Asthma Proc., 2013; 34: 65–71
16. Lin R.Y., Shah S.N.: Increasing hospitalizations due to angioedema in the United States. Ann. Allergy Asthma Immunol., 2008; 101: 185–192
17. Bork K., Hardt J., Witzke G.: Fatal laryngeal attacks and mortality in hereditary angioedema due to C1-INH deficiency. J. Allergy Clin. Immunol., 2012; 130: 692–697
18. Jaiganesh T., Hughan C., Webster A., Bethune C.: Hereditary angioedema: a survey of UK emergency departments and recommendations for management. Eur. J. Emerg. Med., 2012; 19: 271–274
19. Brown N.J., Snowden M., Griffin M.R.: Recurrent angiotensin-converting enzyme inhibitor – associated angioedema. JAMA, 1997; 278: 232–233
20. Roberts D.S., Mahoney E.J., Hutchinson C.T., Aliphas A., Grundfast K.M.: Analysis of recurrent angiotensin converting enzyme inhibitor-induced angioedema. Laryngoscope, 2008; 118: 2115–2120
21. Moellman J.J., Bernstein J.A., Lindsell C., Banerji A., Busse P.J., Camargo C.A., Jr., et al.; American College of Allergy Asthma & Immunology (ACAAI); Society for Academic Emergency Medicine (SAEM): A consensus parameter for the evaluation and management of angioedema in the emergency department. Acad. Emerg. Med., 2014; 21: 469–484
22. Zuraw B.L., Banerji A., Bernstein J.A., Busse P.J., Christiansen S.C., Davis-Lorton M., et al.: US Hereditary Angioedema Association Medical Advisory Board. US Hereditary Angioedema Association Medical Advisory Board 2013 recommendations for the management of hereditary angioedema due to C1 inhibitor deficiency. J. Allergy Clin. Immunol. Pract., 2013; 1: 458–467
23. Cicardi M., Bergamaschini L., Zingale L.C., Gioffré D., Agostoni A.: Idiopathic nonhistaminergic angioedema. Am. J. Med., 1999; 106: 650–654
24. Dewald G., Bork K.: Missense mutations in the coagulation factor XII (Hageman factor) gene in hereditary angioedema with normal C1 inhibitor. Biochem. Biophys. Res. Commun., 2006; 343: 1286–1289
25. Cicardi M., Zanichelli A.: Acquired angioedema. Allergy Asthma Clin. Immunol., 2010; 6: 14
26. Kaplan A.P., Joseph K., Silverberg M.: Pathways for bradykinin formation and inflammatory disease. J. Allergy Clin. Immunol., 2002; 109: 195–209
27. Zuraw B.L., Bernstein J.A., Lang D.M., Craig T., Dreyfus D., Hsieh F., et al.: A focused parameter update: hereditary angioedema, acquired C1 inhibitor deficiency, and angiotensin-converting enzyme inhibitor-associated angioedema. J. Allergy Clin. Immunol., 2013; 131: 1491–1493
28. Benson B.C., Smith C., Laczek J.T.: Angiotensin converting enzyme inhibitorinduced gastrointestinal angioedema: a case series and literature review. J. Clin. Gastroenterol., 2013; 47: 844–849
29. Brown N.J., Ray W.A., Snowden M., Griffin M.R.: Black Americans have an increased rate of angiotensin converting enzyme inhibitor-associated angioedema. Clin. Pharmacol. Ther., 1996; 60: 8–13
30. Miller D.R., Oliveria S.A., Berlowitz D.R., Fincke B.G., Stang P., Lillienfeld D.E.: Angioedema incidence in US veterans initiating angiotensin-converting enzyme inhibitors. Hypertension, 2008; 51: 1624–1630
31. Malde B., Regalado J., Greenberger P.A.: Investigation of angioedema associated with the use of angiotensin-converting enzyme inhibitors and angiotensin receptor blockers. Ann. Allergy Asthma Immunol., 2007; 98: 57–63
32. Toh S., Reichman M.E., Houstoun M., Ross Southworth M., Ding X., Hernandez A.F., et al.: Comparative risk for angioedema associated with the use of drugs that target the renin-angiotensin-aldosterone system. Arch. Intern. Med., 2012; 172: 1582–1589
33. Strom B.L., Carson J.L., Morse M.L., West S.L., Soper K.A.: The effect of indication on hypersensitivity reactions associated with zomepirac sodium and other nonsteroidal antiinflammatory drugs. Arthritis Rheum., 1987; 30: 1142–1148
34. Settipane G.A.: Aspirin and allergic diseases: a review. Am. J. Med., 1983; 74: 102–109
35. Asero R.: Clinical management of adult patients with a history of nonsteroidal anti-inflammatory drug-induced urticaria/angioedema: update. Allergy Asthma Clin. Immunol., 2007; 3: 24–30
36. Beavers C.J., Dunn S.P., Macaulay T.E.: The role of angiotensin receptor blockers in patients with angiotensin-converting enzyme inhibitor-induced angioedema. Ann. Pharmacother., 2011; 45: 520–524
37. Kidney Disease Outcomes Quality Initiative (K/DOQI): K/DOQI clinical practice guidelines on hypertension and antihypertensive agents in chronic kidney disease. Am. J. Kidney Dis., 2004; 43 (suppl. 1): S1–S290
38. Bas M., Greve J., Strassen U., Khosravani F., Hoffmann T.K., Kojda G.: Angioedema induced by cardiovascular drugs: new players join old friends. Allergy, 2015; 70: 1196–1200
39. Bezalel S., Mahlab-Guri K., Asher I., Werner B., Sthoeger Z.M.: Angiotensinconverting enzyme inhibitor-induced angioedema. Am. J. Med., 2015; 128: 120–125
40. Baş M., Hoffmann T.K., Kojda G.: Icatibant in ACE-inhibitor-induced angioedema. N. Engl. J. Med., 2015; 372: 1867–1868
41. Li H.H., Campion M., Craig T.J., Soteres D.F., Riedl M., Lumry W.R., et al.: Analysis of hereditary angioedema attacks requiring a second dose of ecallantide. Ann. Allergy Asthma Immunol., 2013; 110: 168–172
42. Jaiganesh T., Wiese M., Hollingsworth J., Hughan C., Kamara M., Wood P., et al.: Acute angioedema: recognition and management in the emergency department. Eur. J. Emerg. Med., 2013; 20: 10–17
43. Caballero T., Baeza M.L., Cabanas R., Campos A., Cimbollek S., Gómez-Traseira C., et al.; Spanish Study Group on Bradykinin-Induced Angioedema; Grupo Espanol de Estudio del Angioedema mediado por Bradicinina: Consensus statement on the diagnosis, management, and treatment of angioedema mediated by bradykinin. Part I. Classification, epidemiology, pathophysiology, genetics, clinical symptoms, and diagnosis. J. Investig. Allergol. Clin. Immunol., 2011; 21: 333–347; quiz 47
44. Rubinstein E., Stolz L.E., Sheffer A.L., Stevens C., Bousvaros A.: Abdominal attacks and treatment in hereditary angioedema with C1-inhibitor deficiency. BMC Gastroenterol., 2014; 14: 71
45. Jalaj S., Scolapio J.S.: Gastrointestinal manifestations, diagnosis, and management of hereditary angioedema. J. Clin. Gastroenterol., 2013; 47: 817–823
46. Bork K., Staubach P., Eckardt A.J., Hardt J.: Symptoms, course, and complications of abdominal attacks in hereditary angioedema due to C1 inhibitor deficiency. Am. J. Gastroenterol., 2006; 101: 619–627
47. Craig T., Aygören-Pürsün E., Bork K., Bowen T., Boysen H., Farkas H., et al.: WAO guideline for the management of hereditary angioedema. World Allergy Organ. J., 2012; 5: 182–199
48. Lang D.M., Aberer W., Bernstein J.A., Chng H.H., Grumach A.S., Hide M., et al.: International consensus on hereditary and acquired angioedema. Ann. Allergy Asthma Immunol., 2012; 109: 395–402
49. Ishoo E., Shah U.K., Grillone G.A., Stram J.R., Fuleihan N.S.: Predicting airway risk in angioedema: staging system based on presentation. Otolaryngol. Head Neck Surg., 1999; 121: 263–268
50. Brook C.D., Devaiah A.K., Davis E.M.: Angioedema of the upper aerodigestive tract: risk factors associated with airway intervention and management algorithm. Int. Forum Allergy Rhinol., 2014; 4: 239–245
51. Tang A.W.: A practical guide to anaphylaxis. Am. Fam. Physician, 2003; 68: 1325–1332
52. Bernstein J.A., Moellman J.J., Collins S.P., Hart K.W., Lindsell C.J.: Effectiveness of ecallantide in treating angiotensin-converting enzyme inhibitor-induced angioedema in the emergency department. Ann. Allergy Asthma Immunol., 2015; 114: 245–249
53. Lewis L.M., Graffeo C., Crosley P., Klausner H.A., Clark C.L., Frank A., et al.: Ecallantide for the acute treatment of angiotensin-converting enzyme inhibitor-induced angioedema: a multicenter, randomized, controlled trial. Ann. Emerg. Med., 2015; 65: 204–213
54. Bas M., Greve J., Stelter K., Bier H., Stark T., Hoffmann T.K., et al.: Therapeutic efficacy of icatibant in angioedema induced by angiotensin-converting enzyme inhibitors: a case series. Ann. Emerg. Med., 2010; 56: 278–282
55. Prematta M., Gibbs J.G., Pratt E.L., Stoughton T.R., Craig T.J.: Fresh frozen plasma for the treatment of hereditary angioedema. Ann. Allergy Asthma Immunol., 2007; 98: 383–388
56. Beltrami L., Zanichelli A., Zingale L., Vacchini R., Carugo S., Cicardi M.: Longterm follow-up of 111 patients with angiotensin-converting enzyme inhibitor-related angioedema. J. Hypertens., 2011; 29: 2273–2277
57. Bas M., Greve J., Bier H., Knopf A., Stark T., Schuler P., et al.: Emergency management of acute angioedema [in German]. Dtsch Med. Wochenschr., 2010; 135: 1027–1031
58. Caballero T., Baeza M.L., Cabanas R., Campos A., Cimbollek S., Gómez-Traseira C., et al.; Spanish Study Group on Bradykinin-Induced Angioedema (SGBA): Consensus statement on the diagnosis, management, and treatment of angioedema mediated by bradykinin. Part II. Treatment, follow-up, and special situations. J. Investig. Allergol. Clin. Immunol., 2011; 21: 422–441; quiz 42–43
59. Cicardi M., Bork K., Caballero T., Craig T., Li H.H., Longhurst H., et al.; HAWK (Hereditary Angioedema International Working Group): Evidence-based recommendations for the therapeutic management of angioedema owing to hereditary C1 inhibitor deficiency: consensus report of an International Working Group. Allergy, 2012; 67: 147–157
60. Nosbaum A., Bouillet L., Floccard B., Javaud N., Launay D., Boccon-Gibod I., et al.; Groupe d’experts du CREAK; French National Center for Angioedema: Management of angiotensin-converting enzyme inhibitor-related angioedema: recommendations from the French National Center for Angioedema [in French]. Rev. Med. Interne, 2013; 34: 209–213
61. Cicardi M., Bellis P., Bertazzoni G., Cancian M., Chiesa M., Cremonesi P., et al.: Guidance for diagnosis and treatment of acute angioedema in the emergency department: consensus statement by a panel of Italian experts. Intern. Emerg. Med., 2014; 9: 85–92
62. Burton O.T., Oettgen H.C.: Beyond immediate hypersensitivity: evolving roles for IgE antibodies in immune homeostasis and allergic diseases. Immunol. Rev., 2011; 242: 128–143
63. Cruz M.P.: Conestat alfa (ruconest): first recombinant c1 esterase inhibitor for the treatment of acute attacks in patients with hereditary angioedema. P. T., 2015; 40: 109–114
64. Riedl M., Campion M., Horn P.T., Pullman W.E.: Response time for ecallantide treatment of acute hereditary angioedema attacks. Ann. Allergy Asthma Immunol., 2010; 105: 430–436
65. Longhurst H.J.: Management of acute attacks of hereditary angioedema: potential role of icatibant. Vasc. Health Risk Manag., 2010; 6: 795–802
66. Craig T.J., Levy R.J., Wasserman R.L., Bewtra A.K., Hurewitz D., Obtulowicz K., et al.: Efficacy of human C1 esterase inhibitor concentrate compared with placebo in acute hereditary angioedema attacks. J. Allergy Clin. Immunol., 2009; 124: 801–808
KOMENTARZ
prof. dr hab. n. med. Roman J. Nowicki
Katedra i Klinika Dermatologii, Wenerologii i Alergologii, Gdański Uniwersytet Medyczny
Jak cytować: Nowicki R.J.: Komentarz. W: Obrzęk naczynioruchowy na oddziale ratunkowym – praktyczny przewodnik po diagnostyce różnicowej i leczeniu. Med. Prakt., 2018; 7-8: 48–49
Skróty: AAE (acquired angioedema) – nabyty obrzęk naczynioruchowy, AE (angioedema) – obrzęk naczynioruchowy, C1-INH – inhibitor esterazy C1, HAE (hereditary angioedema) – wrodzony obrzęk naczynioruchowy
Obrzęk naczynioruchowy (angioedema – AE) to nagły
obrzęk tkanki podskórnej lub podśluzowej powstający w wyniku rozszerzenia i zwiększenia przepuszczalności
naczyń krwionośnych. AE typowo lokalizuje się w obrębie
powiek, czerwieni wargowej, okolic narządów płciowych i dalszych części kończyn, a także błony śluzowej
górnych dróg oddechowych i przewodu pokarmowego.
Szczególnie groźne dla życia jest wystąpienie obrzęku w obrębie górnych dróg oddechowych, które
może prowadzić do bolesnego połykania, zmiany barwy
głosu, chrypki, duszności i bezdechu (tab. I).1 Obrzęk błony
śluzowej przewodu pokarmowego i związane z tym
nasilone dolegliwości ze strony jamy brzusznej często
prowadzą do błędów diagnostycznych. AE ma charakter
nawrotowy, jest dobrze odgraniczony, niesymetryczny,
nieciastowaty (pod wpływem ucisku nie powstają dołki) i najczęściej ma charakter histaminergiczny (czyli zależny
od histaminy). U 40–50% chorych dorosłych AE histaminergiczny
współistnieje z pokrzywką (tab. II). Kobiety
chorują częściej niż mężczyźni. Trzeba jednak pamiętać
też o rzadziej występującej postaci AE zależnej od bradykininy,
wymagającej innego leczenia niż AE towarzyszący
pokrzywce. Aktualnie wyróżnia się 6 typów wrodzonego
(hereditary angioedema – HAE) i 4 typy nabytego obrzęku naczynioruchowego (acquired angioedema – AAE) bez towarzyszącej pokrzywki (tab. III).2,3
Rozpoznanie AE opiera się na wywiadzie osobniczym i rodzinnym, charakterystycznym obrazie klinicznym i na wynikach badań laboratoryjnych (tab. 1).
Brak poprawy po zastosowaniu leków przeciwhistaminowych,
glikokortykosteroidów i adrenaliny u chorych z AE jest ważną cechą różnicującą różne postaci obrzęku i może wskazywać na AE zależny od bradykininy.2-4
Leczenie ostrego napadu AE zależy od jego lokalizacji i nasilenia objawów. W stanie zagrożenia ostrą
niewydolnością oddechową, gdy występuje stridor lub
znaczny obrzęk twarzy i górnych dróg oddechowych, należy
rozważyć szybkie wykonanie intubacji dotchawiczej.
Chorych z ostrym obrzękiem gardła i górnych dróg oddechowych
powinno się obserwować przez ≥24 h. W przypadku
obrzęku żołądkowo-jelitowego stosuje się leki
przeciwbólowe, rozkurczowe i przeciwwymiotne oraz
nawadnianie dożylne. AE związany z pokrzywką lub
przyjęciem niesteroidowych leków przeciwzapalnych
leczy się tak jak ostrą pokrzywkę.
W leczeniu AE zależnego od bradykininy najskuteczniejsza i dostępna obecnie w Polsce jest substytucja
brakującego lub nieaktywnego inhibitora esterazy C1
(C1-INH) albo zastosowanie antagonisty receptora bradykininy.5
Leczenie napadu należy rozpocząć jak najszybciej.
Chorzy na HAE typu 1 lub 2 bądź C1-INH-AAE powinni
być przeszkoleni w technice podawania koncentratu
C1-INH, aby w razie pierwszych objawów obrzęku umieli
samodzielnie go sobie wstrzyknąć.
Profilaktyka krótkoterminowa (przedzabiegowa) u chorych poddawanych zabiegom związanym z uciskiem
lub naruszającym ciągłość górnego odcinka przewodu
pokarmowego lub dróg oddechowych polega na podaniu
1–6 godzin przed zabiegiem koncentratu C1-INH w dawce zależnej od masy ciała, jak w leczeniu ostrego
napadu HAE. Kolejna dawka powinna zostać przygotowana
do podania w razie potrzeby podczas zabiegu.
Profilaktyka długoterminowa może być wskazana w zależności od częstości napadów (zwykle >1/mies.),
ich ciężkości, jakości życia chorych, dostępności opieki
zdrowotnej i skuteczności leczenia ostrego obrzęku. Koncentrat
C1-INH jest lekiem z wyboru także podczas ciąży i karmienia piersią.2,4,5
| Tabela I. Skala nasilenia obrzęku naczynioruchowego w obrębie głowy i szyi wg Ishoo1 | |
|---|---|
| Stopień | Umiejscowienie i objawy |
| I | pokrzywka, obrzęk twarzy, obrzęk warg |
| II | obrzęk podniebienia miękkiego |
| III | obrzęk języka |
| IV | obrzęk krtani |
| Tabela II. Podział obrzęku naczynioruchowego z pokrzywką | |
|---|---|
| Postać | Przyczyna |
| alergiczny | leki, pokarmy, jady owadów |
| niealergiczny | niesteroidowe leki przeciwzapalne, radiologiczne środki cieniujące, eozynofilia idiopatyczna/zespół hipereozynofilowy, z pokrzywką wibracyjną (zawsze), z zimna (często), cholinergiczną (rzadko) lub słoneczną (rzadko), idiopatyczny |
| Tabela III. Aktualny podział obrzęku naczynioruchowego bez pokrzywki | ||
|---|---|---|
| wrodzony (HAE) | C1-INH-HAE (z niedoboru C1-INH) | HAE-1 (ze zmniejszonym stężeniem C1-INH) |
| HAE-2 (ze zmniejszoną aktywnością C1-INH) | ||
| nC1-INH-HAE (z prawidłowym C1-INH) | FXII-HAE (z mutacją genu czynnika XII) | |
| ANG-HAE (z mutacją genu angiopoetyny 1) | ||
| PLG-HAE (z mutacją genu plazminogenu) | ||
| UNK-HAE (o nieznanej etiologii) | ||
| nabyty (AAE) | idiopatyczny | IH-AAE (histaminergiczny) |
| InH-AAE (niehistaminergiczny) | ||
| o znanym mechanizmie | C1-INH-AAE (z niedoboru C1-INH) | |
| ACEI-AAE (wywołany przez ACEI) | ||
Piśmiennictwo do komentarza:
1. Ishoo E., Shah U.K., Grillone G.A. i wsp.: Predicting airway risk in angioedema: staging system based on presentation. Otolaryngol. Head Neck Surg., 1999; 121: 263–2682. Maurer M., Magerl M., Ansotegui I. i wsp.: The international WAO/EAACI guideline for the management of hereditary angioedema – the 2017 revision and update. Allergy, 2018; doi: 10.1111/ all.13 384
3. Porębski G., Gocki J., Juchacz A. i wsp.: Postępowanie we wrodzonym obrzęku naczynioruchowym z niedoboru inhibitora C1– stanowisko Sekcji HAE Polskiego Towarzystwa Alergologicznego. Część I: klasyfikacja, patofizjologia, objawy kliniczne i rozpoznanie. Alergol. Polska 2018; 5, 2: 98–108
4. Fu L., Kanani A., Lacuesta G. i wsp.: Canadian Physician Survey on the Medical Management of Hereditary Angioedema. Ann. Allergy Asthma Immunol., 2018; doi:10.1016/j.anai.2018.06.017
5. Porębski G., Gocki J., Juchacz A. i wsp.: Postępowanie we wrodzonym obrzęku naczynioruchowym z niedoboru inhibitora C1– stanowisko Sekcji HAE Polskiego Towarzystwa Alergologicznego. Część II: leczenie i zapobieganie napadom, monitorowanie choroby i postępowanie w sytuacjach szczególnych. Alergol. Polska, 2018; 5, 2: 109–120


