Wprowadzenie
Urazy głowy to jedna z najczęstszych przyczyn zgonów i ciężkiego kalectwa w krajach wysoko rozwiniętych. Powodują olbrzymie straty w kontekście społecznym i ekonomicznym.[1]
Rozróżnia się uraz pierwotny, czyli bezpośrednie zadziałanie czynnika niszczącego w momencie zdarzenia, oraz uraz wtórny, który rozwija się w ciągu kolejnych minut, godzin lub dni.
Zadanie ratownika medycznego stanowi ograniczenie zakresu urazu (tzw. neuroprotekcja) we wczesnym okresie, zarówno w fazie przedszpitalnej i transportu międzyszpitalnego, jak i leczenia w SOR (Szpitalny Oddział Ratunkowy).
Postępowanie ratownicze jest niestety nacechowane dużą zmiennością. Często ulegamy złudzeniu, że pacjent „został uratowany”, ponieważ dotarł żywy na salę operacyjną lub oddział intensywnej terapii. Z powodu braku oficjalnie przyjętych standardów postępowania i braku śledzenia losów pacjenta ( tzw. follow up), pozostajemy nieświadomi, jak wielu tych pacjentów umiera w sensie biologicznym lub/i społecznym.
Warto podkreślić, że każdy uratowany milimetr wrażliwej tkanki mózgowej ma olbrzymie znaczenie dla dalszych losów pacjenta – jego zdolności ruchowych, mówienia, pamięci, uczuć wyższych itd. Dlatego też postuluje się rozważenie poniżej opisanych czynności, a także wprowadzenie pełnego „pakietu anestezjologicznego” (opis poniżej) na wczesnym etapie leczenia zawsze wtedy, gdy jest to możliwe. Szybki transport do ośrodka docelowego (z oddziałem neurochirurgicznym) jest priorytetem.
U pacjentów po ciężkim urazie czaszkowo-mózgowym
- unikaj hipoksemii – Sat <90% [6] (dwukrotnie zwiększa śmiertelność!)
- rozważ potrzebę intubacji i wentylacji pod kontrolą kapnografii, utrzymując EtCO2 w dolnych granicach normy (35–40 mm Hg); hiperwentylacja (EtCO2 30–35 mm Hg) – tylko chwilowa (15 min) w przypadku oznak wklinowania [6,8]
- zastosuj obowiązkowo kapnografię (u pacjentów wentylowanych ); jej użycie zmniejsza śmiertelność spowodowaną m.in. powikłaniami jatrogennymi [9]!
- agresywnie zwalczaj hipotensję, uzyskując MAP >80, najlepiej przy maksymalnym CTK sk (skurczowym ciśnieniem tętniczym) <160 mm Hg [3] – jednorazowy epizod hipotensji z CTK sk <90 mm Hg dwukrotnie zwiększa śmiertelność! [5,6]; wyjątek: w przypadku politraumy ze wstrząsem krwotocznym (docelowe MAP? – brak danych, sugerowane utrzymywanie CTK sk, 100–120 mm Hg)
- utrzymuj normotermię, nie dopuszczaj do przegrzania pacjenta (cel – zwolnienie metabolizmu mózgu)! [6,7]
- rozważ podanie mannitolu 20%, ewentualnie 10% NaCl lub furosemidu (jest to jedno z bardziej kontrowersyjnych zaleceń) [5,6,8]
- skontroluj glikemię w każdym przypadku zaburzeń przytomności, w szczególności u dzieci; utrzymuj normoglikemię [8]
- zapewnij 2 duże wkłucia i.v. (16–17 G)
- poluźnij kołnierz ortopedyczny Schanza, popraw stabilizator rurki intubacyjnej, aby nie upośledzał powrotu żylnego z mózgowia [8]
- unieś głowę i tors o 15–30°, kiedy to tylko możliwe [8] (lub pozycja antytrendelendurga przy unieruchomieniu kręgosłupa); zmniejsza to ryzyko zachłyśnięcia przy intubacji, a także obniża ciśnienie śródczaszkowe
– każde zwiększenie CTK sk o 10 mm Hg w przedziale 40–119 mm Hg wiąże się ze zmniejszeniem śmiertelności o 18,8%! [11]
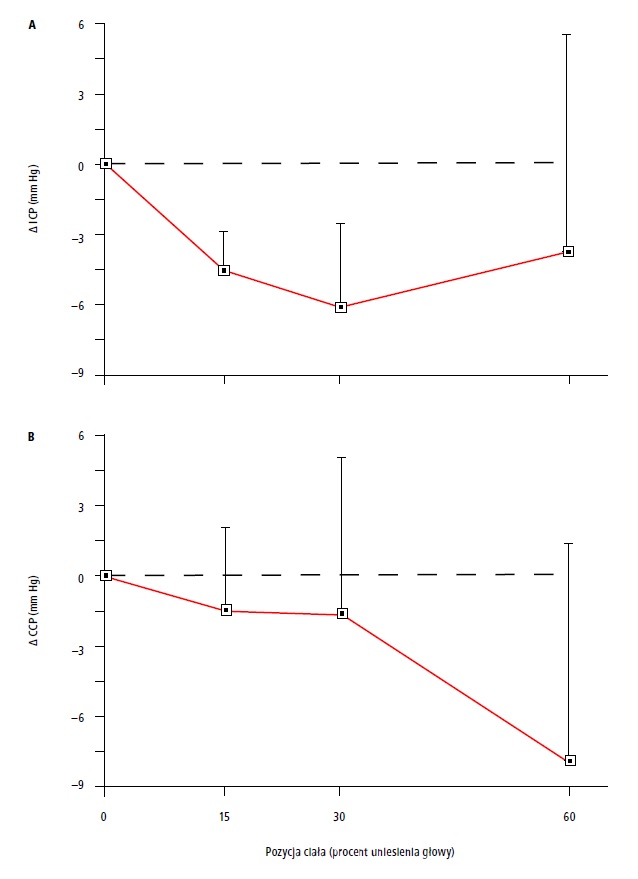
Ryc.1. Przy uniesieniu górnej połowy ciała obniża się ciśnienie śródczaszkowe ICP (najniższe przy ok. 30°). Jednocześnie nieznacznie obniża się ciśnienie perfuzyjne mózgu CPP (B), gwałtownie się załamując przy >30° uniesienia ciała.
- przed analgosedacją (midazolam i fentanyl z wyboru) i zwiotczeniem koniecznie zbadaj pacjenta neurologicznie. Badaj źrenice w regularnych odstępach czasu podczas transportu – wpisz do dokumentacji!
- zwalczaj drgawki lekami przeciwpadaczkowymi – np. klonazepam lub fenytoina i.v.
- wyklucz inne możliwe urazy towarzyszące; w szczególności: niezabezpieczone krwawienie, uraz rdzenia kręgowego ze wstrząsem neurogennym, odmę prężną
- podejmij decyzję o przewiezieniu do ośrodka z możliwością interwencji neurochirurgicznej (wg danych statystycznych – śmiertelność >90%, jeśli krwiak podtwardówkowy nie zostanie usunięty w ciągu 4 h, 30% jeśli zostanie usunięty w ciągu 4 h u ww. pacjentów)
- nie podawaj steroidów przy urazach czaszkowo-mózgowych. [4,8]
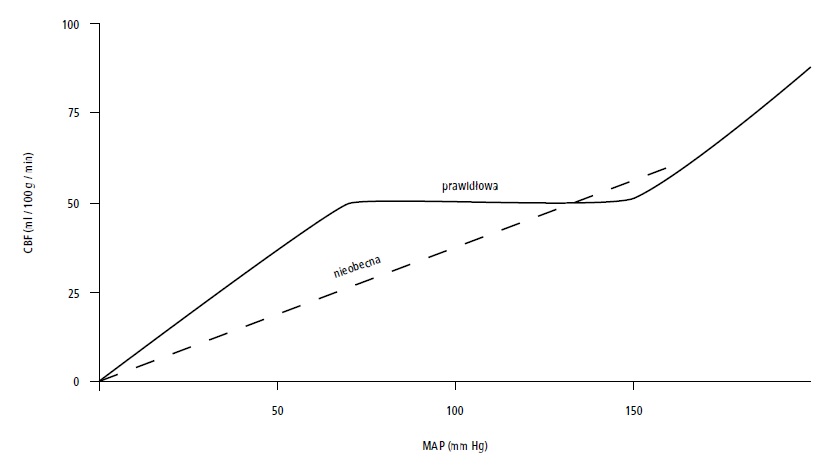
Ryc. 2. Podstawowy patomechanizm zniesionej autoregulacji mózgu (absent) w przypadku urazu czaszkowo-mózgowego. Zależność przepływu mózgowego (CBF) od średniego ciśnienia tętniczego krwi (MAP). Do utrzymania perfuzji mózgowej NIEZBĘDNY jest wyższy MAP.
Powyższe działania mają na celu zmniejszenie ryzyka wtórnego uszkodzenia OUN (tzw. działanie neuroprotekcyjne) – zmniejszenie metabolizmu mózgu, unikanie wzrostu ciśnienia śródczaszkowego oraz umożliwienie jak najszybszego usunięcia patologii wewnątrzczaszkowej (szybki transport do ośrodka interwencyjnego).
W przypadku występowania patologii wewnątrzczaszkowych w fazie nagłej dekompensacji ośrodkowego układu nerwowego (OUN) (oznaki wklinowania) tzn.: (1) jednostronne lub obustronne poszerzenie źrenicy z GCS (wynik w neurologicznej skali Glasgow) ≤8, (2) postępujący wzrost CTK i bradykardia z GCS ≤8 pacjent powinien być znieczulony, zaintubowany (lub alternatywnie zabezpieczone drogi oddechowe) i wentylowany mechanicznie. [1,6]
Na zagrożenie dekompensacją OUN wskazuje nagły spadek GCS co najmniej o 2 punkty (w tej fazie należy przygotować sprzęt i rozważyć intubację ze względu na spodziewany przebieg kliniczny – decyzje podejmowane są indywidualnie). [1]
Należy zapamiętać następujące dane statystyczne:
- u 13% pacjentów z urazem czaszkowo-mózgowym i 15 punktami w skali Glasgow dochodzi do śpiączki
- 12,5% pacjentów z początkowym GCS 13–14 wymaga interwencji neurochirurgicznej.
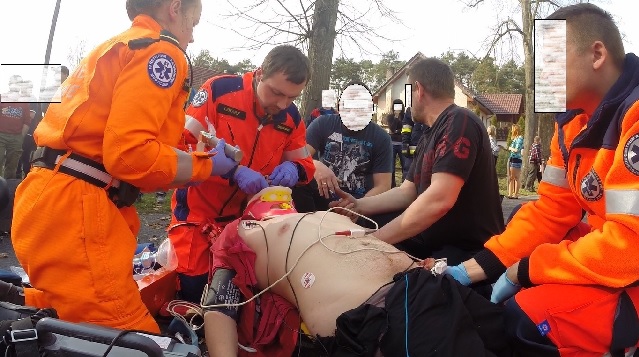
Ryc. 3. Szybka intubacja (rapid sequence intubation – RSI) motocyklisty w fazie przedszpitalnej. Natlenienie, przygotowanie farmakologiczne, pozycja antytlendelenburga, pełne monitorowanie z kapnografią.
PAMIETAJ! U pacjenta z patologią czaszkowo-mózgową należy agresywnie zwalczać: zwiększone ICP – ciśnienie śródczaszkowe, hipotensję, hipoksemię, hiperkapnię, hipokapnię, hipoglikemię, niestabilność krążeniową, zaburzenia rytmu, drgawki oraz gorączkę.
Najczęstsze błędy
- Brak odpowiedniej sedacji, analgezji, stosowanie u splątanego pacjenta wyłącznie metod siłowych (unieruchomienia)
- Brak zabezpieczenia dróg oddechowych u pacjenta nieprzytomnego (GCS ?8)
- Próby intubacji przez niedoświadczony personel; w efekcie powikłania
- Pozostawienie pacjenta na własnym oddechu lub wentylowanego mechanicznie bez zwiotczenia (kaszel i prężenia w trakcie wentylacji mechanicznej i odsysania = wzrost ICP i ryzyko przypadkowej ekstubacji w trakcie transportu)
- Brak monitorowania kapnografii
- Nieadekwatne leczenie hipotensji
- Brak reakcji w przypadku przegrzania pacjenta
- Ucisk na naczynia szyjne i brak uniesienia głowy pacjenta (lub pozycji antytrendelenburga)
- Wentylacja workiem samorozprężalnym bez dostarczania O2 w trakcie transportu; w efekcie hipoksemia
- Tendencja do hiperwentylacji workiem samorozprężalnym; w efekcie hipokapnia i nadmierne obkurczenie naczyń mózgowych.
Istotne wskazania do rozważenia intubacji przed transportem lotniczym u pacjentów z patologią OUN
1. GCS (skala Glasgow) ≤8
2. Dynamiczne pogorszenie świadomości – spadek GCS o ≥2 punkty
3. Utrata lub istotne zagrożenie utraty drożności dróg oddechowych
4. Hipoksemia
5. Hiperkapnia, bradypnoë
6.Hiperwentylacja z tachypnoë
7. Obustronne złamania twarzoczaszki (duży obrzęk +/- aktywne krwawienie)
8. Obfite krwawienie z ust (podejrzenie złamania podstawy czaszki)
9. Drgawki
„Pakiet anestezjologiczny”
Intubację powinien prowadzić doświadczony personel. W niedoświadczonych rękach laryngoskop powoduje więcej szkody niż korzyści. [10]
Wentylacja mechaniczna pacjenta na pokładzie śmigłowca powinna się odbywać z równoczesną analgosedacją i pełnym zwiotczeniem (czyli znieczuleniem ogólnym dożylnym). Zaleca się utrzymywać normoksemię (Sat>94%) oraz normokapnię w dolnych granicach normy. Należy także zbadać pacjenta neurologicznie przed indukcją znieczulenia!
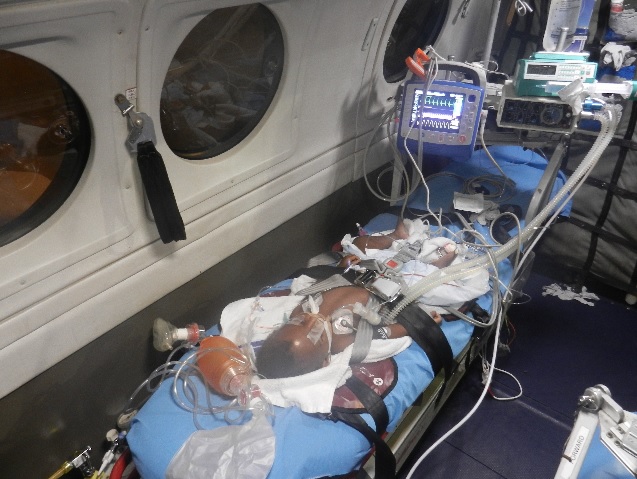
Ryc. 4. Transport międzyszpitalny dziecka z patologią wewnątrzczaszkową. Podtrzymanie znieczulenia ogólnego ze zwiotczeniem, pełne monitorowanie i kontrola temperatury. W przypadku pacjenta wentylowanego mechanicznie worek samorozprężalny z maską powinien być zawsze dostępny.
Leki do analgosedacji
- Fentanyl – podać przed intubacją (1–2 mcg/kg i.v.)
- Midazolam – działa sedacyjne i przeciwdrgawkowo 0,1–0,3 mg/kg i.v. [4]
- Ketamina – dane o przeciwwskazaniach w przypadku urazów czaszkowo-mózgowych są przestarzałe i niewiarygodne; lek przeciwbólowy i sedacyjny, który pozwala utrzymać perfuzję mózgową 0,5–2 mg/kg i.v. [2,4]
- Etomidat – minimalny wpływ na układ krążenia 0,2–0,3 mg/kg i.v.
- Propofol – w przypadku osób nieprzytomnych i/lub we wstrząsie – zalecana znaczna redukcja dawki – nawet do 90% wg niektórych autorów, uwaga na spadki CTK! 0,5–3 mg/kg i.v., przeciwwskazany do indukcji pacjentów we wstrząsie.
- Tiopental – obniża metabolizm mózgu, obecnie mało dostępny, 3–5 mg/kg i.v., powoduje spadki CTK.
Leki zwiotczające
- Chlorsukcynylocholina – powoduje przejściowe podwyższenie ciśnienia śródczaszkowego mało istotne klinicznie, 1,5 mg/kg i.v.
- Rokuronium w dawce 1,2 mg/kg i.v. zapewnia bardzo dobre warunki intubacyjne już po 1 minucie.
Patologia OUN u dzieci [6]
Pamiętaj! Stosuj pediatryczną skalę Glasgow (GCS – Glasgow Coma Scale)
| Tabela 1. Docelowe wartości MAP u dzieci | |
|---|---|
| wiek | MAP |
| 3. mies. | 40–60 |
| od 3 mies. do 1. rż. | 45–75 |
| 1.–5. r.ż. | 50–90 |
| 6.–11. rż. | 60–90 |
| 12.–14. rż. | 65–95 |
Najlepsza odpowiedź wzrokowa
- 4 pkt – otwiera oczy spontanicznie
- 3 pkt – otwiera oczy na polecenie głosowe
- 2 pkt – otwiera oczy w reakcji na ból
- 1 pkt – nie otwiera oczu.
Najlepsza odpowiedź słowna
- 5 pkt – uśmiecha się, wodzi wzrokiem
- 4 pkt – płacz ustępujący po przytuleniu
- 3 pkt – niespokojne w odpowiedzi na bodźce
- 2 pkt – pobudzone, niespokojne
- 1 pkt – brak odpowiedzi słownej.
Najlepsza odpowiedź ruchowa:
- 6 pkt – wykonuje polecenia
- 5 pkt – lokalizuje ból
- 4 pkt – odsuwa się od bólu
- 3 pkt – reakcja zgięciowa
- 2 pkt – reakcja wyprostna
- 1 pkt – brak odpowiedzi ruchowej
Odnośnie do skali GCS należy pamiętać, że punktacja poszczególnych komponentów jest istotniejsza niż całościowy wynik ogólny. Na przykład:
GCS 4 oznaczany jako 1+1+2 (oczy+słowa+ruch) oznacza śmiertelność 48% pacjentów, natomiast GCS 4 w postaci 2+1+1 (oczy+słowa+ruch) – śmiertelność 19%.
Wiarygodne badanie odruchów(czyli przed podaniem sedacji!) w postaci bardzo popularnej, prostej skali stwarza mnóstwo problemów. Szczególnie punkt 3, 4, 5 komponentu ruchowego, który jest prawidłowo oceniany przez tylko 50% neurochirurgów amerykańskich.
Komentarz dodatkowy: zespoły ratunkowe podstawowe
Podczas ratowania pacjentów nieprzytomnych i pobudzonych podstawowe zespoły ratunkowe mają przed sobą niezwykle trudne zadanie. Względy formalno-prawne ich dotyczące obecnie nie pozwalają na zastosowanie optymalnej neuroprotekcji w fazie przedszpitalnej. Kierownik zespołu w takich okolicznościach, uwzględniając bezpieczeństwo zespołu i pacjenta, powinien zadecydować, w jaki możliwie najszybszy sposób ww. warunki neuroprotekcji zostaną spełnione, tzn. transport do centrum urazowego lub SOR czy wezwanie na pomoc zespołu S/LPR?
Sedacja pacjenta w przypadku braku możliwości zaintubowania jest czynnością ryzykowną (możliwość aspiracji treści pokarmowej). W sytuacjach ratunkowych, gdy niewspółpracujący i pobudzony pacjent zagraża sobie i otoczeniu, a lekarz systemu nie jest dostępny, „pacyfikacja” farmakologiczna jest strategią wyboru mniejszego zła.
Jest to technika polecana tylko dla bardzo doświadczonych ratowników, którzy dokładnie znają skutki uboczne działania ww. leków i znają strategie zabezpieczania dróg oddechowych.
W takich okolicznościach należy podać przede wszystkim leki przeciwbólowe (morfina, fentanyl), w następnej kolejności nasenne (midazolam), skrupulatnie monitorować parametry życiowe i być przygotowanym na procedury udrażniające drogi oddechowe i zapewniające najlepszą możliwą wentylację pod obowiązkową kontrolą wydechowego CO2 (maska twarzowa z workiem samorozprężalnym i kapnografia)!
Użycie maski/rurki krtaniowej może się okazać niemożliwe w przypadku zachowanego odruchu gardłowego lub przy wzmożonym napięciu żwaczy.
Podsumowanie
U pacjentów z ciężkimi urazami czaszkowo-mózgowymi na etapie przedszpitalnym należy się skupić przede wszystkim na zapobieganiu urazowi wtórnemu i szybkim bezpiecznym transporcie poszkodowanego do odpowiedniej jednostki szpitalnej (z oddziałem neurochirurgii).
Do najważniejszych elementów postępowania należą: unikanie hipoksemii i hipotensji, które w największym stopniu wpływają na ograniczenie śmiertelności. Pozostałe wyżej wymienione w artykule czynności także decydują o przeżyciu pacjenta, ale przede wszystkim o jakości życia po urazie.
Powyższe wybrane aspekty postępowania mają charakter orientacyjny – są wersją bardzo uogólnioną i skróconą. Przy podejmowaniu decyzji klinicznych zalecane jest indywidualne podejście do każdego pacjenta.
O Autorze:
lek. Tomasz Derkowski - anestezjolog, intensywista, pasjonat medycyny przedszpitalnej. Doświadczenie zdobywał m.in. w Szpitalu Uniwersyteckim w Cambridge, w Szpitalu Wojskowym w Bydgoszczy, West Middlesex University Hospital w Londynie oraz Szpitalu Uniwersyteckim w Krakowie. Pracował w Anglii dla Cega Air Ambulance, w Australii dla Careflight HEMS i The Royal Flying Doctor Service oraz dla Lotniczego Pogotowia Ratunkowego (obecnie).
Piśmiennictwo:
1. Recommendations for the Safe Transfer of Patients with Brain Injury. The Association of Anaesthetists of Great Britain and Ireland, London 2006 .
2. Marland S., Ellerton J., Andolfatto G. i wsp.: Ketamine Use in Anaesthesia. CNS Neuroscience and Therapeutics, 2013: vol. 19 (6): 381–389.
3. Neeraj S. Naval, Robert D. Stevens, Marek A. Mirski i wsp.: Controversies in the management of aneurysmal subarachnoid hemorrhage. Critical Care Medicine, 2006: 34(2): 511-524.
4. Neuroprotection w: Helicopter Operating Procedure. NSW Aeromedical & Medical Retrieval Service, June 2011.
5. Bratton S., Bullock M., Carney N. i wsp.: Guidelines for the Management of Severe Traumatic Brain Injury Guidelines for the Management of Severe Traumatic Brain Injury. Brain Trauma Foundation, 2007; vol. 24.
6. Badjatia N., Carney N., Crocco T. i wsp.: Guidelines for Prehospital Management of Traumatic Brain Injury 2nd edition. Prehospital Emergency Care, 2007: vol. 12(Suppl. 1).
7. Broessner G., Fischer M., Schmutzhard E and B. i wsp.: Controlled prophylactic normothermia. Crit Care, 2012: 16(Suppl 2): A10.
8. Rangel-Castilla L., Gasco J., Hanbali F. i wsp.: Closed Head Injury Treatment & Management. Medscape , 2016.
9. Cook T., Woodall N., Frerk C. i wsp.: Major complications of airway management in the UK: results of the Fourth National Audit Project of the Royal College of Anaesthetists and the Difficult Airway Society. Part 1: Anaesthesia. Br J Anaesth (2011) 106 (5): 617-631.
10. Bossers S., Schwarte L., Loer S. i wsp.: Experience in Prehospital Endotracheal Intubation Significantly Influences Mortality of Patients with Severe Traumatic Brain Injury: A Systematic Review and Meta-Analysis. PLoS ONE 2015, doi: https://doi.org/10.1371/journal.pone.0141034.
11. Spaite D.W., Hu C., Bobrow B. J. i wsp.: Mortality and Prehospital Blood Pressure in Patients With Major Traumatic Brain Injury: Implications for the Hypotension Threshold. JAMA Surg, 2016 Dec 7, doi: https://www.ncbi.nlm.nih.gov/pubmed/27926759.
Piśmiennictwo zalecane:
1. Bhat, R., Hudson, K. & Sabzevari. T. (2008) An Evidence-Based Approach To Severe Traumatic Brain Injury. Emergency Medicine Practice: 10 (12)
2. Ellis, D.Y., Davies, G.E., Pearn, J. & Lockey, D. (2007) Pre hospital rapid-sequence intubation of patients with trauma with Glasgow Coma Score of 13 or 14 and the subsequent incidence of intracranial pathology. Emerg Med J: 24(2):139-41
3. Ellis, D.Y. & Hooper, M. (2010) Cases in Pre-Hospital and Retrieval Medicine. Elsevier, Australia.
4. Brain Trauma Foundation (2007), 3rd edt. Guidelines for the management of severe traumatic brain injury. New York.
5. Appleby, I. (2008). Traumatic brain injury: initial resuscitation and transfer. Anaesthesia and Intensive care medicine: 9 (5) 193-196
6. Kamel, H., Babak, B.N., Nakagawa., Hemphill, C. & Ko, N.U (2001). Hypertonic saline versus mannitol for the treatment of elevated intracranial pressure: a meta-analysis of randomised clinical trials. Critical Care Medicine; 39:554-559
7. Marko, N. (2012). Hypertonic saline, not mannitol, should be considered fold-standard medical therapy for intracranial hypertension. Critical Care; 16:113-115
8. Tan, P.G., Cincotta, M., Clavisi, O., Bragge., P., Wasiak, J., Pattuwage., L & Gruen, R.L. (2011). Pre hospital fluid management in traumatic brain injury. Emergency Medicine Australasia; 23:665-676
9. Hartl, R., Gerber, L, M., Iacono, L., Ni. Q., Lyons., K. & Ghajar. J. (2006) Direct transport within an organised state trauma system decreases mortality in patients with severe traumatic brain injury. Journal Trauma; 60:1250-1256
10. Moss, R., Porter, K. & Greaves, I (2013) Minimal patient handling: a faculty of pre hospital care consensus statement, BMJ; 30:12, 1065-1066
11. https://braintrauma.org/uploads/04/13/Prehospital_Guidelines_2nd_Edition_2.pdf - a long guideline but worth reading
12. Hulme, J. Resuscitation of patients after traumatic brain injury. Trauma 2008; 10:55-63 Moppett, I.K. Traumatic brain injury: assessment, resuscitation and early management. British Journal of Anaesthesia 2007; 99:18-31






