Około 20% kobiet w Polsce jest nosicielkami paciorkowca grupy B. U noworodka zakażenie paciorkowcem może powodować zapalenie płuc lub sepsę i prowadzić do śmierci. Dlatego u ciężarnych kobiet, nie wcześniej niż 5 tygodni przed porodem, wykonuje się badanie w kierunku zakażenia GBS. W przypadku uzyskania dodatniego wyniku stosuje się antybiotykoterapię śródporodową, która stanowi skuteczną metodę ochrony noworodka
Paciorkowiec grupy B w ciąży - przyczyna większości wczesnych zakażeń noworodków
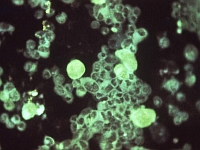
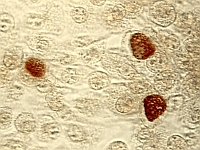
Paciorkowiec grupy B (Streptococcus agalactie lub group B streptococcus – GBS) jest bakterią odpowiedzialną obecnie za większość przypadków wczesnych zakażeń u noworodków, w tym ciężkich zakażeń zagrażających życiu. Bakteria ta jest jednym ze składników flory przewodu pokarmowego oraz pochwy u kobiet, a kolonizacja tym organizmem dotyczy od 10 do 30% ciężarnych. GBS u matki w większości przypadków nie wywołuje objawów chorobowych, ale może wywoływać infekcję układu moczowego, zapalenie błony śluzowej macicy czy błon płodowych i łożyska. Do zakażenia wertykalnego (z matki na dziecko) dochodzi wskutek migracji bakterii z pochwy do płynu owodniowego po rozpoczęciu się porodu lub po odejściu płynu owodniowego, wskutek aspiracji płynu owodniowego do płuc płodu oraz w czasie kontaktu dziecka z bakterią bytującą w pochwie (w tym ostatnim przypadku u większości noworodków dojdzie do kolonizacji, ale choroba się nie rozwinie).
Ile kobiet w ciąży jest nosicielem GBS i jak często dochodzi do zakażeń podczas porodu?
Przed wprowadzeniem rutynowych badań przesiewowych w kierunku nosicielstwa GBS, w USA stwierdzano corocznie ok. 7500 przypadków zakażenia u noworodków, z których blisko połowa kończyła się zgonem (początek lat 70.). Po wprowadzeniu (od 1996 r.) badań przesiewowych (i wdrożeniu odpowiedniego postępowania profilaktycznego) częstość występowania choroby znacznie się zmniejszyła.
W naszym kraju Polskie Towarzystwo Ginekologów i Położników w swych rekomendacjach zaleca prowadzenie tych badań u wszystkich ciężarnych kobiet. Ocenia się, że ok. od 10–30% (w Polsce średnio 20%) kobiet w ciąży jest nosicielami GBS w pochwie i/lub odbytnicy. Szacuje się, że ponad 50% nosicielek przekazuje bakterie noworodkom podczas porodu. Częstość wystąpienia jawnej choroby u noworodków matek nosicielek GBS, niepoddanych antybiotykoterapii profilaktycznej, ocenia się na 1–2% w Polsce średnia częstość wczesnej postaci zakażenia wynosi od 0,34–0,5 na 1000 żywych urodzeń.
Ryzyko infekcji paciorkowcami grupy B wzrasta w przypadku narodzin przed 37. tygodniem ciąży, przedłużającego się odpływania płynu owodniowego, młodego wieku matki, rasy czarnej matki, zakażenia wewnątrzowodniowego oraz bardzo małej masy urodzeniowej noworodka.
GBS w ciąży - przyczyny
Według najnowszych doniesień nosicielstwo GBS może być związane z niekorzystnymi zdarzeniami w ciąży (np. porodem przedwczesnym), szczególnie gdy u kobiety obserwuje się paciorkowce grupy B obecne w moczu. Zaobserwowano, że kolonizacja ma charakter nawrotowy w kolejnych ciążach u prawie 1/3 kobiet. Stwierdzenie obecności GBS w moczu (u każdej ciężarnej należy w I trymestrze wykonać badanie mikrobiologiczne moczu) jest wykładnikiem tzw. masywnej kolonizacji i stanowi czynnik dużego ryzyka wystąpienia wczesnej postaci zakażenia GBS u noworodka.
Zakażenie GBS w ciąży - śmiertelność
Śródporodowe zakażenie GBS może spowodować u noworodka sepsę i zapalenie płuc, rzadziej zapalenie opon mózgowo-rdzeniowych. Śmiertelność z powodu tych powikłań jest znacznie mniejsza niż wcześniej (obecnie wynosi 4–6%) i jest wynikiem znacznego postępu w opiece nad noworodkiem. Cięższy przebieg choroby i większą śmiertelność obserwuje się u wcześniaków.
Badanie GBS w ciąży
U wszystkich kobiet należy przeprowadzić badanie w kierunku nosicielstwa GBS nie wcześniej niż 5 tygodni przed spodziewanym porodem. Oznacza to, że badanie wykonuje się pomiędzy 35. a 37. tygodniem ciąży (wg wytycznych ACOG z 2019 r. między 36. + 0/7 a 36. + 6/7 tygodniem ciąży), niezależnie od przewidywanej drogi porodu. Wyjątek stanowią kobiety, u których zaleca się prowadzenie śródporodowej profilaktyki bez konieczności wykonania badań przesiewowych (kobiety, które urodziły już dziecko z sepsą GBS oraz kobiety, u których w obecnej ciąży stwierdza się GBS w moczu – bacteriuria). Nie zaleca się próby eradykacji nosicielstwa (czyli likwidacji bakterii z organizmu) przed porodem, gdyż po zakończeniu leczenia dochodzi zwykle do szybkiego nawrotu (wyjątkiem jest wdrożenie antybiotykoterapii w przypadku zakażenia dróg moczowych).
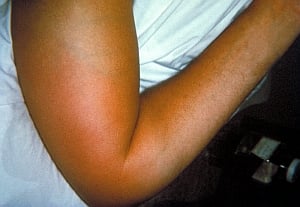 Ryc. 1. Łokieć pacjentki zakażonej paciorkowcem grupy B Fot. Public Health Image Library (PHIL)
Ryc. 1. Łokieć pacjentki zakażonej paciorkowcem grupy B Fot. Public Health Image Library (PHIL)
Próbki do badania w kierunku GBS (tak powinien być oznaczony materiał przesłany do pracowni mikrobiologicznej) pobiera się jałowymi wymazówkami z dolnej 1/3 części pochwy (bez konieczności zakładania wziernika) oraz z odbytnicy (pobierając próbkę, należy wprowadzić wymazówkę do odbytnicy, pokonując opór zwieracza odbytu). Sądzi się, że pobieranie materiału z okolicy okołoodbytniczej (bez penetracji zwieracza) skutkuje podobną skutecznością wykrywania nosicielstwa, ale metoda ta nie jest zalecana przez towarzystwa naukowe. U kobiet uczulonych na penicylinę z dużym ryzykiem wstrząsu anafilaktycznego (informację o tym trzeba umieścić na skierowaniu) należy oznaczyć wrażliwość GBS na klindamycynę i erytromycynę.
W dobrze prowadzonych laboratoriach mikrobiologicznych (stosujących kontrolę jakości) nie ma potrzeby oznaczania wrażliwości na penicylinę, gdyż dotychczas nie stwierdzono szczepów GBS opornych na ten antybiotyk.
Paciorkowiec w ciąży - profilaktyka zakażeń noworodkowych
Śródporodową profilaktykę antybiotykową stosuje się u kobiet, u których stwierdzono:
- obecność GBS w badaniu przesiewowym wykonanym przed porodem między 35. a 37 tygodniem ciąży (między 36. +0/7. a 36. +6/7. tygodniem ciąży według wytycznych ACOG z 2019 r.)
- obecność GBS w moczu w dowolnym tygodniu ciąży
- wystąpienie zakażenia GBS u noworodka we wcześniejszej ciąży.
Wskazaniami do interwencji jest również brak wyniku badania przesiewowego (niewykonanie badania lub nieznany wynik badania) i wystąpienie któregokolwiek z następujących czynników: poród przed 37. tygodniem ciąży, przedwczesne odpłynięcie wód płodowych, czas jaki upłynął od pęknięcia błon płodowych – powyżej 18 godzin oraz śródporodowa gorączka (38,0°C).
Nie ma wskazań do śródporodowej antybiotykoterapii w następujących przypadkach:
- kolonizacja GBS w poprzedniej ciąży, nieskutkująca zakażeniem objawowym noworodka,
- bakteriuria GBS w poprzedniej ciąży w którymkolwiek z trymestrów,
- ujemny wynik badania przesiewowego wykonanego po ukończeniu 35., a przed zakończeniem 37. tygodnia ciąży
- cięcie cesarskie wykonane przed rozpoczęciem się porodu u kobiet z zachowaną ciągłością błon płodowych, niezależnie od wyniku badania przesiewowego i czasu trwania ciąży.
Profilaktyczną antybiotykoterapię wdraża się u wszystkich kobiet, u których rozpoczął się poród (i/lub odpłynęły wody płodowe). Pełne działanie prewencyjne osiąga się po podaniu antybiotyku co najmniej 4 godziny przed zakończeniem porodu, dlatego ważne jest, by rodząca otrzymała profilaktykę tak szybko, jak tylko to możliwe.
Paciorkowiec w ciąży - w jaki sposób prowadzona jest śródporodowa antybiotykoterapia?
Lekiem z wyboru jest penicylina G, do ukończenia porodu. Równie skuteczną alternatywą stosowaną powszechnie w szpitalach jest ampicylina. Należy pamiętać, że nie wolno samodzielnie decydować o przyjmowaniu antybiotyku.
U kobiet uczulonych na penicylinę (ale bez dodatniego wywiadu w kierunku anafilaksji, obrzęku naczyniowego, niewydolności oddechowej lub pokrzywki po podaniu penicyliny albo cefalosporyny) podaje się antybiotyki I generacji cefalosporyn np. cefazolinę. U kobiet uczulonych na penicylinę z grup dużego ryzyka wystąpienia wstrząsu anafilaktycznego podaje się klindamycynę, jeżeli GBS jest wrażliwy na ten antybiotyk. Niestety odsetek szczepów opornych na klindamycynę (i erytromycynę) wzrasta i sięga już nawet 30%. W szczególnych przypadku oporności (tzw. oporność indukowana antybiotykiem) oraz wysokim prawdopodobieństwie silnej reakcji anafilaktycznej na penicylinę stosuje się wankomycynę.
Zapamiętaj
- Badanie w kierunku nosicielstwa GBS należy wykonać w 35.–37. tygodniu ciąży (36.+ 0/7 do 36. + 6/7 wg wytycznych ACOG).
- Dodatni wynik badania (stwierdzone nosicielstwo) jest wskazaniem do śródporodowej antybiotykoterapii. Nie leczy się nosicielstwa GBS przed porodem (wyjątkiem jest zakażenie dróg moczowych GBS).
- Śródporodowa antybiotykoterapia jest skuteczną metodą zapobiegania zakażeniu GBS u dziecka.
Piśmiennictwo
- Rekomendacje Polskiego Towarzystwa Ginekologicznego dotyczące wykrywania nosicielstwa paciorkowców grupy B (GBS) u kobiet w ciąży i zapobiegania zakażeniom u noworodków. Ginekol. Pol., 2008, 79, 221–223
- Verani J..R, MCGee L., Schrag S.J.: Prevention of perinatal group B streptococcal disease. Revised guidelines from CDC, 2010. MMWR, 2010;59: 1–32
- Treappe K.L., Shaffer L.E., Stempel L.E.: Vaginal-perianal compared with vaginal-rectal cultures for detecting group B streptococci during pregnancy. Obstet. Gynecol., 2011, 118, 313–317
- Weintraub A.Y., Kesssous R., Segienko R. i wsp.: Is colonization with GBS in a previous pregnancy associated with adverse perinatal outcomes? Arch. Gynecol. Obstet., 2011, 284, 787–791
- Kowalska B., Niemiec K.T., Drejewicz H. i wsp.: Prevalence of group B streptococcal colonization in pregnant women and their newborns based in the results of examination of patients in the Obstetric and Gynecology Department of the National Research Institute of Mother and Child – a pilot study. Ginekol. Pol., 2003; 74: 1223–1227
- Castor M.L., Whitney C.G., Como-Sabetti K. i wsp.: Antibiotic resistance patterns in invasive group B streptococcal isolates. Infect. Dis. Obstet. Gynecol., 2008;, doi: 10.1155/2008/727505
- Turrentine M.A., Ramirez M.M., Mastrobattista J.M.: Cost-effectivenes of universal prophylaxis in pregnancy with prior group B streptococci colonization. Infect. Dis. Obstet. Gynecol., 2009: doi: 10.1155/2009/934698
- Valkenburg-van den Berg A.W., Sprij A.J., Dekker F.W. i wsp.: Association between colonization with group B streptococcus and preterm delivery: a systematic review. Acta Obstetr. Gynecol. Scand., 2009; 88: 958–967
- Strus M., Pawlik D., Brzychczy-Włoch M. i wsp.: Group B streptococcus colonization of pregnant women and their children observed on obstetrics and neonatal wards of the University Hospital in Krakow, Poland. J. ed.. Microbiol., 2009; 58: 228–233
- Cheng P.J., Chueh H.Y., Liu C.M. i wsp.: Risk factors for recurrence of group B streptococcus colonization in a subsequent pregnancy. Obstet. Gynecol.: 2008;111:704–709
- The American College of Obstetricians and Gynecologists, ACOG Committee Opinion, Replacement Committee Opinion, No. 782, Czerwiec 2019