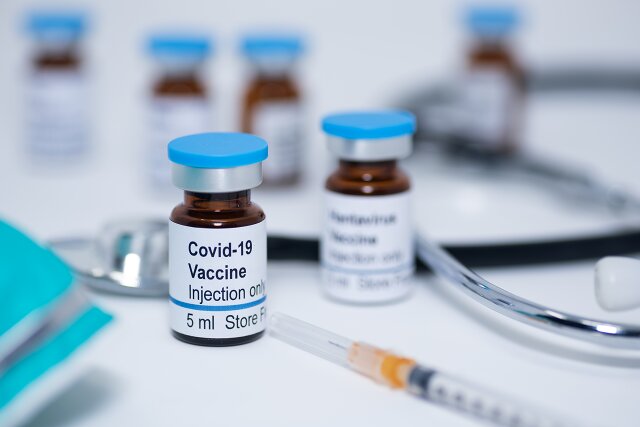Komitet ds. Bezpieczeństwa Farmakoterapii i Oceny Ryzyka (Pharmacovigilance Risk Assessment Committee – PRAC) działający przy Europejskiej Agencji Leków (EMA) zakończył kolejny etap analizy przypadków zdarzeń zakrzepowo-zatorowych, które wystąpiły w związku czasowym ze szczepieniem przeciwko COVID-19 preparatem firmy AstraZeneca (nazwa handlowa Vaxzevria), a jej wyniki przedstawił na posiedzeniu w dniu 7 kwietnia 2021 roku.
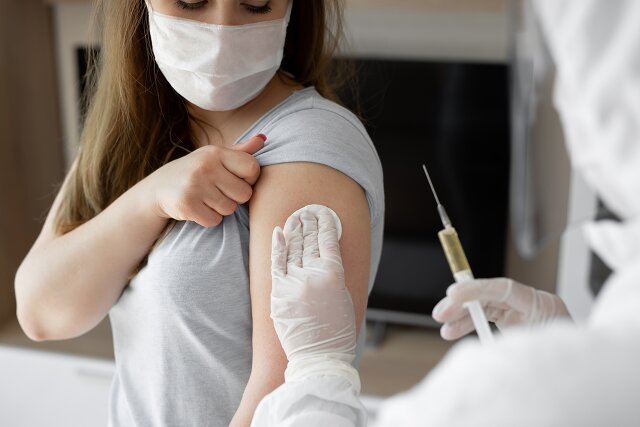
Fot. istockphoto.com
PRAC wskazał, że:
- istnieje prawdopodobny związek między szczepieniem preparatem Vaxzevria a występowaniem bardzo rzadkich, nietypowych zdarzeń zakrzepowo-zatorowych przebiegających z małopłytkowością; zdarzenia te należy uwzględnić w bardzo rzadkich zdarzeniach niepożądanych tego preparatu,
- podtrzymuje swoje wcześniejsze stanowisko, zgodnie z którym korzyści ze szczepienia preparatem Vaxzevria przewyższają potencjalne ryzyko z nim związane.
Wyciągając powyższe wnioski PRAC uwzględnił wszystkie aktualnie dostępne dane naukowe, w tym opinie specjalnie powołanej grupy roboczej ekspertów.
Zgłoszone w ramach rutynowego nadzoru nad NOP nietypowe zdarzenia zakrzepowo-zatorowe przebiegające z małopłytkowością, rzadziej również z krwawieniami, dotyczyły naczyń mózgu (zakrzepica zatok żylnych mózgu; cerebral venous sinus thrombosis – CVST), jamy brzusznej (zakrzepica żył trzewnych; splanchnic veins thrombosis – SVT) i tętnic. Komitet podał, że do 22 marca 2021 roku po zaszczepieniu preparatem Vaxzevria około 25 mln osób w krajach UE i Wielkiej Brytanii do bazy EudraVigilance zgłoszono 62 przypadki CVST i 24 przypadki SVT (w tym 18 zgonów).
EMA wskazała, że jednym z możliwych patomechanizmów tych nietypowych zdarzeń zakrzepowych może być odpowiedź immunologiczna prowadząca do stanu podobnego do tego, który czasami obserwuje się u pacjentów leczonych heparyną, tzw. małopłytkowości wywołanej heparyną (heparin-induced thrombocytopenia - HIT). PRAC zaapelował o przeprowadzenie nowych badań w tym obszarze, a także o zmianę protokołów aktualnie prowadzonych, co pozwoli zebrać więcej danych naukowych na ten temat.
Informacje dla pracowników medycznych:
- przypadki nietypowych zdarzeń zakrzepowo-zatorowych przebiegających z małopłytkowością, rzadziej również z krwawieniami, w tym przypadki CVST i SVT, po szczepieniu preparatem Vaxzevria obserwowano bardzo rzadko; większość zgłoszonych do tej pory przypadków dotyczyła kobiet w wieku <60 lat i występowała w ciągu pierwszych 14 dni po podaniu pierwszej dawki szczepionki,
- możliwym patomechanizmem tych nietypowych zdarzeń jest odpowiedź immunologiczna prowadząca do stanu podobnego do tego, który czasami obserwuje się u pacjentów leczonych heparyną, tzw. małopłytkowości wywołanej heparyną (heparin-induced thrombocytopenia - HIT); aktualnie nie jest możliwe określenie czynników ryzyka wystąpienia tych zdarzeń,
- zaleca się, aby personel medyczny zwracał szczególną uwagę objawy przedmiotowe i podmiotowe wskazujące na zdarzenia zakrzepowo-zatorowe i małopłytkowość, tak aby móc szybko wdrożyć odpowiednie i skuteczne leczenie,
- należy poinformować osoby szczepione, aby natychmiast zgłosiły się do lekarza jeżeli wystąpią u nich następujące objawy: duszność, ból w klatce piersiowej, obrzęk kończyn dolnych, uporczywy ból brzucha, silny i uporczywy ból głowy, niewyraźne widzenie, podbiegnięcia krwawe pojawiające się kilka dni po szczepieniu i poza miejscem wstrzyknięcia.
EMA podkreśla, że szczepionka Vaxzevria skutecznie zapobiega zachorowaniom na COVID-19, zwłaszcza wymagającą hospitalizacji i zgonom z jej powodu. Korzyści ze stosowania preparatu nadal przewyższają potencjalne ryzyko z nim związane. Zaznacza, że instytucje odpowiedzialne za rejestrację leków w poszczególnych krajach mogą wydać dodatkowe zalecenia dotyczące stosowania preparatu Vaxzevria.