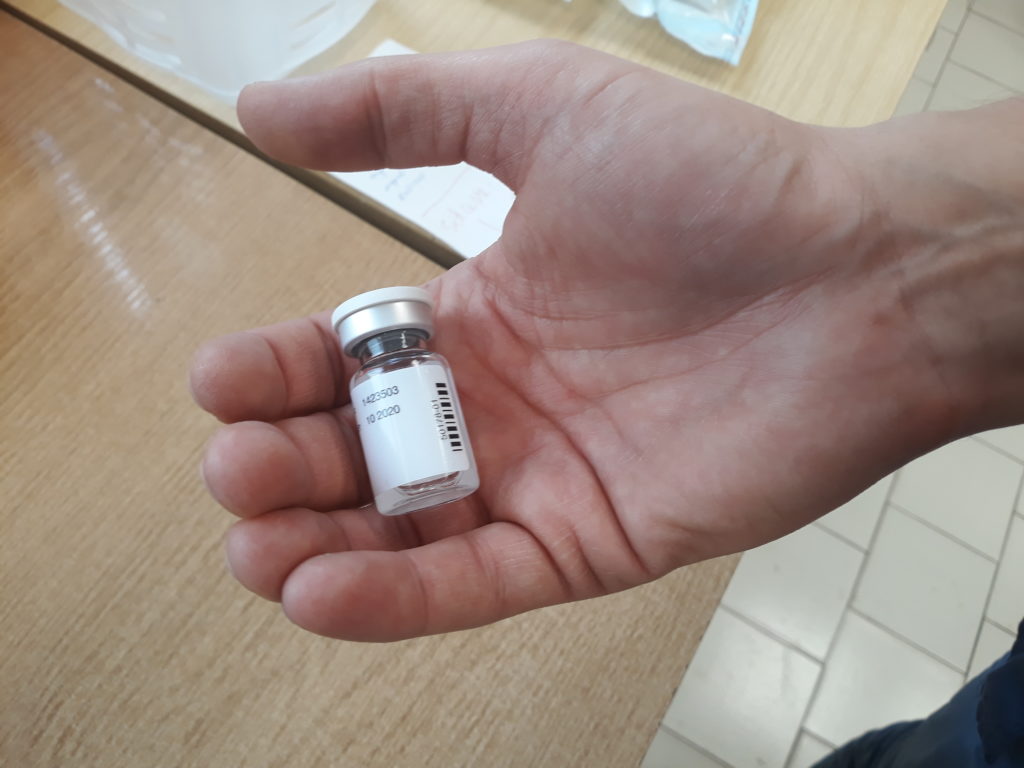
2 stycznia 2020 roku firma AveXis, producent terapii genowej AVXS-101, przeznaczonej dla chorych na rdzeniowy zanik mięśni, uruchomi globalny program dostępu. Firma będzie nieodpłatnie przekazywać sto dawek leku rocznie, a program ma być – według deklaracji producenta – wieloletni.

Fot. pixabay.com
Koszt terapii w Stanach Zjednoczonych (w Unii Europejskiej czeka na dopuszczenie na rynek) to ok. 2,5 mln dolarów. - Uruchamiany od nowego roku globalny Program Kontrolowanego Dostępu (Global Managed Access Program) ma na celu umożliwienie dostępu do terapii genowej AVXS-101 chorym, którzy mogliby odnieść dużą korzyść terapeutyczną – czytamy w komunikacie Fundacji SMA. W ramach programu producent zamierza nieodpłatnie przekazywać do 100 dawek AVXS-101 rocznie dla kwalifikujących się chorych mieszkających poza Stanami Zjednoczonymi, w tym 50 dawek w pierwszym półroczu 2020 roku.
Kto będzie mógł skorzystać z programu? Dzieci do lat dwóch (wiek w dniu podania preparatu), z genetycznie potwierdzonym rdzeniowym zanikiem mięśni dowolnego typu, zarówno te, u których już wystąpiły objawy choroby, jak i bezobjawowych.
- Zgłaszane dzieci muszą spełniać te same kryteria, które były warunkiem włączenia do badań klinicznych START i STRIVE, w tym zwłaszcza minimalny poziom funkcjonalny na skali CHOP-INTEND oraz brak konieczności stosowania wentylacji powyżej 16 godzin na dobę – informuje fundacja.
Zgłoszenia do programu, dokonywane wyłącznie przez lekarza prowadzącego (zgłaszać dziecka nie mogą rodzice!) drogą mailową, będą przyjmowane od 2 stycznia 2020 roku. Muszą zawierać podstawowe dane kliniczne, bez danych identyfikujących pacjenta.
Co dwa tygodnie, zaczynając od 3 lutego 2020 roku, niezależna komisja będzie losowała określoną liczbę zgłoszeń, zależnie od możliwości produkcyjnych. Dla wylosowanych dzieci firma przekaże dawki. Zgłoszenia niewylosowane automatycznie przechodzą do kolejnych losowań, chyba że lekarz zgłosi, że chory przestał spełniać warunki programu.
Fundacja przypomina, że preparat AVXS-101 można stosować tylko jeżeli u pacjenta wskaźnik przeciwciał AAV9 jest niższy niż 1:50 – będzie on potwierdzany badaniem przed przekazaniem leku. Wyższy wskaźnik oznacza brak możliwości zastosowania leczenia.
Pacjenci nie będą musieli udawać się do USA, by otrzymać leczenie – będzie to możliwe w wyspecjalizowanych szpitalach, które mają możliwość „prowadzenia opieki nad chorym dzieckiem zgodnie z międzynarodowym standardem opieki”. Te standardy oznaczają również monitorowanie stanu pacjenta przez minimum trzy miesiące.
- Ogromnie doceniamy uruchomienie tego programu. Umożliwi on prowadzenie leczenia SMA nowym, obiecującym preparatem. Ogromną szansę mają zwłaszcza dzieci, które nie odpowiadają na leczenie nusinersenem – podkreśla Fundacja SMA w opublikowanym we wtorek wieczorem komunikacie. Nusinersen od roku jest refundowany w Polsce i dostępny dla pacjentów za darmo. Lek, jak podkreślali kilka dni temu na konferencji prasowej eksperci, jest bezpieczny i skuteczny, a jego skuteczność jest tym większa, im wcześniej zostanie podany (optymalnie – przed pojawieniem się objawów).
W tej chwili w Polsce (ale także w innych krajach Europy) trwają zbiórki pieniężne na sfinansowanie terapii genowej. W tej chwili tylko na największym portalu crowdfundingowym Siepomaga.pl aktywnych jest pięć zbiórek. Najbliższa osiągnięcia celu jest zbiórka dla Alexa, na którego koncie jest już ponad 7,8 mln zł – do zebrania pozostaje ok. 1,2 mln zł.
Program nieodpłatnego dostępu do leku nie zmniejszy skali zbiórek na leczenie. Trudno sobie wyobrazić, by rodzice, którzy już wykazali się determinacją, planując terapię w USA, zakładając zbiórkę i organizując potężne przedsięwzięcie, jakim jest zebranie kwoty 9 mln zł, zawierzyli szanse dziecka ślepemu losowi. Zwłaszcza, że zgłoszeń z całego świata nadejdą, prawdopodobnie, tysiące.