Diagnostyka niedoborów odporności
10.03.2003
How to evaluate suspected immunodeficiency
Pediatric Annals, 1998; 27: 743-750
Ciąg dalszy dostępny po zalogowaniu dla osób związanych zawodowo z ochroną zdrowia.
Zaloguj się lub przejdź do portalu dla pacjentów.
Zaloguj się lub przejdź do portalu dla pacjentów.
Wybrane treści dla pacjenta
-
 Odwarstwienie siatkówki u dzieci Odwarstwienie siatkówki to poważna choroba gałki ocznej, która nie leczona prawie zawsze prowadzi do utraty widzenia w zajętym oku. Polega ona na odłączeniu większości jej warstw od leżącego bliżej zewnętrznej ściany gałki ocznej nabłonka barwnikowego siatkówki i naczyniówki.
Odwarstwienie siatkówki u dzieci Odwarstwienie siatkówki to poważna choroba gałki ocznej, która nie leczona prawie zawsze prowadzi do utraty widzenia w zajętym oku. Polega ona na odłączeniu większości jej warstw od leżącego bliżej zewnętrznej ściany gałki ocznej nabłonka barwnikowego siatkówki i naczyniówki. -
 Zaburzenia lękowe u dzieci i młodzieży Zaburzenia lękowe mogą dotykać nawet do 20% dzieci i nastolatków. W okresie dzieciństwa i dojrzewania występują różne postacie zaburzeń lękowych.
Zaburzenia lękowe u dzieci i młodzieży Zaburzenia lękowe mogą dotykać nawet do 20% dzieci i nastolatków. W okresie dzieciństwa i dojrzewania występują różne postacie zaburzeń lękowych. -
 Alergia pokarmowa u dzieci Alergię pokarmową łatwo można pomylić ze znacznie częstszą nietolerancją pokarmową, z powodu występowania podobnych objawów ze strony przewodu pokarmowego. Jeśli Twoje dziecko cierpi na nietolerancję pokarmową, to zjedzenie niewielkiej ilości danego pokarmu nie wywoła u niego żadnych dolegliwości. W przypadku alergii pokarmowej nawet śladowa ilość uczulającego pokarmu może spowodować reakcję alergiczną.
Alergia pokarmowa u dzieci Alergię pokarmową łatwo można pomylić ze znacznie częstszą nietolerancją pokarmową, z powodu występowania podobnych objawów ze strony przewodu pokarmowego. Jeśli Twoje dziecko cierpi na nietolerancję pokarmową, to zjedzenie niewielkiej ilości danego pokarmu nie wywoła u niego żadnych dolegliwości. W przypadku alergii pokarmowej nawet śladowa ilość uczulającego pokarmu może spowodować reakcję alergiczną. -
 Wizyta adaptacyjna dziecka w gabinecie stomatologicznym Mam dla Państwa propozycję małej zabawy. Proszę teraz nie myśleć o zielonym słoniu. I o czym Państwo przed chwilą pomyśleli? Większość z Państwa niewątpliwie pomyślała właśnie o zielonym słoniu. Tak funkcjonuje nasz mózg. Dlatego dziecko nie wie, że powinno się bać dentysty, jeśli rodzic nie użyje w kontekście dentysty słowa „ból” czy „strach”.
Wizyta adaptacyjna dziecka w gabinecie stomatologicznym Mam dla Państwa propozycję małej zabawy. Proszę teraz nie myśleć o zielonym słoniu. I o czym Państwo przed chwilą pomyśleli? Większość z Państwa niewątpliwie pomyślała właśnie o zielonym słoniu. Tak funkcjonuje nasz mózg. Dlatego dziecko nie wie, że powinno się bać dentysty, jeśli rodzic nie użyje w kontekście dentysty słowa „ból” czy „strach”. -
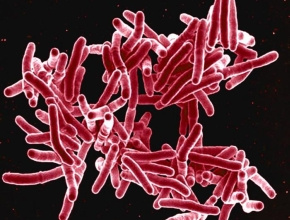
 Gruźlica dziecięca Wczesne objawy gruźlicy często są niecharakterystyczne. Należą do nich stany podgorączkowe, pocenie się (szczególnie w nocy), utrzymujący się kaszel, chudnięcie. Objawy zaawansowanej gruźlicy zależą od lokalizacji jej ognisk.
Gruźlica dziecięca Wczesne objawy gruźlicy często są niecharakterystyczne. Należą do nich stany podgorączkowe, pocenie się (szczególnie w nocy), utrzymujący się kaszel, chudnięcie. Objawy zaawansowanej gruźlicy zależą od lokalizacji jej ognisk. -
 Niedoczynność tarczycy u dzieci Niedoczynność tarczycy to zespół objawów wynikających z niedoboru hormonów tarczycy lub defektu ich receptora.
Niedoczynność tarczycy u dzieci Niedoczynność tarczycy to zespół objawów wynikających z niedoboru hormonów tarczycy lub defektu ich receptora. -
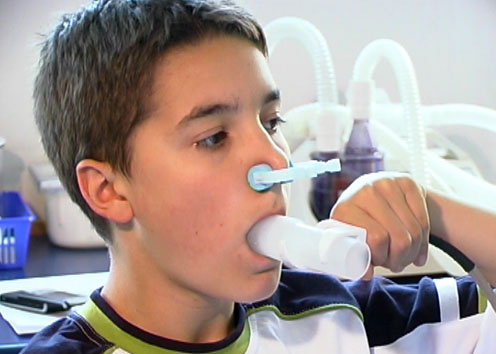
 Astma u dzieci - mechanizmy i przyczyny U większości ludzi kontakt z tymi substancjami nie powoduje żadnej reakcji, ale u osób uczulonych we krwi znajdują się przeciwciała przeciwko nim skierowane. Należą one zwykle do immunoglobulin klasy E (IgE).
Astma u dzieci - mechanizmy i przyczyny U większości ludzi kontakt z tymi substancjami nie powoduje żadnej reakcji, ale u osób uczulonych we krwi znajdują się przeciwciała przeciwko nim skierowane. Należą one zwykle do immunoglobulin klasy E (IgE). -
 Infekcje dróg oddechowych u dzieci U dzieci, szczególnie tych uczęszczających do żłobka, przedszkola lub posiadających starsze rodzeństwo w wieku przedszkolnym, rozpoznaje się średnio 8–10 infekcji dróg oddechowych w ciągu roku. Większość z nich to łagodne, samo-ograniczające się zakażenia górnych dróg oddechowych. Niektóre, np. zapalenie płuc lub zapalenie oskrzelików, mogą mieć jednak cięższy przebieg.
Infekcje dróg oddechowych u dzieci U dzieci, szczególnie tych uczęszczających do żłobka, przedszkola lub posiadających starsze rodzeństwo w wieku przedszkolnym, rozpoznaje się średnio 8–10 infekcji dróg oddechowych w ciągu roku. Większość z nich to łagodne, samo-ograniczające się zakażenia górnych dróg oddechowych. Niektóre, np. zapalenie płuc lub zapalenie oskrzelików, mogą mieć jednak cięższy przebieg. -
 Toksoplazmoza u dzieci Toksoplazmoza jest odzwierzęcą chorobą pasożytniczą wywołaną przez pierwotniaka Toxoplasma gondii. Pasożyta rozsiewają koty, wydalając z kałem pierwotniaki, które mogą przetrwać w glebie przez kilkanaście miesięcy.
Toksoplazmoza u dzieci Toksoplazmoza jest odzwierzęcą chorobą pasożytniczą wywołaną przez pierwotniaka Toxoplasma gondii. Pasożyta rozsiewają koty, wydalając z kałem pierwotniaki, które mogą przetrwać w glebie przez kilkanaście miesięcy. -
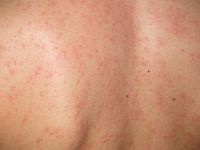
 Pokrzywka u dzieci U dzieci pokrzywka zwykle ma charakter ostry i może się wiązać ze spożyciem określonego pokarmu, zastosowaniem leku czy współistniejącą infekcją górnych dróg oddechowych.
Pokrzywka u dzieci U dzieci pokrzywka zwykle ma charakter ostry i może się wiązać ze spożyciem określonego pokarmu, zastosowaniem leku czy współistniejącą infekcją górnych dróg oddechowych.
O tym się mówi
-
Ile szpitali potrzebujemy w Polsce?
Żaden szpital nie zostanie zamknięty. Ale co to w zasadzie znaczy „szpital” i czy brak zagrożenia likwidacją oznacza brak zmian?
-
Pozorny sprzeciw
Ministerstwo nauki tworzy grunt pod umożliwienie kontynuowania kształcenia przyszłych lekarzy w szkołach, które nie mają wymaganego zaplecza dydaktycznego – uważają przedstawiciele samorządu lekarskiego.
-
System przypomina zmurszały budynek
Liczyliśmy na to, że ten rząd zmieni metodę i ustawę, stanie w prawdzie i głośnio przyzna, że pieniędzy jest zdecydowanie za mało. Tak się nie stało, kontynuowana jest polityka zaciemniania obrazu, co nas bardzo boli – mówi prezes NRL Łukasz Jankowski.