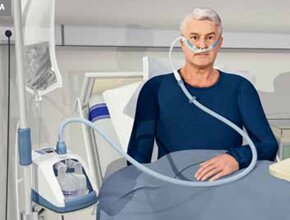
W wytycznych Surviving Sepsis Campaign dotyczących leczenia krytycznie chorych na COVID-19 (przedstawionych w nr. 4/2020 „Medycyny Praktycznej” – przyp. red.) sugeruje się stosowanie tlenoterapii biernej, jeśli SpO2 wynosi <92% (zalecenie słabe/niska jakość danych) oraz zaleca się włączanie tlenoterapii biernej przy SpO2 <90% (zalecenie silne/umiarkowana jakość danych). Auto rzy wytycznych sugerują, by HFNOT stosować u chorych z COVID-19 i hipoksemią utrzymującą się pomimo stosowania konwencjonalnej tlenoterapii biernej (zalecenie słabe/niska jakość danych) oraz by w tej grupie pacjentów preferować stosowanie HFNOT zamiast nieinwazyjnej wentylacji mechanicznej. U chorych, u których stosuje się HFNOT, zaleca się ścisłe monitorowanie wydolności oddechowej oraz wczesną intubację w razie narastania niewydolności oddechowej. Podkreśla się również, że podczas HFNOT powstaje aerozol, co się wiąże z ryzykiem transmisji wirusa, dlatego personel medyczny musi mieć założone odpowiednie środki ochrony indywidualnej, a chory powinien – jeśli to możliwe – przebywać w pomieszczeniu z podciśnieniem. Niektórzy eksperci zalecają również, by rozpoczynać HFNOT od stosunkowo małych przepływów (15–30 l/min) w celu minimalizacji wytwarzania aerozolu.
Przypadek kliniczny
76-letniego mężczyznę z nadciśnieniem tętniczym, cukrzycą typu 2, chorobą niedokrwienną serca oraz przewlekłą niewydolnością serca z zachowaną frakcją wyrzutową lewej komory w wywiadzie przeniesiono ze szpitalnego oddziału ratunkowego na oddział wewnętrzny, na którym pracujesz. Na podstawie obrazu radiologicznego (rozległe zmiany naciekowo-niedodmowe w polu dolnym płuca lewego na radiogramie), objawów (kaszel, duszność, ból o charakterze opłucnowym), temperatury ciała (38,8°C) oraz wyników badania przedmiotowego (trzeszczenia i ściszenie szmerów oddechowych nad dolnymi polami płucnymi po stronie lewej) i badań laboratoryjnych (zwiększone stężenie białka C-reaktywnego) rozpoznano pozaszpitalne zapalenie płuc. Przy przyjęciu na oddział chory był w stanie ogólnym średnim – niewydolny oddechowo (SpO2 82% podczas tlenoterapii biernej przez kaniule donosowe z przepływem 4 l/min, częstotliwość oddechów 30/min), wydolny krążeniowo (ciśnienie tętnicze 130/80 mm Hg, częstotliwość rytmu serca 95/min, czas powrotu kapilarnego 2 s), bez zaburzeń stanu świadomości (15 pkt w skali Glasgow).
Pytanie 1
Jakie badanie laboratoryjne należy wykonać u pacjenta z podejrzeniem niewydolności oddechowej?
Złotym standardem rozpoznawania niewydolności oddechowej jest gazometria krwi tętniczej. Krew należy pobrać z tętnicy promieniowej. U opisywanego chorego uzyskano następujący wynik: pH 7,51, pCO2 32 mm Hg, pO2 46 mm Hg, HCO3– 24 mmol/l, stężenie mleczanu 1,4 mmol/l. Rozpoznano hipoksemiczną niewydolność oddechową z zasadowicą oddechową, związaną z hipokapnią w następstwie hiperwentylacji, i ustalono docelową wartość SpO2 na 92–96%. Postanawiasz zastosować u pacjenta HFNOT.
Pytanie 2
Jakich ustawień użyjesz na początku? Na jakiej podstawie będziesz podejmował decyzje o ich modyfikacji?
Używając miarki dostarczonej przez producenta urządzenia do HFNOT, wybierasz dla chorego kaniulę w odpowiednim rozmiarze (w opisywanym przypadku M), następnie ustawiasz przepływ na reduktorze (20 l/min) oraz na urządzeniu (40 l/min) – FiO2 na ekranie urządzenia wynosi 59%. Temperaturę mieszaniny oddechowej ustalasz na 37°C. Skuteczność zastosowanej terapii oceniasz, monitorując SpO2, częstotliwość oddechów i stan świadomości chorego. Po podłączeniu HFNOT chory oddycha wolniej (22/min), SpO2 się poprawia (89%), stan świadomości chorego pozostaje prawidłowy (15 pkt w skali Glasgow). Pacjent twierdzi, że powietrze podawane przez urządzenie jest dla niego za ciepłe.
Pytanie 3
Czy pacjent wymaga modyfikacji ustawień urządzenia?
Monitorowane parametry częściowo się poprawiły, lecz nadal nie są optymalne. W tej sytuacji najlepszym rozwiązaniem jest zwiększenie przepływu mieszaniny oddechowej zarówno na urządzeniu (np. do 50 l/min, co zwiększy wygenerowany CPAP), jak i na reduktorze (aby doszło do zwiększenia FiO2, którego wartość jest wyświetlana na ekranie monitora, np. do 70%). Jeżeli twoim zdaniem CPAP ma w tym przypadku drugorzędne znaczenie, wystarczy zwiększyć przepływ tlenu na reduktorze, tak by zaobserwować adekwatne zwiększenie FiO2 na ekranie urządzenia. Z uwagi na złą tolerancję temperatury podawanego powietrza wskazane jest jej obniżenie do 34°C.
Po wprowadzeniu zmian w ustawieniach urządzenia SpO2 zwiększyło się do 93%, a częstotliwość oddechów zmniejszała się do 16/min. Chory dob rze znosi temperaturę mieszaniny oddechowej. W kontrolnej gazometrii krwi tętniczej stwierdzasz: pH 7,45, pCO2 36 mm Hg, pO2 65 mm Hg, HCO3– 24 mmol/l, stężenie mleczanu 1,3 mmol/l.
Pytanie 4
Na jakie objawy należy teraz zwrócić uwagę?
Chory nadal wymaga ścisłego monitorowania wydolności oddechowej. Szczególną uwagę należy zwrócić na SpO2 (wartość docelowa 92–96%), częstotliwość oddechów (przyśpieszenie oddychania może świadczyć o narastaniu niewydolności oddechowej) oraz stan świadomości (pogorszenie może świadczyć o narastającej hipoksemii lub hiperkapnii – jeśli masz wątpliwości, wykonaj kontrolną gazometrię krwi tętniczej!). W razie nasilania się niewydolności oddechowej może się okazać konieczne wezwanie ZWR lub konsultującego anestezjologa w celu oceny wskazań do intubacji dotchawiczej i wentylacji mechanicznej płuc. Uwaga: opóźnianie intubacji pogarsza rokowanie pacjenta!
Piśmiennictwo:
1. Alhazzani W., Moller M.H., Arabi Y.M. i wsp.: Surviving Sepsis Campaign: guidelines on the management of critically ill adults with coronavirus disease 2019 (COVID-19). Intensive Care Med., 2020; doi: 10.1007/s00 134-020-06 022-52. Rochwerg B., Granton D., Wang D.X. i wsp.: High flow nasal cannula compared with conventional oxygen therapy for acute hypoxemic respiratory failure: a systematic review and meta-analysis. Intensive Care Med., 2019; 45: 563–572
3. Kang B.J., Koh Y., Lim C.M. i wsp.: Failure of high-flow nasal cannula therapy may delay intubation and increase mortality. Intensive Care Med., 2015; 41: 623–632