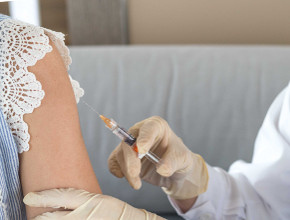
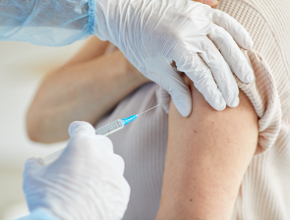
Amerykański Urząd ds. Żywności i Leków (FDA) zarejestrował pierwszą szczepionkę przeciwko COVID-19. Do tej pory preparat ten stosowano na podstawie pozwolenia na tzw. użycie w sytuacji wyjątkowej (emergency use authorization – EUA).
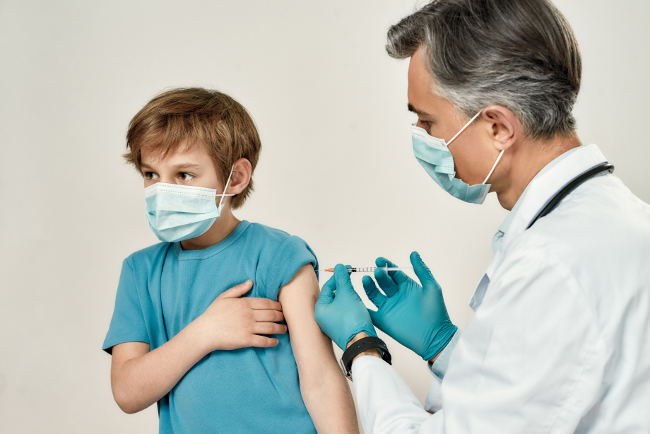
Fot. www.istockphoto.com/pl
Zmiana warunków dopuszczenia do stosowania dotyczy szczepionki mRNA firmy Pfizer/BioNTech (Comirnaty) u osób w wieku ≥16 lat. Stosowanie preparatu u dzieci i nastolatków w wieku 12–15 lat oraz podawanie trzeciej dawki szczepionki osobom z wybranymi niedoborami odporności nadal objęte jest warunkami EUA.
Janet Woodcock, pełniąca obowiązki komisarza FDA, podkreśliła, że zarejestrowanie pierwszej szczepionki przeciwko COVID-19 jest kamieniem milowym w walce z pandemią. Zarówno preparat Comirnaty, jak i inne szczepionki, spełniają naukowe standardy bezpieczeństwa, skuteczności i jakości wymagane przy pozwoleniu na użycie w sytuacji wyjątkowej. Jednak ta rejestracja może mieć szczególne znacznie dla tych osób, które do tej pory miały wątpliwości dotyczące szczepienia przeciwko COVID-19.
W Stanach Zjednoczonych szczepionkę mRNA przeciwko COVID-19 firmy Pfizer/BioNTech (Comirnaty) dopuszczono do stosowania u osób w wieku ≥16 lat na podstawie EUA w grudniu 2020 roku, następnie w maju 2021 roku rozszerzono wskazania wiekowe na populację w wieku 12–15 lat.
Szczepionki zarejestrowane przez FDA przechodzą standardowy proces oceny jakości, bezpieczeństwa i skuteczności. W przypadku wszystkich szczepionek Urząd ocenia dane wymagane w przedłożonym przez producenta wniosku o rejestrację preparatów biologicznych (biologics license application – BLA). Firmy Pfizer i BioNTech złożyły wniosek o BLA w maju 2021 roku i etapami przekazywały do FDA wszystkie niezbędne dane naukowe. FDA wydała decyzję o rejestracji szczepionki Comirnaty na podstawie przekazanych już wcześniej danych wymaganych przy wydaniu EUA i analizy kolejnych, zaktualizowanych danych z badania klinicznego szczepionki, obejmujących dłuższy okres obserwacji oraz większą populację.