Skróty: ChPL – Charakterystyka Produktu Leczniczego, MenACWY – szczepionka przeciwko meningokokom grup A, C, W-135 i Y
Wprowadzenie
Lekarze coraz częściej zastanawiają się, jak realizować program szczepień obowiązkowych z uwzględnieniem zalecanego szczepienia przeciwko meningokokom grup A, C, W-135 i Y (MenACWY) u niemowląt. Z Charakterystyki Produktu Leczniczego (ChPL) Nimenrix – jedynej MenACWY zarejestrowanej do stosowania w tym wieku – wynika bowiem, że czas podania tego preparatu należy koniecznie uzależnić od czasu podania szczepionek zawierających komponentę tężcową oraz że jednoczasowe podanie MenACWY wpływa na osiągane stężenia przeciwciał przeciwko meningokokom. Niektórzy lekarze zaczęli odpowiednio modyfikować obowiązkowy kalendarz szczepień u niemowląt, aby postępować zgodnie z zapisami w ChPL szczepionki Nimenrix, jeśli rodzice decydują się na szczepienie również przeciwko meningokokom grupy A, C, W i Y. W niniejszym artykule przeanalizowano zasadność takiego postępowania oraz oceniono korzyści i ryzyko wynikające z dosłownego stosowania się do zapisów w ChPL Nimenrix.
ChPL Nimenrix
Rozszerzony zakres wieku
Szczepionka Nimenrix zawiera polisacharydy Neisseria meningitidis grupy A, C, W-135 i Y skoniugowane z toksoidem tężcowym jako nośnikiem białkowym (MenACWY-TT).1 Do niedawna preparat ten był zarejestrowany wyłącznie do stosowania >1. roku życia w schemacie 1-dawkowym. Na początku 2017 roku szczepionkę zarejestrowano jednak również dla niemowląt do stosowania w schemacie 2+1: pierwszą dawkę szczepionki podaje się w wieku 6–12 tygodni, kolejną po 2 miesiącach od pierwszej dawki, a następnie dawkę przypominającą w 2. roku życia. Co ważne, szczepionka nie jest zarejestrowana (dawka pierwsza) dla dzieci w wieku od ukończenia 12. tygodnia życia do ukończenia 1. roku życia.
Koadministracja z innymi preparatami
Jak w przypadku każdej szczepionki, producent przeprowadził badania dotyczące możliwości jednoczesnego podania preparatu MenACWY i innych szczepionek. Wyniki obserwacji uwzględniono w ChPL Nimenrixu. Poniżej zacytowano zapisy najistotniejsze dla omawianego zagadnienia: „Oceniano bezpieczeństwo i immunogenność szczepionki Nimenrix podawanej kolejno lub w tym samym czasie ze szczepionką zawierającą toksoid błoniczy, toksoid tężcowy, bezkomórkowy składnik krztuścowy, inaktywowane wirusy polio (typ 1, 2 i 3), antygen powierzchniowy wirusa zapalenia wątroby typu B oraz fosforan polirybozylorybitolu Haemophilus influenzae typu b sprzężony z toksoidem tężcowym (DTaP-HBV-IPV/Hib) u dzieci w 2. roku życia. Podanie szczepionki Nimenrix miesiąc po szczepionce DTaP-HBV-IPV/Hib prowadziło do uzyskania niższych wartości GMT w stosunku do grup A, C i W-135 mierzonych rSBA w porównaniu do podawania jednoczesnego (p. pkt 4.5). Znaczenie kliniczne tej obserwacji jest nieznane. (…) O ile to możliwe, szczepionka Nimenrix i szczepionka zawierająca TT, na przykład szczepionka DTaP-HBV-IPV/Hib, powinny być podawane w tym samym czasie lub szczepionkę Nimenrix należy podać co najmniej miesiąc przed szczepionką zawierającą TT.1
Konsekwencje dosłownego stosowania się do zapisów w ChPL
Biorąc pod uwagę liczbę szczepień przewidzianych dla dzieci w pierwszych miesiącach życia oraz konieczność rozpoczęcia szczepienia przeciwko meningokokom grup A, C, W i Y w wieku 6–12 tygodni, trudno sprostać wymaganiom opisanym w ChPL szczepionki Nimenrix. Opierając się na powyższych zapisach, niektórzy lekarze zajmujący się realizacją szczepień ochronnych u niemowląt modyfikują kolejność i czas podawania obowiązkowych szczepionek przeciwko błonicy, tężcowi i krztuścowi (DTPa/DTPw) u pacjentów, podając MenACWY w pierwszej kolejności, miesiąc przed szczepionką DTP, lub stosując jednocześnie szczepionkę DTPa i MenACWY, a opóźniając podanie innych preparatów. Na rycinie 1.A i B przedstawiono przykładowe schematy szczepień, jakie lekarze rozważają w takich sytuacjach. Ponieważ większość rodziców, którzy decydują się na zakup MenACWY, wybiera dla swoich dzieci również preparaty wysoce skojarzone typu „6 w 1” lub „5 w 1”, w prezentowanych przykładach uwzględniono stosowanie preparatów DTPa/IPV/Hib/HBV („6 w 1”). Należy zwrócić uwagę, że takie rozłożenie szczepień na pierwszych wizytach szczepiennych zaburza priorytety szczepień, a ryzyko związane z dosłownym stosowaniem się do ChPL jest niewspółmiernie większe od korzyści związanych z uzyskaniem nieco większych stężeń przeciwciał wobec grup A, C i W-135.
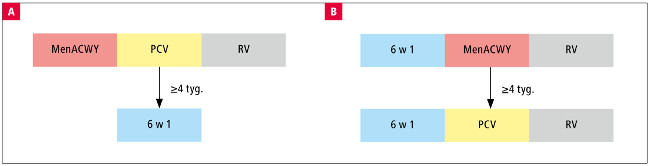
Ryc. 1. Przykłady nieprawidłowego zaplanowania szczepień na pierwszych wizytach szczepiennych (począwszy od 6. tyg.ż.): (A) podanie na pierwszej wizycie szczepiennej preparatu MenACWY, a dopiero później szczepionki „6 w 1”, co opóźnia uodpornienie przeciwko krztuścowi, (B) na dwóch pierwszych wizytach szczepiennych zaplanowano po dwa wstrzyknięcia na jednej wizycie, czgo często oczekują rodzice niemowląt, jednak jest to niedopuszczalne z punktu widzenia zapisów w PSO oraz nieoptymalne dla pacjenta ze względu na ryzyko zakażeń pneumokokowych.
Skróty: 6 w 1 – skojarzona szczepionka przeciwko błonicy, tężcowi, krztuścowi (bezkomórkowa), poliomielitis (inaktywowana), Haemophilus influenzae typu b i wirusowemu zapaleniu wątroby typu B (DTPa-IPV-Hib-HBV), MenACWY – skoniugowana 4-walentna szczepionka przeciwko meningokokom grypy A, C, Y i W-135, PCV – skoniugowana szczepionka przeciwko pneumokokom, RV – szczepionka przeciwko rotawirusom
Zaproponowane w pierwszym przykładzie (ryc. 1.A) podanie szczepionki MenACWY w wieku 6 tygodni, miesiąc przed szczepieniem DTPa/IPV/Hib/HBV, jest absolutnie niedopuszczalne z punktu widzenia właściwej profilaktyki przeciwkrztuścowej, ponieważ zapadalność niemowląt na krztusiec jest wielokrotnie większa niż zapadalność na inwazyjną chorobę meningokokową. Według danych European Centre for Disease Prevention and Control (ECDC), w 2016 roku zapadalność na krztusiec (przypadki potwierdzone) w krajach Unii Europejskiej i Europejskiego Obszaru Gospodarczego (UE/EOG) u niemowląt wyniosła około 70–75/100 000 populacji,2 przy czym dane te mogą być poważnie niedoszacowane. Trzeba też pamiętać, że podana zapadalność jest uśredniona, a przecież Polska jest jednym z liderów pod względem zachorowalności na krztusiec w Europie – w 2016 roku w naszym kraju zgłoszono 6828 przypadków krztuśca (we wszystkich grupach wiekowych), a w UE/EOG 48 500.2 Z kolei zapadalność wśród niemowląt na inwazyjną chorobę meningokokową wywołaną przez jakąkolwiek grupę serologiczną wyniosła w Polsce w 2016 roku 11,5/100 000,3 przy czym wiadomo, że w tej grupie wiekowej dominują zakażenia wywołane przez meningokoki grupy B (>70% przypadków, a w niektórych latach jeszcze większe odsetki),4,5 a nie typu A, C, W-135 lub Y, przed którymi chroni szczepionka Nimenrix. Należy również pamiętać, że szczepienie przeciwko krztuścowi jest obowiązkowe, a więc większość niemowląt jest skutecznie zabezpieczonych przed tą chorobą, czego nie można powiedzieć o szczepionce MenACWY, którą rzadko stosuje się w warunkach polskich u niemowląt. Ten fakt jeszcze bardziej podkreśla proporcje między ryzykiem zakażenia tymi dwoma rodzajami patogenów w wieku niemowlęcym. Nie bez przyczyny Program Szczepień Ochronnych (PSO) przewiduje pierwsze szczepienie przeciwko krztuścowi już w wieku 6 tygodni, które powinno się traktować jako priorytetowe w aspekcie dużego ryzyka zachorowania na tę chorobę.6
Z podobnych przyczyn nieoptymalny jest również schemat przedstawiony na rycynie 1.B – choć w tym przypadku szczepienie DTPa/IPV/Hib/HBV zaplanowano łącznie z MenACWY, opóźnione jest szczepienie przeciwko pneumokokom. Taki schemat lekarze rozważają, gdy rodzice nie zgadzają się na wykonanie na jednej wizycie szczepiennej >2 wstrzyknięć (obecnie częste zjawisko). Ponieważ jednak ryzyko zakażenia pneumokokowego jest w wieku niemowlęcym większe niż ryzyko infekcji meningokokowej, szczepienie przeciwko pneumokokom należy traktować jako priorytetowe, również w aspekcie jego obowiązkowości wynikającej z PSO.
Czy można ekstrapolować zapisy w ChPL na populację niemowlęcą?
Kluczowym aspektem w analizie zaleceń dotyczących preparatu Nimenrix wydaje się jednak to, że przytoczone dane dotyczące immunogenności szczepionki MenACWY podawanej jednoczasowo lub w miesięcznych odstępach od szczepionki z komponentą tężcową dotyczyły dzieci w 2. roku życia. Chociaż w drugiej części cytowanego zapisu, który przez autorów ChPL został ujęty jako rekomendacja („o ile to możliwe […] powinny być podawane”), nie znajdujemy odniesienia do tej grupy wiekowej, należy się zastanowić, czy nie jest to zbyt daleko idące uogólnienie.
Warto zauważyć, że zapisy te były obecne także w starszej wersji ChPL preparatu Nimenrix,7 gdy był on zarejestrowany do stosowania wyłącznie >1. roku życia. W kontekście dostępnych danych klinicznych zapis ten jest więc pewną pozostałością z wcześniejszej rejestracji preparatu. Ekstrapolowanie tego zalecenia na dzieci w wieku 6–12 tygodni jest zatem zdecydowanie niewłaściwe, tym bardziej, że w tym „ciasnym” przedziale wiekowym większość programów szczepień obowiązujących na świecie przewiduje podanie wielu innych szczepionek. Natomiast w 2. roku życia przewidziano znacznie mniej preparatów, a zalecane przedziały czasu ich podania dają o wiele większą swobodę niż w pierwszych miesiącach życia. Postępowanie zgodnie z ChPL u dzieci w 2. roku życia nie powinno więc stanowić większego problemu.
Bardzo istotne jest również to, że jak dotąd nie opublikowano danych dotyczących immunogenności preparatu Nimenrix podawanego w różnych kombinacjach z innymi szczepionkami w 1. roku życia. Należy zatem uznać, że nie ma danych popierających tezę o konieczności uzależniania terminów podania MenACWY od terminów innych szczepień przewidzianych w wieku niemowlęcym.
Koniecznie należy się również odnieść do przytoczonego w ChPL zdania: „Znaczenie kliniczne tej obserwacji jest nieznane”. Liczne dowody naukowe wskazują, że kliniczna skuteczność szczepionek nie wynika jednoznacznie z ich immunogenności wykazanej w badaniach serologicznych. Nie wiadomo zatem, czy zaobserwowane mniejsze stężenia przeciwciał przeciwko serogrupom A, C i W-135 mają jakikolwiek negatywny wpływ na ostateczną skuteczność kliniczną preparatu Nimenrix (również u dzieci w 2. rż.). To zdanie jest kluczowe w aspekcie rozumienia siły zalecenia wyrażonego w ChPL.
Podsumowanie
Powyższe rozważania pozwalają jednoznacznie stwierdzić, że zapisy w ChPL preparatu Nimenrix nie powinny decydować o czasie i kolejności podania szczepionek przewidzianych w PSO dla niemowląt. Kluczowa i priorytetowa jest bowiem realizacja szczepień zgodnie z obowiązkowym PSO. Oczywiście nie należy rezygnować z podawania szczepionki MenACWY w wieku niemowlęcym, chcąc „sprostać” karkołomnym zapisom w ChPL – zastosowanie preparatu MenACWY, obok innych szczepień, jest optymalnym rozwiązaniem dla niemowlęcia i należy dążyć do jego realizacji. Niemniej jednak przy planowaniu kolejności podawania poszczególnych szczepień w pierwszych tygodniach życia należy postępować zgodnie z nadrzędną i uniwersalną zasadą zachowania dowolnych odstępów między szczepionkami inaktywowanymi. Na rycinie 2. zaproponowano różne schematy szczepień (A, B i C) w pierwszych miesiącach życia z uwzględnieniem wszystkich obowiązkowych i zalecanych dla wieku preparatów i jednocześnie zaplanowaniem jak najmniejszej liczby wizyt szczepiennych (ze względu na dostępność preparatów o różnym stopniu skojarzenia można zaproponować wiele innych kombinacji, ale ich omówienie przekracza ramy tej publikacji).
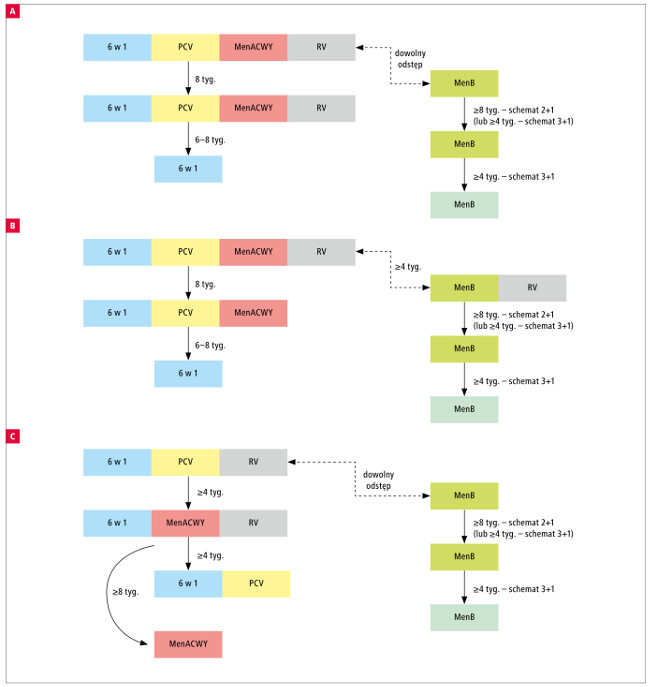
Ryc. 2. Przykłady prawidłowego rozplanowania szczepień obowiązkowych i zalecanych w pierwszych miesiącach życia, przy uwzględnieniu jak najmniejszej liczby wizyt szczepiennych: (A) schemat zgodny z terminami wizyt przewidzianych w PSO, umożliwiający sprawną realizację wszystkich szczepień obowiązkowych i zalecanych w ramach najmniejszej, możliwej liczby wizyt szczepiennych. Często jest nieakceptowany przez rodziców ze względu na przewidziane na pierwszej wizycie 3 wstrzyknięcia; (B) wariant podobny do 2A, w którym drugą dawkę doustnej RV przewidziano razem z pierwszym wstrzyknięciem szczepionki MenB; (C) wariant ten przewiduje szczepienie preparatem „6 w 1” „przyspieszone” w stosunku do zapisów w PSO (w którym między pierwszymi dawkami szczepień DTP i Hib przewidziano odstęp 8-tygodniowy). Schemat ten jest zgodny z ChPL preparatów typu „6 w 1”, a jednocześnie pozwala zaplanować tylko 2 wstrzyknięcia na pierwszych wizytach szczepiennych, co rodzice lepiej akceptują niż wykonanie 3 wstrzyknięć. Ograniczeniem tego schematu jest wiek podania pierwszej dawki MenACWY, czyli najpóźniej 12. tydzień życia – nie można więc go zastosować u niemowląt, które rozpoczynają szczepienia >8. tygodnia życia.
We wszystkich przykładach (A, B i C) zaplanowano szczepienie MenB na osobnej wizycie szczepiennej (postępowanie sugerowane przez producenta w celu zmniejszenia ryzyka kumulacji łagodnych NOP [gorączki, bólu w miejscu wstrzyknięcia). W przypadku szczepionki MenB należy uwzględnić 2 (schemat 2+1) lub 3 (schemat 3+1) dawki odpowiednio w 2- lub 1-miesięcznych odstępach, w zależności od wieku dziecka, w którym rozpoczynane są szczepienia. Dla uproszczenia graficznego w schematach uwzględniono 2-dawkową RV, więc przy wyborze szczepionki 3-dawkowej należy zaplanować późniejsze podanie jeszcze trzeciej dawki.
Skróty: 6 w 1 – skojarzona szczepionka przeciwko błonicy, tężcowi, krztuścowi (bezkomórkowa), poliomielitis (inaktywowana), Haemophilus influenzae typu b i wirusowemu zapaleniu wątroby typu B (DTPa-IPV-Hib-HBV), MenACWY – skoniugowana 4-walentna szczepionka przeciwko meningokokom grypy A, C, Y i W-135, MenB – białkowa szczepionka przeciwko meningokokom grupy B, PCV – skoniugowana szczepionka przeciwko pneumokokom, RV – szczepionka przeciwko rotawirusom
Wobec opisanych wątpliwości wydaje się, że producent preparatu Nimenrix powinien zweryfikować dotychczasowe zalecenia i sformułować nowe zasady koadministracji szczepionki w wieku niemowlęcym.
Na zakończenie podkreślmy jeszcze raz, że obecnie nie ma wystarczających danych nakazujących jednoczasowe podawanie lub zachowanie jakichkolwiek konkretnych odstępów i kolejności między podaniem szczepionki przeciwko Men ACWY i innych szczepionek u niemowląt.
Piśmiennictwo:
1. Charakterystyka Produktu Leczniczego Nimenrix. www.pfizerpro.com.pl2. ECDC. Pertussis Annual Epidemiological Report – 2016. www.ecdc.europa.eu/en
3. Biuletyn Choroby Zakaźne i Zatrucia w Polsce (2016) wwwold.pzh.gov.pl/oldpage/epimeld/index_p.html
4. Inwazyjna choroba meningokokowa w Polsce w 2014 roku. Wstępne dane KOROUN. Warszawa, 24.07.2015
5. Skoczyńska A., Kucha A., Waśko I. i wsp.: Inwazyjna choroba meningokokowa u chorych poniżej 20. roku życia w Polsce w latach 2009–2011. Pediatr. Pol., 2012; 87 (5): 438–443
6. Załącznik do komunikatu Głównego Inspektora Sanitarnego z dnia 25 października 2018 r. w sprawie Programu Szczepień Ochronnych na rok 2019. Dziennik Urzędowy Ministra Zdrowia, poz. 104 (25 października 2018 r.)
7. Charakterystyka Produktu Leczniczego Nimenrix (wersja z 2012 r.). www.ec.europa.eu/health/documents

























