Opracowała lek. Iwona Rywczak
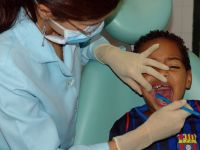
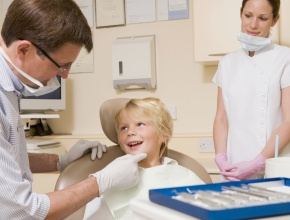
W 2007 r. w kanadyjskiej prowincji Ontario zainicjowano powszechne szczepienia przeciwko ludzkiemu wirusowi brodawczaka (HPV), którymi objęto dziewczęta w wieku 13 lat. Szczepienia realizowano preparatem 4-walentnym (HPV-4). W omawianym badaniu dokonano przeglądu zdarzeń niepożądanych po szczepieniu HPV-4 zgłoszonych do systemu nadzoru nad niepożądanymi odczynami poszczepiennymi (NOP) w okresie od 1 września 2007 roku do 31 grudnia 2011 roku. Uwzględniono NOP dotyczące dziewcząt w wieku 12–15 lat. W analizowanym okresie w ramach programu szczepień rozprowadzono 691 994 dawki HPV-4. Łącznie zidentyfikowano 152 podejrzeń NOP związanych czasowo ze szczepieniem HPV-4, o których powiadomiono w 133 zgłoszeniach (19,2 zgłoszeń/100 000 dawek). Najczęstszymi zdarzeniami niepożądanymi były: „reakcje alergiczne ze strony skóry lub błon śluzowych” (25%), osutka skórna (22%) i odczyny w miejscu podania szczepionki (20%). Zgłoszono 10 ciężkich zdarzeń, w tym po 2 przypadki reakcji anafilaktycznej i drgawek, 1 przypadek małopłytkowości i 1 zgon. Szczegółowe dochodzenie wykazało, że przyczyną zgonu była nierozpoznana wcześniej choroba serca. Zgłoszone przypadki reakcji anafilaktycznej nie spełniały kryteriów anafilaksji ustalonych przez Brighton Collaboration. W przypadku drgawek dokładniejsze dane dostępne były tylko dla 1 zgłoszenia – dotyczyło ono pacjentki z wywiadem w kierunku drgawek gorączkowych w pierwszych 2 latach życia, u której ostatecznie rozpoznano padaczkę. Z powodu podejrzenia NOP 62% pacjentów szukało pomocy w placówce pozaszpitalnej, 17% zgłosiło się na oddział ratunkowy, a 7 wymagało hospitalizacji.
Autorzy badania wyciągnęli wniosek, że dane z systemu nadzoru nad NOP wskazują na bezpieczeństwo szczepionki HPV-4. Obserwacje te są zgodne z wynikami badań przeprowadzonych przed zarejestrowaniem HPV-4 oraz już po jej dopuszczeniu do obrotu. Nie wykryto niepokojących sygnałów dotyczących bezpieczeństwa tej szczepionki.