Hepatologia – postępy 2018/2019
15.11.2019
Ciąg dalszy dostępny po zalogowaniu dla osób związanych zawodowo z ochroną zdrowia.
Zaloguj się lub przejdź do portalu dla pacjentów.
Zaloguj się lub przejdź do portalu dla pacjentów.
Wybrane treści dla pacjenta
-
 Stłuszczenie wątroby – objawy, przyczyny, leczenie Stłuszczenie wątroby to stan, w którym w komórkach wątroby gromadzą się krople tłuszczu. Stłuszczenie wątroby może być spowodowane działaniem toksycznej substancji – często alkoholu (jest to wówczas alkoholowe stłuszczenie wątroby) lub nie ma jednej konkretnej przyczyny – mówimy wtedy o niealkoholowej stłuszczeniowej chorobie wątroby.
Stłuszczenie wątroby – objawy, przyczyny, leczenie Stłuszczenie wątroby to stan, w którym w komórkach wątroby gromadzą się krople tłuszczu. Stłuszczenie wątroby może być spowodowane działaniem toksycznej substancji – często alkoholu (jest to wówczas alkoholowe stłuszczenie wątroby) lub nie ma jednej konkretnej przyczyny – mówimy wtedy o niealkoholowej stłuszczeniowej chorobie wątroby. -
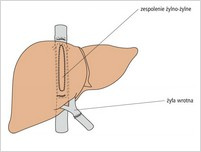
 Przeszczep wątroby Przeszczepienie wątroby jest metodą leczenia niektórych poważnych chorób wątroby, stosowaną w sytuacjach, kiedy wyczerpano już inne możliwości leczenia. Wskazaniami do przeszczepienia są ciężkie choroby wątroby, takie jak marskość wątroby, nowotwory czy niewydolność wątroby. Przeciwwskazania do przeszczepienia to m.in. czynna choroba alkoholowa, rak wątroby z przerzutami i ciężkie zakażenia ogólnoustrojowe. Rokowanie po przeszczepieniu jest dobre, około 70–80% osób ma szansę na wieloletnie przeżycie.
Przeszczep wątroby Przeszczepienie wątroby jest metodą leczenia niektórych poważnych chorób wątroby, stosowaną w sytuacjach, kiedy wyczerpano już inne możliwości leczenia. Wskazaniami do przeszczepienia są ciężkie choroby wątroby, takie jak marskość wątroby, nowotwory czy niewydolność wątroby. Przeciwwskazania do przeszczepienia to m.in. czynna choroba alkoholowa, rak wątroby z przerzutami i ciężkie zakażenia ogólnoustrojowe. Rokowanie po przeszczepieniu jest dobre, około 70–80% osób ma szansę na wieloletnie przeżycie. -
 Niedożywienie u chorych na POChP U chorych na POChP problemem może być zarówno otyłość, jak i niedożywienie. Niedożywienie występuje znacznie częściej u chorych na zaawansowaną POChP, występuje u 30–60% hospitalizowanych pacjentów z POChP. Najbardziej rozpowszechnioną formą niedożywienia wśród chorych jest niedożywienie białkowo-energetyczne, które charakteryzuje się zbyt małym spożyciem produktów bogatych w białko i energię. Badania wskazują na gorszą czynność układu oddechowego u chorych z niedożywieniem niż chorych otyłych.
Niedożywienie u chorych na POChP U chorych na POChP problemem może być zarówno otyłość, jak i niedożywienie. Niedożywienie występuje znacznie częściej u chorych na zaawansowaną POChP, występuje u 30–60% hospitalizowanych pacjentów z POChP. Najbardziej rozpowszechnioną formą niedożywienia wśród chorych jest niedożywienie białkowo-energetyczne, które charakteryzuje się zbyt małym spożyciem produktów bogatych w białko i energię. Badania wskazują na gorszą czynność układu oddechowego u chorych z niedożywieniem niż chorych otyłych. -

-

-
 Rak wątroby (nowotwory złośliwe wątroby): rodzaje, objawy, leczenie i rokowanie Do pojawienia się guza w wątrobie może dojść w wyniku przerzutów innych nowotworów do wątroby lub nowotwór rozwija się z tkanek znajdujących się w wątrobie – najczęściej jest to rak wątrobowokomórkowy. Zmiany nowotworowe w wątrobie mogą długo nie dawać żadnych objawów. Leczenie i rokowanie w raku wątroby zależy od stopnia zaawansowania choroby
Rak wątroby (nowotwory złośliwe wątroby): rodzaje, objawy, leczenie i rokowanie Do pojawienia się guza w wątrobie może dojść w wyniku przerzutów innych nowotworów do wątroby lub nowotwór rozwija się z tkanek znajdujących się w wątrobie – najczęściej jest to rak wątrobowokomórkowy. Zmiany nowotworowe w wątrobie mogą długo nie dawać żadnych objawów. Leczenie i rokowanie w raku wątroby zależy od stopnia zaawansowania choroby -
 Niealkoholowa stłuszczeniowa choroba wątroby (stłuszczenie wątroby NAFLD, MAFLD) Niealkoholowa stłuszczeniowa choroba wątroby (NAFLD) to stłuszczenie wątroby niezwiązane ze spożywaniem alkoholu, przyjmowaniem leków lub chorobami genetycznymi. To najczęstsza przewlekła choroba wątroby. NAFLD najczęściej wiąże się z zespołem metabolicznym i powoduje zwiększenie ryzyka przedwczesnej miażdżycy i zgonu z przyczyn sercowo-naczyniowych
Niealkoholowa stłuszczeniowa choroba wątroby (stłuszczenie wątroby NAFLD, MAFLD) Niealkoholowa stłuszczeniowa choroba wątroby (NAFLD) to stłuszczenie wątroby niezwiązane ze spożywaniem alkoholu, przyjmowaniem leków lub chorobami genetycznymi. To najczęstsza przewlekła choroba wątroby. NAFLD najczęściej wiąże się z zespołem metabolicznym i powoduje zwiększenie ryzyka przedwczesnej miażdżycy i zgonu z przyczyn sercowo-naczyniowych -
 Polineuropatie Mianem polineuropatii określa się zespół objawów wynikających z uszkodzenia wielu nerwów obwodowych. Do najczęstszych przyczyn polineuropatii należą: cukrzyca, nadużywanie alkoholu, choroby genetyczne, procesy autoimmunologiczne i zapalne, niedożywienie, leki, choroby endokrynologiczne, toksyny, choroby nowotworowe.
Polineuropatie Mianem polineuropatii określa się zespół objawów wynikających z uszkodzenia wielu nerwów obwodowych. Do najczęstszych przyczyn polineuropatii należą: cukrzyca, nadużywanie alkoholu, choroby genetyczne, procesy autoimmunologiczne i zapalne, niedożywienie, leki, choroby endokrynologiczne, toksyny, choroby nowotworowe. -
 Zespół krótkiego jelita Zespół krótkiego jelita to stan po wycięciu lub wyłączeniu z pasażu pokarmu części lub całego jelita cienkiego, prowadzący do tak znacznego zmniejszenia wchłaniania, że odżywianie drogą przewodu pokarmowego nie pozwala na utrzymanie stanu zdrowia pacjenta. W leczeniu stosuje się przede wszystkim żywienie pozajelitowe w domu.
Zespół krótkiego jelita Zespół krótkiego jelita to stan po wycięciu lub wyłączeniu z pasażu pokarmu części lub całego jelita cienkiego, prowadzący do tak znacznego zmniejszenia wchłaniania, że odżywianie drogą przewodu pokarmowego nie pozwala na utrzymanie stanu zdrowia pacjenta. W leczeniu stosuje się przede wszystkim żywienie pozajelitowe w domu. -

Konferencje MP
-
Endoskopia 2026
Katowice, 5 września
- wzajemna edukacja w endoskopii – jak szkolić siebie i innych?
- kwalifikacja zmian do leczenia
- diagnostyka optyczna nowotworów przewodu pokarmowego
- zmiany w jelicie grubym – leczenie endoskopowe czy chirurgiczne?
-
Chirurgia 2026
Obejrzyj wykłady
- krwawienie do dolnego odcinka przewodu pokarmowego
- anatomia chirurgiczna okolicy pachwiny oraz pachy
- resekcja międzyzwieraczowa odbytnicy
- współczesna chirurgia raka trzustki
- endoskopia trzeciej przestrzeni
-
Interna 2026
Obejrzyj wykłady
- zapalenie mięśnia sercowego – aktualne wytyczne ESC
- zapalenie błony śluzowej żołądka
- przewlekła choroba nerek – osiąganie remisji
- Treat-to-target (T2T) w chorobach reumatycznych
- hiperaldosteronizm pierwotny
Napisz do nas
Zadaj pytanie ekspertowi, przyślij ciekawy przypadek,
zgłoś absurd, zaproponuj temat dziennikarzom.
Pomóż redagować portal.
Pomóż usprawnić system ochrony zdrowia.