Tłumaczyła lek. Iwona Rywczak
Skróty: Hib – Haemophilus influenzae typu b, HPV – ludzki wirus brodawczaka, HPV-4 – 4-walentna szczepionka przeciwko HPV, IChP – inwazyjna choroba pneumokokowa, PCV-7 – 7-walentna skoniugowana szczepionka przeciwko pneumokokom, PCV-13 – 13-walentna skoniugowana szczepionka przeciwko pneumokokom
Translated with permission from Clinical Infectious Diseases, Evan J. Anderson, Michael A. Daugherty, Larry K. Pickering, Walter A. Orenstein, Ram Yogev; Protecting the community through child vaccination, Clinical Infectious Diseases, https://doi.org/10.1093/cid/ciy142. © The Authors 2018. Published by Oxford University Press for the Infectious Diseases Society of America. All rights reserved. For permissions, e-mail: journals.permissions@oup.com.
Streszczenie
Bezpośredni efekt szczepień u dzieci jest dobrze znany, jednak zbyt małe znaczenie przypisuje się korzyściom z pośredniej ochrony populacyjnej dla zdrowia publicznego. O ochronie populacyjnej mówimy, gdy osoby zaszczepione blokują łańcuch transmisji drobnoustroju. Osoby nieszczepione lub zaszczepione niekompletnie są wtedy chronione poprzez zapobieganie ekspozycji na zakażenie oraz ograniczenie rozprzestrzeniania się drobnoustrojów w populacji. Po wprowadzeniu nowych szczepionek do programów szczepień dzieci istotne zmniejszenie zapadalności na choroby zakaźne odnotowano także u dzieci, młodzieży i dorosłych, którzy nie byli nimi objęci. Ochrona nieodpornych osób w danej populacji zależy od utrzymania dużych wskaźników wyszczepialności. Większa świadomość znaczenia ochrony populacyjnej poprawi strategie szczepień dzieci, co w przyszłości zapewni ochronę społeczeństwa przed chorobami zakaźnymi.
Dzięki realizacji programów szczepień ochronnych u dzieci zapadalność na wiele chorób zakaźnych zmniejszyła się do rekordowo małych wartości, w wielu przypadkach poniżej poziomu zakładanego na podstawie wyszczepialności i skuteczności rzeczywistej szczepionek. Dodatkowe zmniejszenie zapadalności, wykraczające poza bezpośredni efekt szczepień, to tzw. ochrona populacyjna wynikająca z ochrony „nieuodpornionych” osób (np. nieszczepionych i niechorujących wcześniej na daną chorobę zakaźną, nieodpowiadających na szczepienia) dzięki zmniejszeniu ryzyka ekspozycji na zakażenie. W piśmiennictwie ochronę populacyjną określano jako „odporność zbiorowiskowa”, „ochrona zbiorowiskowa”, „efekt stadny”, „odporność populacyjna”, „pośredni efekt szczepień” i „ochrona pośrednia”. Autorzy artykułu preferują pojęcie „ochrona populacyjna”, ponieważ termin ten nie sugeruje, że osoby nieszczepione lub inne osoby podatne na zakażenie w danej populacji są odporne na daną chorobę. Natomiast osoby (społeczności) podatne na zakażenie są chronione przed zachorowaniem i zgonem dzięki szczepieniom, które przełamują łańcuch transmisji zakażeń w populacji.
Szczepienia zapewniają dzieciom i dorosłym istotne korzyści z ochrony populacyjnej. Zapadalność na niemal wszystkie choroby, którym można zapobiegać poprzez szczepienia, zmniejszyła się o ≥95% od czasu ich wprowadzenia, mimo że wskaźniki wyszczepialności są znacznie mniejsze (tab. 1.).1,2 Ochrona populacyjna jest szczególnie ważna dla osób, które nie mogą być szczepione (np. ze względu na zbyt młody wiek, współistnienie różnych chorób, chemioterapię), oraz dla osób, u których nie uzyskano skutecznej odpowiedzi immunologicznej na szczepienie (np. osób, które nie odpowiedziały na szczepienie lub z pierwotnymi i wtórnymi niedoborami odporności). Ochrona populacyjna zależy od takich czynników, jak polityka szczepień, niezdecydowane postawy wobec szczepień i nagromadzenie w danym środowisku nieszczepionych lub niekompletnie zaszczepionych dzieci. W niniejszym artykule przedstawiono dane na temat ochrony populacyjnej dzieci i dorosłych, omówiono podstawy teoretyczne i ograniczenia ochrony populacyjnej oraz strategie jej optymalizacji.
| Tabela 1. Zmiany w epidemiologii wybranych chorób, którym można zapobiegać poprzez szczepienia w Stanach Zjednoczonycha | ||||
|---|---|---|---|---|
| Choroba, której można zapobiegać poprzez szczepienie | Średnia roczna liczba zachorowań (okres przed wprowadzeniem szczepień) | Wskaźnik wyszczepialności w 2015 r. (%)b | Roczna liczba zachorowań w 2016 r.c | Roczna liczba zachorowań przed wprowadzeniem szczepień vs liczba zachorowań wg najnowszych danych, (redukcja w %) |
| błonica | 21 053 (1936–1945) | 85 | 0 | 100 |
| WZW typu A | 117 333 (1986–1995) | 60 | 2500 | 98 |
| inwazyjne zakażenia Hibd | 20 000 (1980) | 83 | 22 | >99 |
| odra | 530 217 (1953–1962) | 92 | 69 | >99 |
| świnka | 162 344 (1963–1968) | 92 | 5311 | 97 |
| krztusiec | 200 752 (1934–1943) | 85 | 15 737 | 92 |
| IChP (wszystkie grupy wiekowe) | 63 067 (1997–1999) | 84 | 29 000 | 54 |
| IChP (dzieci do 5. rż.) | 16 069 (1997–1999) | 84 | 1800 | 89 |
| polio, postać porażenna | 16 316 (1951–1954) | 94 | 0 | 100 |
| różyczka | 47 745 (1966–1968) | 92 | 5 | >99 |
| rotawiruse | 62 500 (1990) | 73 | 11 250 | 82 |
| ospa wietrzna | 4 085 120 (1990–1994) | 92 | 126 639 | 97 |
| a Dane z 1. i 2. pozycji piśmiennictwa oraz uzyskane od Sarah Roush, National Center for Immunization and Respiratory Diseases, Centers for Disease Control and
Prevention (informacja ustna). b Szacowany wskaźnik wyszczepialności ≥4 dawkami bezkomórkowej szczepionki przeciwko błonicy, tężcowi i krztuścowi, ≥2 dawkami szczepionki przeciwko WZW typu A, ≥3 dawkami skoniugowanej szczepionki przeciwko Hib (w zależności od podanego preparatu), ≥1 dawką szczepionki przeciwko odrze, śwince i różyczce, ≥4 dawkami skoniugowanej szczepionki przeciwko pneumokokom, ≥3 dawkami inaktywowanej szczepionki przeciwko polio, ≥2 dawkami szczepionki przeciwko rotawirusom (w zależności od podanego preparatu) oraz ≥1 dawką szczepionki przeciwko ospie wietrznej. c Roczna liczba przypadków WZW typu A, IChP, zakażenia rotawirusem, ospy wietrznej w 2015 r. d Zachorowania oszacowane jako inwazyjne zakażenie Hib u dzieci do 5. rż. e Zachorowania oszacowane jako zakażenie rotawirusem wymagające hospitalizacji u dzieci do 3. rż. Hib – Haemophilus influenzae typu b, IChP – inwazyjna choroba pneumokokowa, WZW – wirusowe zapalenie wątroby | ||||
Ochrona populacyjna nieszczepionych dzieci i dorosłych
Dane epidemiologiczne wskazują na korelację
między znacznym zmniejszeniem obciążeń związanych z chorobami zakaźnymi a wprowadzeniem
różnych programów szczepień dla dzieci (ryc. 1.,
tab. 1.). Wskazują one wyraźnie na ochronę populacyjną,
jednak istotne znaczenie mogą także mieć
pewne trendy sekularne (np. lepsza higiena, inne
interwencje na poziomie zdrowia publicznego).
Ochrona populacyjna jest szczególnie widoczna,
gdy obciążenia związane z daną chorobą zmniejszają
się w populacjach dzieci nieobjętych programem
szczepień oraz nieszczepionych dorosłych. W niniejszym artykule zjawisko to opisano w odniesieniu
do szczepienia dzieci przeciwko Streptococcus
pneumoniae, rotawirusom, Haemophilus
influenzae typu b (Hib), ludzkiemu wirusowi brodawczaka
(HPV) i wirusowi różyczki.
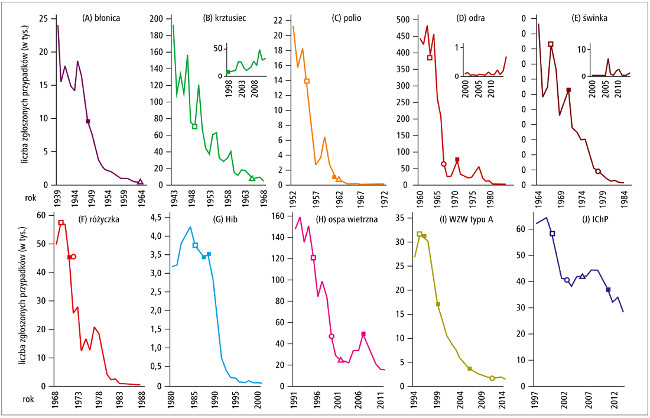
Ryc. 1. Roczna liczba przypadków chorób, którym można zapobiegać poprzez szczepienia, zgłoszonych w Stanach Zjednoczonych w okresie 20–25 lat (w przypadku Hib [tylko dzieci do 5. rż.) oraz inwazyjnej choroby pneumokokowej [IChP] liczbę przypadków oszacowano): błonica (A), krztusiec (B), porażenna postać poliomyelitis (C), odra (D), świnka (E), różyczka (F), Hib (G), ospa wietrzna (H), WZW typu A (I), IChP (J). Kwadraty niezacienione oznaczają wprowadzenie nowych szczepionek, kwadraty zacienione – zmianę preparatu lub strategii szczepień, okręgi – osiągnięcie 50% wskaźnika wyszczepialności u dzieci w wieku 19–35 miesięcy, trójkąty – osiągnięcie 75% wskaźnika wyszczepialności u dzieci w wieku 19–35 miesięcy lub 1–4 lat (w zależności od badania). Dana pochodzą z National Notifiable Diseases Surveillance System, Active Bacterial Core surveillance, Supplemental Pertussis Surveillance System, United States Immunization Survey, National Immunization Survey oraz 3.–12. pozycji piśmiennictwa. Nie uwzględniono szczepień przeciwko rotawirusom, grypie oraz szczepionek stosowanych u młodzieży (przeciwko meningokokom grupy C i HPV). Dane dla poszczególnych drobnoustrojów: (A) szczepionkę zawierającą toksoid błoniczy po raz pierwszy zarejestrowano w 1923 r., a całokomórkową szczepionkę przeciwko błonicy, tężcowi i krztuścowi (DTPw) wprowadzono w 1948 r., po raz pierwszy wskaźnik wyszczepialności dzieci w wieku 1–4 lat osiągnął 75% w 1964 r. (B) bezkomórkową szczepionkę przeciwko błonicy, tężcowi i krztuścowi (DTPa) po raz pierwszy zarejestrowano w 1991 r., amerykański Advisory Committee on Immunization (ACIP) zalecił wyłączne stosowanie szczepionek bezkomórkowych w ramach powszechnych szczepień (5 dawek) w 1998 r. (C) inaktywowaną szczepionkę przeciwko polio zarejestrowano w 1955 r., a szczepionkę doustną w 1961 r. Wskaźnik wyszczepialności dzieci w wieku 1–4 lat osiągnął 75% w 1962 r. (D) pierwszą szczepionkę zawierającą żywego wirusa odry zarejestrowano w 1963 r., wskaźnik wyszczepialności dzieci w wieku 1–4 lat osiągnął 50% w 1967 r. Szczepionkę przeciwko odrze, śwince i różyczce (MMR) zarejestrowano w 1971 r. (E) szczepionkę zawierającą atenuowanego wirusa świnki zarejestrowano w 1967 r., wskaźnik wyszczepialności dzieci w wieku 1–4 lat osiągnął 50% w 1978 r. (F) szczepionkę przeciwko różyczce zarejestrowano w 1969 r., wskaźnik wyszczepialności dzieci w wieku 1–4 lat osiągnął 50% w 1971 r. (G) polisacharydową szczepionkę przeciwko Hib zarejestrowano w 1985 r., a szczepionkę skoniugowaną w 1987 r., powszechne szczepienie zalecono w 1988 r. (H) „żywą” szczepionkę przeciwko ospie zarejestrowano w 1995 r., wskaźnik wyszczepialności dzieci w wieku 19–35 mies. osiągnął 50% w 1999 r., a 75% w 2001 r. Powszechne szczepienia 2 dawkami zalecono w 2006 r. (I) szczepionkę przeciwko WZW typu A zarejestrowano w 1995 r., a w 1996 r. zalecono szczepienie grup ryzyka. W 1999 r. ACIP rozszerzył zalecenia o dzieci zamieszkujące stany z dużymi wskaźnikami zapadalności na WZW typu A, a powszechne szczepienia wszystkich dzieci zalecił w 2006 r. Wskaźnik wyszczepialności dzieci w wieku 19–35 mies. osiągnął 50% w 2011 r. (J) 7-walentną skoniugowaną szczepionkę przeciwko pneumokokom wprowadzono do programu szczepień w 2000 r., wskaźnik wyszczepialności dzieci w wieku 19–35 mies. osiągnął 50% w 2003 r., a 75% w 2007 r. Szczepionkę 13-walentną wprowadzono w 2010 r. Przedrukowano z: Fine P.E.M., Mulholland K., Scott J.A., Edmunds W.J.: Community protection. In: Plotkin S.A., Orenstein W.A., Offit P.A., Edwards K.M., eds.: Vaccines. Philadelphia, PA, Elsevier, 2018: 1512–1531. © 2018, with permission from Elsevier.
Skróty: Hib – Haemophilus influenzae typu b, HPV – ludzki wirus brodawczaka, WZW – wirusowe zapalenie wątroby
Od czasu wprowadzenia w 2000 roku 7-walentnej
skoniugowanej szczepionki przeciwko pneumokokom
(PCV-7) w Stanach Zjednoczonych
odnotowano zmniejszenie zapadalności na inwazyjną
chorobę pneumokokową (IChP) u dzieci, w tym o 42% u nieuprawnionych do szczepień
PCV-7 niemowląt do 2. miesiąca życia (dane z 2004 r.).13 Po wprowadzeniu w 2010 roku skoniugowanej
szczepionki 13-walentnej (PCV-13), która
zastąpiła PCV-7, do 2013 roku, kiedy wskaźnik
wyszczepialności PCV-13 wyniósł 82%, ogólna
zapadalność na IChP u dzieci do 5. roku życia
zmniejszyła się o 64%, a w przypadku IChP wywołanej
przez 6 dodatkowych typów serologicznych
uwzględnionych w szczepionce o 93%. Co ważne,
zmniejszenie zapadalności na IChP (o 75%)
wywołaną przez typy serologiczne uwzględnione w PCV-13 odnotowano również u dzieci w wieku
5–17 lat nieobjętych programem szczepień (p. Med. Prakt. Szczepienia 3/2015, s. 98 – przyp. red.).14
Powszechne szczepienie PCV-7 dzieci do 2. roku
życia w Stanach Zjednoczonych znamiennie
zmniejszyło wskaźniki hospitalizacji z powodu
IChP u dorosłych oraz śmiertelność z powodu
IChP wśród hospitalizowanych dorosłych.14,15
90% z niemal 800 000 hospitalizacji, których
udało się uniknąć w latach 2000–2006 dzięki
szczepieniom PCV-7, dotyczyło pneumokokowego
zapalenia płuc u dorosłych.16 W badaniu przeprowadzonym w stanie Connecticut stwierdzono, że w regionach (wyszczególnionych na podstawie
kodu pocztowego), w których wskaźniki wyszczepialności 3 lub 4 dawkami PCV-7 były mniejsze
od przeciętnej wartości, obserwowano częstsze zachorowania
na IChP u dorosłych wywołaną przez
typy serologiczne uwzględnione w PCV-7.17 Do lat
2012–2013 zapadalność na IChP wywołaną przez 6 dodatkowych typów uwzględnionych w PCV-13
zmniejszyła się u dorosłych o 58–72%, natomiast w przypadku typów nieszczepionkowych wartości
nie zmieniły się lub nieznacznie się zwiększyły.14
Ogółem szacuje się, że dzięki szczepieniom PCV-7 i PCV-13 w latach 2001–2012 w Stanach Zjednoczonych
udało się uniknąć niemal 400 000 zachorowań
na IChP (>50% redukcja w grupie wiekowej
>5 lat) i około 30 000 zgonów (prawie 90% redukcja w grupie wiekowej >5 lat).14 Poza tym zmniejszenie
liczby zachorowań na IChP oporną na antybiotyki
zaobserwowano nie tylko u dzieci do 5. roku
życia (78–96%), ale także u dorosłych (50–69%).14
Powszechne szczepienia niemowląt przeciwko
rotawirusom rozpoczęto w 2006 roku (w Stanach
Zjednoczonych – przyp. red.). Do 2008 roku
wskaźnik wyszczepialności ≥1 dawką osiągnął 57% u dzieci w 1. roku życia i 17% u dzieci w 2. roku
życia, natomiast u dzieci w wieku >2 lat był on bardzo
mały i nie miał istotnego znaczenia.18 Jednak
dane z krajowego systemu nadzoru epidemiologicznego
wykazały znamienne zmniejszenie w 2008
roku częstości hospitalizacji z powodu biegunki
rotawirusowej lub jakiejkolwiek ostrej biegunki u dzieci ze wszystkich grup wiekowych, a do roku
2010 odnotowano kolejną redukcję tych wartości.19 Do 2012 roku wskaźnik hospitalizacji dzieci do 5. roku życia z powodu biegunki rotawirusowej zmniejszył się o 94%, a w tym czasie szczepionkę
przeciwko rotawirusom otrzymało jedynie 69%
dzieci w wieku 19–35 miesięcy.20 Po wprowadzeniu
szczepień niemowląt w 2006 roku stwierdzono
rzadsze występowanie biegunki rotawirusowej u dorosłych. Dane z Chicago wskazują na mniejszą o 48% częstość występowania biegunki rotawirusowej u dorosłych, których próbki stolca badano
po wprowadzeniu powszechnych szczepień dzieci
przeciwko rotawirusom (p. Med. Prakt. Szczepienia
2/2013, s. 56 – przyp. red.).21 Podobną redukcję zaobserwowano w analizie wypisów ze szpitala starszych
dzieci i dorosłych do ukończenia 44. roku życia z rozpoznanym zakażeniem rotawirusowym.19
W badaniu kliniczno-kontrolnym obejmującym
Indian Nawaho (Stany Zjednoczone) stwierdzono,
że po wprowadzeniu szczepień przeciwko Hib ryzyko
inwazyjnego zakażenia Hib u dzieci do 2. roku
życia pochodzących ze społeczności, w których
30% dzieci otrzymało szczepionkę przeciwko Hib,
było o 57% mniejsze niż u dzieci zamieszkujących w społecznościach z 10% wskaźnikiem wyszczepialności.22 Dane z krajowego system nadzoru z lat 1989–1991 wskazują na zmniejszenie o 71%
liczby zachorowań wywołanych przez Hib wśród
amerykańskich dzieci w wieku ≤14 miesięcy – rok
przed wprowadzeniem szczepień w tej grupie wiekowej.23 Podobne wyniki uzyskano w badaniach
przeprowadzonych we Włoszech, Gambii i Izraelu.24-26
W porównaniu z okresem przed wprowadzeniem
szczepień, częstość wykrywania typów HPV
uwzględnionych w 4-walentnej szczepionce przeciwko
HPV (HPV-4) zmniejszyła się o 64% wśród
Amerykanek w wieku 14–19 lat i o 34% u kobiet w wieku 20–24 lat (p. Med. Prakt. Szczepienia 2/2016, s. 65 – przyp. red.).27 Redukcja ta jest większa
od oczekiwanej, ponieważ tylko 51% dziewcząt i kobiet w wieku 14–19 lat i 33% kobiet w wieku
20–24 lat otrzymało ≥1 dawkę HPV-4.27 W latach
2013–2014 u chłopców i mężczyzn w wieku
14–24 lat zamieszkujących w Stanach Zjednoczonych
rzadziej stwierdzano typy uwzględnione w HPV-4 niż typy nieszczepionkowe. Ta różnica
mogła w pewnym stopniu wynikać ze szczepień
młodych mężczyzn, jednak prawdopodobnie była
głównie związana z ochroną populacyjną uzyskaną
dzięki szczepieniom dziewcząt i młodych kobiet.28 U urodzonych w Australii nieszczepionych
mężczyzn w wieku ≤21 lat częstość występowania
typów HPV uwzględnionych w HPV-4 po wprowadzeniu
szczepień dziewcząt i młodych kobiet
zmniejszyła się o 31%.29 Dodatkowo w badaniu
przeprowadzonym w Danii stwierdzono zmniejszenie
zapadalności na brodawki płciowe z 365
do 77/100 000 osobolat u nieszczepionych młodych
mężczyzn, co korelowało ze szczepieniem przeciwko
HPV młodych kobiet.30
Celem wprowadzenia szczepień przeciwko
różyczce było zmniejszenie zapadalności na zespół
różyczki wrodzonej (CRS), który występuje w przypadku zakażenia wirusem różyczki nieodpornej
kobiety na początku ciąży. W Stanach Zjednoczonych
podjęto decyzję o szczepieniu małych
dzieci (zarówno chłopców, jak i dziewczynek), które
były głównym źródłem zakażenia wirusem różyczki,
dzięki czemu zapadalność na CRS szybko
się zmniejszyła.31 Natomiast w Wielkiej Brytanii i Japonii szczepieniami objęto dziewczęta przed
okresem pokwitania, aby im zapewnić bezpośrednią
ochronę przy wejściu w wiek rozrodczy. Niestety
zakażenia wirusem różyczki i przypadki CRS
obserwowano do czasu wprowadzenia powszechnych
szczepień młodszych dzieci obojga płci.32,33
Podstawy teoretyczne ochrony populacyjnej
W celu lepszego zrozumienia podłoża ochrony populacyjnej dzieci i dorosłych wynikającej z powszechnych szczepień dzieci poniżej opisano jej teoretyczne podstawy. Aby drobnoustrój chorobotwórczy przeżył, konieczne jest zakażenie (lub w wybranych przypadkach kolonizacja) nieodpornej osoby, która zaraża tym drobnoustrojem inne podatne osoby. W populacji, w której wszystkie osoby nie są odporne na daną chorobę, oczekiwaną liczbę osób, którą zarazi jeden chory, określa się jako podstawową liczbę odtwarzania (R0). Im większa jest R0, tym większa jest liczba kolejnych przypadków zachorowań i tym większa jest progowa liczba odpornych osób w populacji, przy której można zapobiec wybuchowi ogniska epidemicznego (tab. 2.). Niektóre drobnoustroje są wysoce zaraźliwe (np. R0 dla odry wynosi 12–18 przypadków, a dla krztuśca 5–17 przypadków), natomiast inne są względnie mało zaraźliwe, na przykład R0 dla grypy wynosi 1,4–4 przypadków (tab. 2.).10 Ponieważ rzadko się zdarza, aby cała populacja była nieodporna na zakażenie, rzeczywista liczba odtwarzania (Rn) oznacza obserwowaną liczbę osób, którą zaraził jeden chory. Rn charakteryzuje się dużą zmiennością pomiędzy populacjami, ponieważ zależy ona od biologicznych właściwości drobnoustroju (np. sposobu transmisji i czasu wydalania patogenu), czynników związanych z gospodarzem (np. częściowa odporność, wiek), cyklicznych zmian w epidemiologii choroby oraz wyjściowej odporności i niejednorodności populacji. Rn będzie się zmniejszać wraz ze zwiększaniem się poziomu odporności w populacji na skutek szczepień lub zakażenia danym drobnoustrojem.
| Tabela 2. Szacunkowe wartości R0 i związane z nimi wartości progowe dla eliminacji transmisji najczęstszych chorób, którym można zapobiegać poprzez szczepieniaa | |||
|---|---|---|---|
| Choroba | R0 | Niestandaryzowany progowy poziom odporności dla eliminacji transmisji (%) | |
| błonica | 6–7 | 83–85 | |
| grypab | 1,4–4 | 30–75 | |
| odra | 12–18 | 92–94 | |
| świnka | 4–7 | 75–86 | |
| krztusiec | 5–17 | 80–94 | |
| polioc | 2–20 | 50–95 | |
| różyczka | 6–7 | 83–85 | |
| ospa prawdziwa | 5–7 | 80–85 | |
| ospa wietrznad | 8–10? | ? | |
| a Wartości podane w tabeli są szacunkowe i nie odzwierciedlają w pełni dużych różnic w obrębie populacji. Nie przedstawiają również złożonych mechanizmów immunologicznych, od których zależy epidemiologia i utrzymywanie się zakażenia. Szczegóły omówiono w artykule. Odpowiednie wartości progowe obliczono wg wzoru: 1 - (1/R0). Przedrukowano i poprawiono za zgodą Fine i wsp.10 b R0 dla wirusów grypy prawdopodobnie jest bardzo zmienna w zależności od podtypu wirusa. c Ocena utrudniona z uwagi na brak jednoznacznych danych o odporności na zakażenie oraz wpływ poziomu higieny. d Odporność nie zapobiega zakażeniu, nie określono niestandaryzowanego progu odporności. R0 – podstawowa liczba odtwarzania | |||
Do eliminacji transmisji zakażenia niezbędny jest progowy odsetek odpornych osób w danej populacji (na ogół wyrażany jako [1 - (1/R0)] × 100 [p. ryc. 2.]).10 Dla przykładu, jeśli R0 dla wybranego drobnoustroju wynosi 4, to 1 zakażona osoba zarazi 4 inne osoby, zakładając, że cała populacja jest nieodporna na zakażenie. Jeżeli odsetek odpornych osób w populacji (poziom odporności) wynosi <75%, transmisja drobnoustroju będzie się utrzymywać i nasilać. Przy poziomie odporności >75% przeciętna zakażona osoba zarazi <1 kolejną osobę i ostatecznie transmisja zakażenia zostanie przerwana. Jeżeli 75% osób w populacji jest odpornych na daną chorobę, 1 chory zaraża średnio 1 osobę i transmisja zakażenia pozostanie na stałym poziomie (próg odporności [p. tab. 2.]). W populacji odsetek odpornych osób powinien być duży (≥92%), w przeciwnym razie zakażenia wysoce zaraźliwymi drobnoustrojami, takimi jak wirus odry i pałeczka krztuśca, nadal będą się rozprzestrzeniać. W przypadku mniej zaraźliwych patogenów (np. wirusa różyczki i świnki) transmisję zakażenia można zwykle zatrzymać przy mniejszym poziomie odporności – odpowiednio około 83 i 75%. Te wartości progowe mogą się różnić w zależności od wieku, rodzaju kontaktów społecznych i położenia geograficznego. Należy zauważyć, że teorie R0, Rn i poziomu odporności są bardzo złożone, a zrozumienie i możliwość modelowania ochrony populacyjnej będzie ewoluować.10 Niemniej jednak szacowany progowy poziom odporności dla eliminacji transmisji zakażenia powinien stanowić docelowy poziom wyszczepialności, dzięki któremu można uzyskać efekt ochrony populacyjnej.
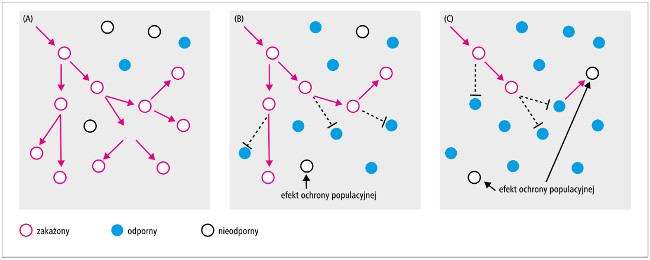
Ryc. 2. Transmisja drobnoustroju w populacji, dla którego podstawowa liczba odtwarzania wynosi 2. (A) Jeżeli uodporniono 12,5% populacji, transmisja drobnoustroju zwiększa się wykładniczo w kolejnym pokoleniu (dopóki nie dojdzie do nagromadzenia się wcześniej zakażonych osób). (B) Jeżeli uodporniono 50% populacji, transmisja zakażenia jest upośledzona i można zaobserwować efekt ochrony populacyjnej. (C) Jeżeli uodporniono 75% populacji, transmisja będzie ograniczona i ostatecznie ulegnie przerwaniu. Przedrukowano z: Fine P.E.M., Mulholland K., Scott J.A., Edmunds W.J.: Community protection. In: Plotkin S.A., Orenstein W.A., Offit P.A., Edwards K.M., eds.: Vaccines. Philadelphia, PA, Elsevier, 2018: 1512–1531. © 2018, with permission from Elsevier.
Chociaż osiągnięcie tych progowych poziomów jest niezbędne dla eliminacji choroby, w rozważaniach dotyczących ochrony populacyjnej często pomijano dane sugerujące, że nawet mniejsze wskaźniki wyszczepialności dzieci mogą znacząco zmniejszyć zapadalność na choroby zakaźne. Zgodnie z danymi przedstawionymi w tabeli 3., prognozowany matematycznie wpływ szczepień może zmniejszyć o >70% liczbę potencjalnych zachorowań aż do piątej generacji wtórnych przypadków zakażenia drobnoustrojem o R0 równym 4, jeśli odsetek zaszczepionej populacji wynosił tylko 25%. Na przykład, od czasu wprowadzenia w Stanach Zjednoczonych szczepień przeciwko wirusowemu zapaleniu wątroby (WZW) typu A ogólna liczba zachorowań zmniejszyła się o 98%, a w 2014 roku ≥2 dawki tej szczepionki otrzymało jedynie 58% dzieci.11,12 Dodatkowo roczny wskaźnik umieralności z powodu WZW typu A w grupie wiekowej 20–39 lat zmniejszył się o 48%, a w grupie wekowej ≥60 lat o 37% mimo bardzo małego wskaźnika wyszczepialności wśród dorosłych.34 Dane z amerykańskich systemów nadzoru wykazały zmniejszenie zapadalności na wiele chorób, którym można zapobiegać poprzez szczepienia, na długo przed osiągnięciem poziomu odporności niezbędnego do eliminacji choroby (ryc. 1.).
| Tabela 3. Prognozowane matematycznie zwiększanie się liczby przypadków choroby zakaźnej przy podstawowej liczbie odtwarzania równej 4 i niestandaryzowanym poziomie odporności 75%a | |||||||
|---|---|---|---|---|---|---|---|
| odsetek odpornych osób w populacji | rzeczywista liczba odtwarzania | 1. generacja | 2. generacja | 3. generacja | 4. generacja | 5. generacja | całkowita liczba zachorowań dla 5 generacji przypadków wtórnych |
| 0 | 4 | 4 | 16 | 64 | 256 | 1024 | 1364 |
| 25 | 3 | 3 | 9 | 27 | 81 | 243 | 363 |
| 50 | 2 | 2 | 4 | 8 | 16 | 32 | 62 |
| 75 | 1 | 1 | 1 | 1 | 1 | 1 | 5 |
| 100 | 0 | 0 | 0 | 0 | 0 | 0 | 0 |
| a Prognozowanie matematyczne dla nieskończonej populacji, która jest jednorodna, a osoby chore nie są zgrupowane, tylko rozmieszczone w populacji między osobami zdrowymi. Założenia te nie będą spełnione w rzeczywistych warunkach, szczególnie w przypadku zwiększającej się liczby generacji przypadków wtórnych. | |||||||
Ograniczenia szczepień i ochrony populacyjnej
Ochronę populacyjną można uzyskać dzięki
szczepieniom skierowanych wyłącznie przeciwko
drobnoustrojom, dla których człowiek jest jedynym
rezerwuarem, a nie przeciwko drobnoustrojom
bytującym w innych środowiskach (np. laseczka
tężca w glebie). Efekt ochrony populacyjnej jest
widoczny po wielu latach, jeżeli odstęp między
ostrym zakażeniem a związanymi z nim następstwami
jest odpowiednio długi, tak jak w przypadku
szczepionki przeciwko HPV, która zapobiega
zachorowaniom na nowotwory szyjki macicy oraz
jamy ustnej i gardła, oraz szczepionki przeciwko
WZW typu B w kontekście zapobiegania marskości
wątroby i rakowi wątrobowokomórkowemu.
Pojęcie „odporność” często odnosi się do ochrony
zarówno przed zakażeniem (replikacją drobnoustroju
bezobjawową lub z towarzyszącymi objawami
klinicznymi), jak i chorobą (zakażeniem oraz
związanymi z nim objawami). W rzeczywistości jest
to bardziej skomplikowane, ponieważ różne szczepionki
zapewniają zmienną ochronę przed nosicielstwem,
zakażeniem, zachorowaniem i zaraźliwością.
Na przykład za pomocą skoniugowanych szczepionek
można uzyskać ochronę przed nosicielstwem
Hib i S. pneumoniae, co ma wpływ na transmisję i skutkuje większą ochroną populacyjną. Częściowa
odporność może chronić zaszczepioną osobę przed
chorobą o ciężkim przebiegu (np. biegunką rotawirusową
wymagającą hospitalizacji), ale ochrona
przed łagodną chorobą lub bezobjawowym zakażeniem
jest mniejsza.35 Chociaż większość szczepionek
cechuje się dużą efektywnością, niektóre osoby
mogą nie wytworzyć odpowiedzi immunologicznej
po szczepieniu. Poza tym na immunogenność szczepionek
może wpływać wiek,36 choroby współistniejące37,38 i stosowane leki.39
Odporność może się również zmieniać, ponieważ
odpowiedź swoista na patogen zmniejsza się,
jeżeli nie jest ona odpowiednio często „wzmacniana”
poprzez kontakt z dzikim drobnoustrojem lub
szczepienie. Zanikająca odporność może osłabić
ochronę populacyjną i zwiększyć ryzyko pojawienia
się ognisk epidemicznych (np. nawrót zachorowań
na świnkę wśród zaszczepionych studentów
wyższych uczelni [p. Med. Prakt. Szczepienia 2/2018, s. 37–43 – przyp. red.]).40 Zatem osoby nieodporne często nie zdają sobie sprawy, że zależą
od ochrony populacyjnej.
W przypadku niektórych drobnoustrojów może
nastąpić zmiana w krążących szczepach, tj. częstszego
występowania tych nieuwzględnionych w składzie szczepionki (np. rotawirus G12P,8 typ
serologiczny 19A pneumokoka po wprowadzeniu
PCV-7 oraz H. influenzae typów innych niż b).41
Co ważne, obciążenia netto związane z chorobą
zawsze się zmniejszały po wprowadzeniu szczepień,
nawet jeśli notowano większą zapadalność
na choroby wywoływane przez typy nieszczepionkowe.14,21
Zjawisko ochrony populacyjnej obserwowano w odniesieniu do prawie wszystkich szczepionek
stosowanych u dzieci (ryc. 1., tab. 1.), z wyjątkiem
szczepienia przeciwko grypie, w przypadku którego
dane są niejednoznaczne. Monto i wsp.42 sugerowali,
że szczepienie dzieci w wieku szkolnym
może ograniczyć rozprzestrzenianie się wirusa
wśród domowników. Porównali wpływ szczepienia
przeciwko grypie w 2 miastach w stanie Michigan
– w jednym (Tecumseh) prowadzono szczepienia w szkołach, a w drugim (Adrian) takiego
programu nie realizowano. Po zaszczepieniu 86%
uczniów zapadalność na chorobę grypopodobną w gospodarstwach domowych w Tecumseh była
3-krotnie mniejsza. Dane z Japonii sugerują, że
obowiązkowe szczepienie dzieci w wieku szkolnym
zapobiegały rocznie 37 000–49 000 zgonów,
niezależnie od przyczyny. Efekt ten nie był widoczny
po zaprzestaniu obowiązkowych szczepień
uczniów.43 Jednak w badaniach populacyjnych nie
uzyskano jednoznacznych dowodów na wytworzenie
ochrony populacyjnej, co prawdopodobnie
wynika z częstych zmian szczepów wirusa grypy
krążących w populacjach i względnie małych
wskaźników wyszczepialności przeciwko grypie.
Uważa się, że szczepionki są ofiarą własnego
sukcesu.44 Ponieważ choroby, którym można zapobiegać
poprzez szczepienia, występują rzadko i zapomniano już o dużym ryzyku powikłań i zgonów z ich powodu (ryc. 1., tab. 1.), co częściowo jest
efektem ochrony populacyjnej nieszczepionych
osób, zwiększyło się zadowolenie społeczeństwa, a jednocześnie obawa przed możliwymi działaniami
niepożądanymi szczepionek, czego skutkiem
są niezdecydowane postawy wobec takich
metod uodpornienia.44,45 Nieszczepione dzieci
mogą uniknąć ryzyka powikłań i zgonów z powodu
chorób, którym można zapobiegać poprzez
szczepienia, dzięki ochronie zapewnianej przez
dzieci zaszczepione. Ochrona populacyjna może
wzbudzać fałszywe poczucie bezpieczeństwa, częściowo z uwagi na fakt, że wskaźniki wyszczepialności
mogą się istotnie różnić w obrębie tej samej
populacji, co wynika z nielosowego grupowania
się osób nieszczepionych.
Na przykład w badaniu z retrospektywnym
zbieraniem danych przeprowadzonym w stanie Colorado
oceniono wpływ braku zgody na szczepienia z powodów osobistych (tj. niezwiązanych z przeciwwskazaniami
medycznymi – przyp. red.) na ryzyko
zachorowań na odrę i krztusiec. Zaszczepione dzieci
(3–18 lat) zamieszkujące hrabstwa, w których
dużo osób rezygnowało ze szczepień należnych w wieku szkolnym, były narażone na większe
ryzyko zachorowania na odrę (ryzyko względne
[RR]: 1,6 [95% CI: 1,0–2,4]) i na krztusiec (RR:
1,9 [95% CI: 1,7–2,1]) niż dzieci z hrabstw o małym
odsetku rezygnacji ze szczepień.46 Ogniska
epidemiczne krztuśca notowano również częściej w szkołach z większym odsetkiem nieszczepionych
uczniów (śr. 4,3 vs 1,5%; p = 0,001).46 W okręgach, w których stwierdzano grupowanie się osób rezygnujących
ze szczepień, ryzyko zwiększonej
liczby zachorowań na krztusiec było 2,5-krotnie
większe.47,48 Ogniska epidemiczne odry, podobne
do ogniska w Disneylandzie z 2014 roku, łączono z przeniesieniem zakażenia do populacji o małych
wskaźnikach wyszczepialności.49
Maksymalizacja ochrony populacyjnej w przyszłości
Głównym celem szczepień powinna pozostać
bezpośrednia ochrona dzieci narażonych na zachorowania.
Działania te powinny obejmować racjonalne
rozszerzenie zaleceń dotyczących szczepień
na grupy ryzyka.35 Jeżeli chcemy osiągnąć
optymalne dodatkowe indywidualne i społeczne
korzyści z ochrony populacyjnej, konieczne są
intensywne działania mające na celu uzyskanie i utrzymanie dużych wskaźników wyszczepialności,
obejmujące m.in. zapewnienie dostępu
do szczepionek, ciągłą edukację na temat korzyści
ze szczepień, prowadzenie badań dotyczących
epidemiologii chorób przed wprowadzeniem szczepień i po ich wprowadzeniu, a także uwzględnienie
kwestii ochrony populacyjnej w ocenie efektywności
kosztowej szczepionek.
Kluczowe znaczenie dla utrzymaniu ochrony
populacyjnej ma zapewnienie dostępu do szczepionek
oraz objęcie szczepieniami wszystkich dzieci.
Amerykański program Vaccines for Children
zapewnia bezpłatne szczepienia szczepionkami
uwzględnionymi w zaleceniach Advisory Committee
on Immunization Practices (ACIP) i Centers
for Disease Control and Prevention. Program ten
poprawił wskaźniki wyszczepialności, szczególnie
wśród dzieci żyjących poniżej granicy ubóstwa.
Federalne i stanowe systemy opieki zdrowotnej
powinny dążyć nie tylko do usunięcia barier finansowych w realizacji szczepień, ale również
zapewnić zaopatrzenie w szczepionki, zwiększyć
świadomość społeczeństwa w zakresie zaleceń dotyczących
szczepień oraz usprawniać współpracę
pomiędzy stanowymi departamentami zdrowia a lokalnymi podmiotami związanymi z realizacją
szczepień ochronnych.50
Chociaż jest to trudne, badania powinny lepiej
modelować i przewidywać efekty ochrony populacyjnej,
które będą widoczne w przyszłości. Opisywanie
trendów zachorowalności w konkretnych
grupach wiekowych w odniesieniu do wskaźników
wyszczepialności może mieć zasadnicze znaczenie w podejmowaniu decyzji o realizacji szczepień
na szczeblu krajowym. Na przykład dzięki danym z systemu nadzoru potwierdzających przypadki
zachorowań u zaszczepionych osób, amerykański
ACIP zalecił podanie dawki przypominającej
szczepionki przeciwko odrze, śwince i różyczce
oraz przeciwko ospie wietrznej. Monitorowanie zjawiska
zastępowania serotypów oraz modelowanie
rozprzestrzeniania się drobnoustroju w populacji
może pomóc decydentom w ustaleniu, w jaki
sposób stosować aktualnie dostępne szczepionki
lub czy należy je zastąpić innymi preparatami
(np. zamiana PCV-7 na PCV-13). W ocenie możliwości
wytworzenia ochrony populacyjnej przed
rejestracją szczepionki można wykorzystać badania z randomizacją klasterową – randomizacji
podlegają grupy osób, a następnie porównuje się
ryzyko przeniesienia zakażenia w grupach zaszczepionych i nieszczepionych grupach kontrolnych.51 Ta metoda może być pomocna w badaniach
nad nowymi szczepionkami.
Ważne jest, aby w miarę możliwości w analizie
ekonomicznej programów szczepień uwzględnić
oszczędności w kosztach opieki zdrowotnej wynikające z ochrony populacyjnej. W amerykańskim
badaniu stwierdzono, że dzięki programowi
szczepień dzieci w 2009 roku zaoszczędzono
20 miliardów dolarów jako koszty bezpośrednie,
lecz po uwzględnieniu kosztów pośrednich, takich
jak absencja rodziców w pracy i koszty związane z dojazdem do przychodni, oszczędności wyniosły
76 miliardów dolarów.52 Dodatkowo szczepienia
wpłynęły na stosowanie antybiotyków o szerokim
zakresie działania53 oraz oporność na leki
przeciwdrobnoustrojowe dzięki zmniejszeniu
krążenia w populacji bakterii opornych na wiele
antybiotyków.14 Analizy efektywności kosztowej i modelowanie matematyczne, które prawidłowo
uwzględniają w obliczeniach ochronę populacyjną,
mają istotny wpływ na politykę szczepień. W niektórych
przypadkach szczepionki okazały się
być efektywniejsze kosztowo, gdy uznano wpływ
ochrony populacyjnej.54
Wnioski
Poddając się szczepieniu, uzyskuje się nie tylko bezpośrednią ochronę, ale również chroni się rodzinę, przyjaciół i inne osoby przed zakażeniem poprzez zablokowanie transmisji zakażenia na osoby z kontaktu. Ochrona populacyjna ma kluczowe znaczenie dla nieodpornych osób, których ochrona przed chorobami zakaźnymi zależy od dużego wskaźnika wyszczepialności w populacji. Do tej grupy należą niemowlęta, które nie mogą być szczepione ze względu na zbyt młody wiek, kobiety ciężarne, osoby w podeszłym wieku oraz osoby z niedoborem odporności (np. z chorobą nowotworową). Efekty ochrony populacyjnej uzyskanej dzięki szczepieniom można wykorzystać w innych sferach zdrowia publicznego, takich jak oporność drobnoustrojów na antybiotyki, grypa pandemiczna, zakażenia wirusem ebola i zika. Ochrona populacyjna uzyskana dzięki skutecznym programom szczepień dzieci i dorosłych ma istotne znaczenie dla poprawy stanu zdrowia całej populacji.
Podziękowania: Elizabeth Briere, Sandy Roush, Charles Vitek i Michael Iademarco dostarczyli część danych epidemiologicznych
wykorzystanych w artykule. Autorzy dziękują również Ramowi
Yogevowi, który niedawno przeszedł na emeryturę. Prowadzone z nim dyskusje o szczepieniach dzieci zaowocowały powstaniem
niniejszego artykułu.
Konflikt interesów: E.J.A. otrzymał fundusze na prowadzenie badań
klinicznych od MedImmune, Regeneron, PaxVax oraz od NovaVax, a także pełnił funkcję konsultanta dla AbbVie. Pozostali autorzy nie
zgłosili potencjalnych konfliktów interesów. Wszyscy autorzy
dostarczyli formularz ICMJE ujawnienia konfliktu interesów. Redakcja
ujawniła wszystkie konflikty, które były związane z artykułem.
Piśmiennictwo:
1. Roush S.W., Murphy T.V., Vaccine-Preventable Disease Table Working Group: Historical comparisons of morbidity and mortality for vaccine-preventable diseases in the United States. JAMA, 2007; 298: 2155–21632. Hill H.A., Elam-Evans L.D., Yankey D., Singleton J.A., Dietz V.: Vaccination coverage among children aged 19–35 months – United States, 2015. MMWR, 2016; 65: 1065–1071
3. Adams D.A., Fullerton K., Jajosky R.A. et al.: Summary of notifiable infectious diseases and conditions – United States, 2013. MMWR, 2015; 62: 1–122
4. Simpson D.M., Ezzati-Rice T.M., Zell E.R.: Forty years and four surveys: how does our measuring measure up? Am. J. Prev. Med., 2001; 20: 6–14
5. National Immunization Survey (NIS) – children (19–35 months). Available at: www.cdc.gov/vaccines (Accessed 30 November 2016)
6. Adams D.A., Thomas K.R., Jajosky R.A. et al.: Summary of notifiable infectious diseases and conditions – United States, 2014. MMWR, 2016; 63: 1–152
7. Centers for Disease Control and Prevention. Summary of notifiable diseases in the United States. MMWR, 1980; 28: 1–96
8. Centers for Disease Control and Prevention. Summary of notifiable diseases, United States, 1993. MMWR, 1994; 42: 1–73
9. Adams D.A., Jajosky R.A., Ajani U., et al.: Summary of notifiable diseases – United States, 2012. MMWR, 2014; 61: 1–121
10. Fine P.E.M., Mulholland K., Scott J.A., Edmunds W.J.: Community protection. (In:) Plotkin S.A., Orenstein W.A., Offit P.A., Edwards K.M., eds. Vaccines. Philadelphia, PA, Elsevier, 2018: 1512–1531
11. Centers for Disease Control and Prevention. Notice to readers: final 2013 reports of nationally notifiable infectious diseases. MMWR, 2014; 63: 702
12. Hill H.A., Elam-Evans L.D., Yankey D., Singleton J.A., Kolasa M.: National, state, and selected local area vaccination coverage among children aged 19–35 months – United States, 2014. MMWR, 2015; 64: 889–896
13. Poehling K.A., Talbot T.R., Griffin M.R., et al.: Invasive pneumococcal disease among infants before and after introduction of pneumococcal conjugate vaccine. JAMA, 2006; 295:1668–1674
14. Moore M.R., Link-Gelles R., Schaffner W., et al.: Effect of use of 13-valent pneumococcal conjugate vaccine in children on invasive pneumococcal disease in children and adults in the USA: analysis of multisite, population-based surveillance. Lancet Infect. Dis., 2015; 15: 301–309
15. Whitney C.G., Farley M.M., Hadler J., et al.: Active Bacterial Core Surveillance of the Emerging Infections Program Network. Decline in invasive pneumococcal disease after the introduction of protein-polysaccharide conjugate vaccine. N. Engl. J. Med., 2003; 348: 1737–1746
16. Simonsen L., Taylor R.J., Young-Xu Y., Haber M., May L., Klugman K.P.: Impact of pneumococcal conjugate vaccination of infants on pneumonia and influenza hospitalization and mortality in all age groups in the United States. MBio, 2011; 2: e00309–10
17. Pingali S.C., Warren J.L., Mead A.M., Sharova N., Petit S., Weinberger D.M.: Association between local pediatric vaccination rates and patterns of pneumococcal disease in adults. J. Infect. Dis., 2016; 213: 509–515
18. Cortese M.M., Tate J.E., Simonsen L., Edelman L., Parashar U.D.: Reduction in gastroenteritis in United States children and correlation with early rotavirus vaccine uptake from national medical claims databases. Pediatr. Infect. Dis. J., 2010; 29: 489–494
19. Gastanaduy P.A., Curns A.T., Parashar U.D., Lopman B.A.: Gastroenteritis hospitalizations in older children and adults in the United States before and after implementation of infant rotavirus vaccination. JAMA, 2013; 310: 851–853
20. Leshem E., Tate J.E., Steiner C.A., Curns A.T., Lopman B.A., Parashar U.D.: Acute gastroenteritis hospitalizations among US children following implementation of the rotavirus vaccine. JAMA, 2015; 313: 2282–2284
21. Anderson E.J., Shippee D.B., Weinrobe M.H., et al.: Indirect protection of adults from rotavirus by pediatric rotavirus vaccination. Clin. Infect. Dis., 2013; 56: 755–760
22. Moulton L.H., Chung S., Croll J., Reid R., Weatherholtz R.C., Santosham M.: Estimation of the indirect effect of Haemophilus influenzae type b conjugate vaccine in an American Indian population. Int. J. Epidemiol., 2000; 29: 753–756
23. Adams W.G., Deaver K.A., Cochi S.L., et al.: Decline of childhood Haemophilus influenzae type b (Hib) disease in the Hib vaccine era. JAMA, 1993; 269: 221–226
24. Adegbola R.A., Secka O., Lahai G., et al.: Elimination of Haemophilus influenzae type b (Hib) disease from The Gambia after the introduction of routine immunization with a Hib conjugate vaccine: a prospective study. Lancet, 2005; 366: 144–150
25. Dagan R., Fraser D., Roitman M., et al. Israeli Pediatric Bacteremia and Meningitis Group. Effectiveness of a nationwide infant immunization program against Haemophilus influenzae b. Vaccine, 1999; 17: 134–141
26. Gallo G., Ciofi degli Atti M.L., Cerquetti M., Piovesan C., Tozzi A.E., Salmaso S.: Impact of a regional Hib vaccination programme in Italy. Vaccine, 2002; 20: 993–995
27. Markowitz L.E., Liu G., Hariri S., Steinau M., Dunne E.F., Unger E.R.: Prevalence of HPV after introduction of the vaccination program in the United States. Pediatrics, 2016; 137: e20151968
28. Gargano J.W., Unger E.R., Liu G. et al.: Prevalence of genital human papillomavirus in males, United States, 2013–2014. J. Infect. Dis., 2017; 215: 1070–1079
29. Chow E.P., Machalek D.A., Tabrizi S.N., et al.: Quadrivalent vaccine-targeted human papillomavirus genotypes in heterosexual men after the Australian female human papillomavirus vaccination programme: a retrospective observational study. Lancet Infect. Dis., 2016; 17: 68–77
30. Bollerup S., Baldur-Felskov B., Blomberg M.,Baandrup L., Dehlendorff C., Kjaer S.K.: Significant reduction in the incidence of genital warts in young men 5 years into the Danish human papillomavirus vaccination program for girls and women. Sex Transm. Dis., 2016; 43: 238–242
31. Williams N.M., Preblud S.R.: Rubella and congenital rubella surveillance, 1983. MMWR CDC Surveill. Summ., 1984; 33: 1SS–10SS
32. Anderson R.M., Grenfell B.T.: Quantitative investigations of different vaccination policies for the control of congenital rubella syndrome (CRS) in the United Kingdom. J. Hyg. (Lond), 1986; 96: 305–333
33. Nationwide rubella epidemic – Japan, 2013. MMWR, 2013; 62: 457–462
34. Vogt T.M., Wise M.E., Bell B.P., Finelli L.: Declining hepatitis A mortality in the United States during the era of hepatitis A vaccination. J. Infect. Dis., 2008; 197: 1282–1288
35. Anderson E.J.: Time to begin a new chapter and expand rotavirus immunization. Clin. Infect. Dis., 2014; 59: 982–986
36. Mulligan M.J., Bernstein D.I., Winokur P., et al.: DMID 13–0032 H7N9 Vaccine Study Group. Serological responses to an avian influenza A/H7N9 vaccine mixed at the point-of-use with MF59 adjuvant: a randomized clinical trial. JAMA, 2014; 312: 1409–1419
37. Nath K.D., Burel J.G., Shankar V., et al.: Clinical factors associated with the humoral immune response to influenza vaccination in chronic obstructive pulmonary disease. Int. J. Chron. Obstruct. Pulmon. Dis., 2014; 9: 51–56
38. Brydak L.B., Machała M., Centkowski P., Warzocha K., Biliński P.: Humoral response to hemagglutinin components of influenza vaccine in patients with non-Hodgkin malignant lymphoma. Vaccine, 2006; 24: 6620–6623
39. Yri O.E., Torfoss D., Hungnes O., et al.: Rituximab blocks protective serologic response to influenza A (H1N1) 2009 vaccination in lymphoma patients during or within 6 months after treatment. Blood, 2011; 118: 6769–6771
40. Patel L.N., Arciuolo R.J., Fu J., et al.: Mumps outbreak among a highly vaccinated university community – New York City, January–April 2014. Clin. Infect. Dis., 2017; 64: 408–412
41. MacNeil J.R., Cohn A.C., Farley M., et al.: Current epidemiology and trends in invasive Haemophilus influenzae disease – United States, 1989–2008. Clin. Infect. Dis., 2011; 53: 1230–1236
42. Monto A.S., Davenport F.M., Napier J.A., Francis T. Jr: Modification of an outbreak of influenza in Tecumseh, Michigan by vaccination of schoolchildren. J. Infect. Dis., 1970; 122: 16–25
43. Reichert T.A., Sugaya N., Fedson D.S., Glezen W.P., Simonsen L., Tashiro M.: The Japanese experience with vaccinating schoolchildren against influenza. N. Engl. J. Med., 2001; 344: 889–896
44. Orenstein W.A., Ahmed R.: Simply put: vaccination saves lives. Proc. Natl. Acad. Sci. USA, 2017; 114: 4031–4033
45. Edwards K.M.: State mandates and childhood immunization. JAMA, 2000; 284: 3171–3173
46. Feikin D.R., Lezotte D.C., Hamman R.F., Salmon D.A., Chen R.T., Hoffman R.E.: Individual and community risks of measles and pertussis associated with personal exemptions to immunization. JAMA, 2000; 284: 3145–3150
47. Omer S.B., Enger K.S., Moulton L.H., Halsey N.A., Stokley S., Salmon D.A.: Geographic clustering of nonmedical exemptions to school immunization requirements and associations with geographic clustering of pertussis. Am. J. Epidemiol., 2008; 168: 1389–1396
48. Atwell J.E., Van Otterloo J., Zipprich J., et al.: Nonmedical vaccine exemptions and pertussis in California, 2010. Pediatrics, 2013; 132: 624–630
49. Halsey N.A., Salmon D.A.: Measles at Disneyland, a problem for all ages. Ann. Intern. Med., 2015; 162: 655–656
50. Protecting the public’s health: critical functions of the Section 317 Immunization Program – a report of the National Vaccine Advisory Committee. Public Health Rep., 2013; 128: 78–95
51. Clemens J., Shin S., Ali M.: New approaches to the assessment of vaccine herd protection in clinical trials. Lancet Infect. Dis., 2011; 11: 482–487
52. Zhou F., Shefer A., Wenger J., et al.: Economic evaluation of the routine childhood immunization program in the United States, 2009. Pediatrics, 2014; 133: 557–585
53. National Vaccine Advisory Committee. A call for greater consideration for the role of vaccines in national strategies to combat antibiotic-resistant bacteria: recommendations from the National Vaccine Advisory Committee – approved by the National Vaccine Advisory Committee on June 10, 2015. Public Health Rep., 2016; 131: 11–16
54. Dhankhar P., Nwankwo C., Pillsbury M., et al.: Public health impact and cost-effectiveness of hepatitis a vaccination in the United States: a disease transmission dynamic modeling approach. Value Health, 2015; 18: 358–367