SPECJALNIE dla „Medycyny Praktycznej – Szczepień”

|
dr n. med. Ryszard Konior Kierownik Oddziału Pediatrii i Neurologii Dziecięcej Krakowskiego Szpitala Specjalistycznego im. Jana Pawła II w Krakowie |
Skróty: IChM – inwazyjna choroba meningokokowa, PSO – program szczepień ochronnych
Wprowadzenie
Inwazyjna choroba meningokokowa (IChM) należy
do najcięższych pozaszpitalnych zakażeń bakteryjnych
jakie mogą wystąpić u człowieka. Obarczona
jest bardzo dużą śmiertelnością oraz dużym
ryzykiem trwałych powikłań (p. Med. Prakt. Szczepienia 3/2017, s. 29–39 – przyp. red.). Z powodu
zmieniającej się epidemiologii szczepienia
przeciwko meningokokom, w odróżnieniu od innych
szczepień ochronnych, wymagają okresowej
modyfikacji. Jak dotąd nie opracowano bowiem
uniwersalnej szczepionki przeciwko wszystkim
chorobotwórczym meningokokom. Przypomnijmy,
że wśród 13 znanych grup serologicznych
meningokoków, które rozróżniamy na podstawie
składu polisacharydowego otoczki, 6 uważanych
jest za chorobotwórcze. Należą do nich grupy: A,
B, C, X, Y i W135, przy czym za >90% zakażeń
na świecie odpowiadają meningokoki z grupy: A,
B, C, W-135 i Y.
Niektóre kraje europejskie wprowadziły powszechne,
refundowane szczepienia przeciwko
meningokokom grupy C, B i/lub A, C, W-135 i Y
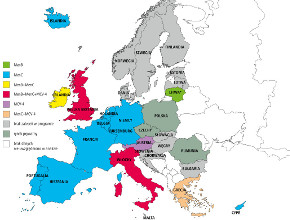
(p. Programy powszechnych szczepień przeciwko meningokokom w Europie – przyp. red.). Czy jest szansa na wprowadzenie
takich szczepień w Polsce?
Kilka niewiadomych
Meningokoki są rozpowszechnione na całym świecie, ale dystrybucja poszczególnych typów serologicznych w różnych regionach geograficznych podlega niewyjaśnionym jeszcze prawom. Nie wiemy, dlaczego grupa A, która co roku wywołuje zachorowania epidemiczne na terenie Afryki Subsaharyjskiej, obecnie praktycznie nie występuje w Europie, a jeszcze 50 lat temu obserwowano ją nawet na terenie Polski. Nie rozumiemy również, dlaczego w ciągu ostatnich 30 lat zachorowania epidemiczne wywołane grupą C oraz W-135 miały inny przebieg niż zachorowania wywołane przez grupę B. O ile epidemie wywołane meningokokami grupy C i W-135 miały ostry przebieg, trwały tylko kilka lat i wygasały samoistnie, to w przypadku meningokoków grupy B mieliśmy do czynienia z tzw. pełzającymi wieloletnimi epidemiami, które praktycznie udało się zatrzymać dopiero dzięki szczepieniom. Tak było w przypadku epidemii na Kubie (w latach 1976–1992), w Norwegii (w latach 1974–1990) oraz w Nowej Zelandii (w latach 1991–2007).1
Nosicielstwo
Dla zrozumienia sposobu rozpowszechniania się zakażeń meningokokowych najważniejsza jest informacja, że jedyną niszą ekologiczną dla meningokoków jest błona śluzowa nosowej częsci gardła człowieka. Zatem źródłem zakażenia meningokokowego może być wyłącznie inny człowiek, który jest nosicielem tej bakterii. Transmisja meningokoków następuje drogą kropelkową w bezpośrednim kontakcie człowieka z drugim człowiekiem. Nosicielami meningokoków na całym świecie jest około 10% populacji. Nosicielstwo to może być większe w środowiskach zamkniętych (internaty, bazy wojskowe, więzienia) i wynosić nawet 80–100%. Niejasne jest nadal, dlaczego przy tak częstym nosicielstwie meningokoków zapadalność na IChM jest stosunkowo nieduża. Aby zachorować na IChM, konieczna jest zatem wcześniejsza kolonizacja nosowej częsciej gardła i nabycie nosicielstwa. Musimy sobie zdać sprawę z tego, że żyjemy w Europie, w której nie ma już barier granicznych i tym samym ograniczeń w podróżowaniu. Co roku pomiędzy krajami Unii Europejskiej (UE) przemieszczają się miliony ludzi. Dotyczy to również Polaków. Wiele spośród naszej młodzieży uczy się w szkołach lub studiuje na uczelniach zagranicznych. Równie dużo młodzieży z innych krajów Europy i świata przebywa w Polsce choćby czasowo. W tej grupie wiekowej jest najwięcej nosicieli meningokoków, dlatego młodzież odpowiada za szerokie rozprzestrzenianie się tych bakterii w populacji. Jest to zatem całkowicie odmienna sytuacja niż w przypadku pneumokoków, gdzie decydującą rolę w ich rozprzestrzenianiu się odgrywają małe dzieci. Jak wynika z metaanalizy opublikowanej w „The Lancet”, największe nosicielstwo meningokokowe przypada na 19. rok życia (śr. 23% osób będących nosicielami) i utrzymuje się na dużym poziomie nawet do 25. roku życia.2 Inne badania nosicielstwa przeprowadzone w Wielkiej Brytanii oraz Holandii wykazały, że skokowe (nawet 3-krotne) zwiększenie nosicielstwa, z bardzo małego u małych dzieci, ma miejsce w wieku około 14–15 lat, czyli w okresie zmiany szkoły na średnią, a potem jeszcze bardziej dramatycznie zwiększa się zaraz po rozpoczęciu nauki na uczelniach wyższych, osiągając nawet 60%. Obserwacje te potwierdzają badania przeprowadzone na Uniwersytecie Nottingham w Wielkiej Brytanii.3-5 Wiąże się to z podejmowaniem tzw. ryzykownych zachowań, czyli przebywaniem w zatłoczonych pomieszczeniach (kluby młodzieżowe, puby), czynnym i biernym paleniem, używaniem wspólnych szklanek i sztućców, a także intymnymi pocałunkami z wieloma partnerami.6
Jaką bronią dysponujemy?
Szczepionki przeciwko meningokokom można podzielić na trzy grupy. Najstarsze z nich to szczepionki polisacharydowe, zawierające jako antygen jeden rodzaj otoczki wielocukrowej meningokoka lub kilka pochodzących od różnych grup, na przykład A oraz C lub A, C, W-135 i Y. Z powodu małej immunogenności u małych dzieci oraz braku efektu pamięci immunologicznej szczepionek tych nie należy stosować do pierwotnego uodpornienia. Z powodzeniem można je natomiast podawać jako dawki przypominające po szczepieniu szczepionkami skoniugowanymi. Szczepionki skoniugowane, podobnie jak polisacharydowe, posiadają jako antygen otoczki polisacharydowe, ale są one połączone z białkiem, którym najczęściej jest toksyna tężcowa (TT) lub zmodyfikowana genetycznie toksyna błonicza (CRM197). Takie połączenie sprawia, że szczepionki te są immunogenne nawet u najmłodszych niemowląt, wytwarzają pamięć immunologiczną i ograniczają nosicielstwo, co w przypadku ich powszechnego stosowania może prowadzić do wytworzenia odporności populacyjnej. Na polskim rynku dostępne są następujące szczepionki skoniugowane: NeisVac C (MCVC), Meningitec (MCVC), Nimenrix (MenACWY) i Menveo (MenACWY).7-10 Do trzeciej grupy należą szczepionki białkowe skierowane przede wszystkim przeciwko meningokokom grupy B. To najnowsze osiągnięcie współczesnej wakcynologii, bowiem wcześniej nie udało się opracować skutecznej szczepionki na podstawie antygenu otoczkowego tej grupy (p. Med. Prakt. Szczepienia 2/2016, s. 47–55 – przyp. red.). Wiemy już, że szczepionki te charakteryzują się dobrą immunogennością, ale z powodu ich krótkiego stosowania nie wiemy, czy wpływają na nosicielstwo meningokoków. Nie wiemy też, jak długo będzie się utrzymywać skuteczność szczepienia i w związku z tym, czy w przyszłości konieczne będzie podanie dawki przypominającej. W Europie zarejestrowane są 2 szczepionki przeciwko meningokokom grupy B: Bexsero, którą można stosować już po ukończeniu 2. miesiąca życia, oraz Trumenba, której obecna rejestracja pozwala na stosowanie u dzieci >10. roku życia.11,12
W jakim miejscu jest Europa?
Polskie i europejskie dane epidemiologiczne wskazują
na dużą zmienność zapadalności na IChM w zależności od miejsca zamieszkania oraz czasu.
Okresowo w Europie pojawiają się bardziej
inwazyjne klony meningokokowe odpowiedzialne
za zwiększenie zapadalności, powstawanie ognisk
epidemicznych oraz większą śmiertelność. Po pewnym
czasie te inwazyjne klony są wypierane przez
inne mniej inwazyjne, a po kilku latach pojawiają
się ponownie. Czasem jest to ten sam materiał
genetyczny skryty pod inną otoczką polisacharydową.
W krajach, w których wprowadzono powszechne
szczepienia szczepionkami skoniugowanymi
(p. ryc. 2., Programy powszechnych szczepień przeciwko meningokokom w Europie – przyp. red.), a co za tym idzie
uzyskano odporność populacyjną, udało się w ten
sposób ewidentnie zmniejszyć liczbę zachorowań
na IChM. Takie zjawisko obserwowano po wprowadzeniu
szczepień przeciwko meningokokom grupy
C w pierwszym dziesięcioleciu obecnego wieku w Wielkiej Brytanii, Holandii, Belgii i Hiszpanii.
W jakim miejscu jesteśmy teraz w Polsce?
W Polsce szczepionki przeciwko meningokokom
są zalecane, ale nie refundowane, a ich stosowanie
nie jest powszechne. Ocenia się, że w latach
2007–2010, kiedy w Polsce obserwowano zwiększenie
zachorowalności na IChM wywołaną przez
meningokoki grupy C oraz powstanie wielu ognisk
epidemicznych, MCVC podano ponad 500 000 dzieci i młodzieży (na podstawie szacunkowej liczby
sprzedanych dawek szczepionek), ale było to stanowczo
za mało, aby wzbudzić odporność populacyjną.
Po zmniejszeniu zapadalności na IChM
po 2010 roku i zniknięciu z mediów informacji o przypadkach posocznicy wyszczepialność dramatycznie
się zmniejszyła.
O ile w okresie występowania ognisk epidemicznych w latach 2007–2011 zapadalność na IChM w Polsce oscylowała pomiędzy 0,70 a 1,03/100 000/rok, ze szczytem w 2007 (1,03/100 000) i 2008
roku (0,98/100 000), to później w latach 2012–2017
zmniejszyła się do 0,49–0,63/100 000/rok. W 2017
roku zarejestrowano 228 przypadków IChM, co
przekłada się na zapadalność rzędu 0,59/100 000.
Na przestrzeni ostatnich 10 lat wyraźnie widać
dużą różnicę w zapadalności w zależności od rejonu
zamieszkania. Przez cały ten czas duża
zapadalność utrzymywała się w województwach
północnych: pomorskim, zachodnio-pomorskim i warmińsko-mazurskim, zwykle wynosiła blisko
1/100 000, a okresowo nawet 1,45/100 000.13
Największa zapadalność na IChM przypada
na 1. rok życia. W ostatnich latach wahała się ona
12–16/100 000/rok, w 2. roku życia 2,5–8, a w każdym
następnym do 5. roku życia 2–4/100 000,
dlatego niemowlęta i dzieci <5. roku życia powinny
stanowić w Polsce pierwszy cel szczepień przeciwko
meningokokom. Po 5. roku życia zapadalność
wyraźnie się zmniejsza, aby znów się zwiększyć u młodzieży w wieku 15–19 lat. Na dużym poziomie
utrzymuje się aż do okresu młodej dorosłości
włącznie (20–24 lat).13-16
Młodzież i młodzi dorośli w wieku 15–24 lat
to ważna grupa wiekowa zachorowań na IChM. W Europie, w tej grupie wiekowej zachodzi szczególna
dysproporcja pomiędzy jej odsetkiem w całej
populacji (11,2%) a odsetkiem zachorowań na IChM
(17,5%). W porównaniu z całą populacją dorosłych
(<65. rż.), populacja młodzieży i młodych dorosłych
charakteryzuje się największą śmiertelnością z powodu
IChM.17,18 Nie bez znaczenia dla takiego skutku
choroby u młodzieży i młodych dorosłych jest
fakt, że klasyczne objawy IChM są bardziej zamaskowane, a osutka krwotoczna pojawia się później
niż u niemowląt i małych dzieci. Z tego powodu w tej grupie wiekowej czas pomiędzy początkiem
choroby a przyjęciem do szpitala jest prawie 2-krotnie
dłuższy niż u niemowląt (22 vs 13 h).19
W Europie dominują zachorowania wywołane
przez grupy B i C, choć w ostatnich latach zaobserwowano
zwiększenie liczby zachorowań spowodowanych
serotypami Y oraz W-135. W związku z tym w niektórych krajach UE, gdzie wcześniej
prowadzono szczepienia populacyjne szczepionką
MCVC, zmieniła się profilaktyka zakażeń meningokokowych.
Preparat MCVC zastąpiono MenACWY, a u młodzieży w wieku 12–15 lat wprowadzono
dodatkowe szczepienie preparatem MenACWY. W Polsce dominują zachorowania wywołane serotypem
B, które stanowią średnio 70% wszystkich
zakażeń, a w populacji dzieci <1. roku życia nawet
blisko 90%. Za większość pozostałych zachorowań
odpowiadają meningokoki grupy C (śr. 25%, w populacji
dzieci <1. rż. – 10%) oraz w niewielkim stopniu
inne grupy.14-16 Znaczenie grup innych niż B i C
zwiększa się wraz z wiekiem (p. ryc.).
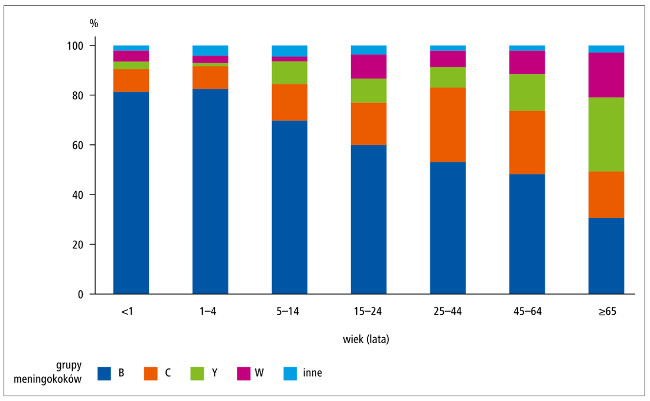
Ryc. Dystrybucja zachorowań na IChM w zależności od grupy meningokoków i wieku pacjentów w krajach Unii Europejskiej/Europejskiego Obszaru Gospodarczego (ECDC 2014). Uwzględniono dane pochodzące z Hiszpanii, Holandii, Litwy, Luksemburgu, Łotwy, Malty, Norwegii, Polski, Portugalii, Rumunii, Słowacji, Słowenii, Szwecji, Wielkiej Brytanii.
Będziemy musieli poczekać
W świetle przedstawionych polskich danych epidemiologicznych,
przy stosunkowo małej zapadalności
na IChM w ostatnich latach i bardzo
dużych kosztach zakupu szczepionek, zwłaszcza
przeciwko meningokokom grupy B, obecnie nie
ma szans na ich wprowadzenie do obowiązkowego
programu szczepień ochronnych (PSO) dla całej
populacji niemowląt. O ile powszechne szczepienia
przeciwko meningokokom typu C wprowadzane w Europie zachodniej po 2000 roku w okresie hiperepidemicznym
są kontynuowane, to powszechne
szczepienia niemowląt przeciwko meningokokom
grupy B zostały wprowadzono tylko w 3 krajach
europejskich (w Irlandii, Wielkiej Brytanii i we Włoszech). W lipcu 2018 roku planowane jest
rozpoczęcie szczepień przeciwko meningokokom
grupy B również na Litwie, gdzie zapadalność
jest zdecydowanie większa niż w Polsce (p. ryc. 1., Programy powszechnych szczepień przeciwko meningokokom w Europie – przyp. red.). Analizy farmako-ekonomiczne
przeprowadzone niedawno dla Niemiec, Francji
oraz Holandii, krajów o podobnej do Polski zapadalności
na IChM, nie skłoniły jeszcze władz
tych krajów do wprowadzenia szczepionki przeciwko
meningokokom grupy B do PSO. Na decyzję o powszechnym zastosowaniu tej szczepionki w przyszłości z pewnością wpłynie informacja, czy
ogranicza ona nosicielstwo.20-25
W Polsce priorytetem powinno być wprowadzenie
obowiązkowych szczepień przeciwko meningokokom
grupy B oraz A, C, W-135 i Y w ściśle
określonych grupach ryzyka, takich jak w zaleceniach
Advisory Committee on Immunization
Practices (ACIP), ponieważ prawdopodobieństwo
zachorowania na IChM w niektórych z tych grup
zwiększa się nawet 1000-krotnie (p. ramka).26-27
Mimo obecnie obserwowanej stosunkowo małej
zapadalności na IChM, należy pamiętać o dramatycznych
skutkach zachorowania oraz o zmiennym
charakterze epidemiologii tej choroby. Ponieważ
nie wiadomo, czy w najbliższych latach
zapadalność na IChM ponownie się nie zwiększy,
szczepienia przeciwko meningokokom należy zalecać
wszystkim, a zwłaszcza grupom wiekowym
charakteryzującym się największą zapadalnością,
do których należą:
- niemowlęta (MenB + MenC lub MenACWY)
- małe dzieci (MenB oraz MenACWY)
- młodzież i młodzi dorośli (Men B, jeśli nie byli szczepieni wcześniej tą szczepionką, a MenACWY nawet gdy byli szczepieni MCV-C lub MenACWY w okresie wczesnodziecięcym); optymalnie szczepienie należy przeprowadzić w wieku 12–15 lat, czyli w okresie poprzedzającym skok nosicielstwa meningokokowego
- osoby podróżujące lub zamieszkujące czasowo (niezależnie od wieku) w krajach, w których IChM występuje hiperepidemicznie (zwłaszcza gdy utrzymują bliski i przedłużony kontakt z lokalną ludnością).
Ramka. Grupy ryzyka, które należy objąć obowiązkowymi i refundowanymi szczepieniami przeciwko meningokokom:
- osoby z anatomiczną lub czynnościową asplenią
- osoby z wrodzonymi lub nabytymi niedoborami w układzie dopełniacza (C3, C5-C9), properdyny oraz czynnika H i D
- osoby przyjmujące ekulizumab (Soliris) stosowany w leczeniu nocnej napadowej hemoglobinurii oraz atypowym zespole hemolityczno-nerczycowym
- osoby zakażone HIV
- pracownicy laboratoriów mikrobiologicznych, którzy rutynowo mają kontakt z izolatami Neisseria meningitidis
- osoby z grup zwiększonego ryzyka w przypadku wystąpienia ogniska epidemicznego (wybór szczepionki zależy od serotypu meningokokowego, który odpowiada za wystąpienie danego ogniska).
Podsumowanie
Decyzja o rozpoczęciu powszechnych, refundowanych szczepień przeciwko meningokokom zależy od wielu czynników: zapadalności na daną chorobę w populacji, konsekwencji zdrowotnych zachorowania, obecności lub braku efektu populacyjnego po wprowadzeniu szczepień, ale również od wielkości środków finansowych przeznaczanych na ochronę zdrowia w danym kraju. W obecnej sytuacji próżno czekać na wprowadzenie obowiązkowych szczepień przeciwko meningokokom w całej populacji niemowlęcej, ani też w grupie młodzieżowej (tak jak w Stanach Zjednoczonych). Być może jest szansa na refundowane szczepienia w grupach ryzyka, a jeżeli nie to może jest to miejsce na finansowanie w ramach samorządowych programów profilaktyki? Póki co, nam, lekarzom i pielęgniarkom, pozostaje uświadamiać naszych pacjentów i rodziców małych pacjentów o zagrożeniach jakie mogą nieść] ze sobą meningokoki i wyraźnie zalecać szczepienia przeciwko tym bakteriom.
Piśmiennictwo:
1. Granoff M.D., Pelton S., Harrison H.L.: Meningococcal diseases. (W): Plotkin S.A., Orenstein W.A., Offit P.A. (red.): Vaccines. Wyd. 6. Elsevier, 20132. Christensen H., May M., Bowen L. i wsp.: Meningococcal carriage by age: a systematic review and meta-analysis. Lancet Infect. Dis., 2010; 10: 853–61
3. Jeppesen C.A., Snape M.D., Robinson H. i wsp.: Meningococcal carriage in adolescents in the United Kingdom to inform timing of an adolescent vaccination strategy. J. Infect., 2015; 71: 43–52
4. Van Ravenhorst M.B., Bijlsma M.W., Van Houten M.A. i wsp.: Meningococcal carriage in Dutch adolescents and young adults; a cross-sectional and longitudinal cohort study. Clin. Microbiol. Infect., 2017; 573.el-573.e7
5. Ala’Aldeen D., Oldfield N., Bidmos F. i wsp.: Carriage of Meningococci by University Students, United Kingdom. Emerg. Infect. Dis., 2011; 9: 1761–1763
6. MacLennon J., Kafatos G., Neal K. i wsp.: Social behavior an meningococcal carriage in British teenagers, Emerging Infectious Diseases. Emerg. Infect. Dis., 2006; 12: 950–957
7. Charakterystyka produktu leczniczego NeisVac C
8. Charakterystyka produktu leczniczego Meningitec
9. Charakterystyka produktu leczniczego Nimenrix
10. Charakterystyka produktu leczniczego Menveo
11. Charakterystyka produktu leczniczego Bexsero
12. Charakterystyka produktu leczniczego Trumenba
13. NIZP-PZH. Meldunki o zachorowaniach na choroby zakaźne, zakażeniach i zatruciach w Polsce. wwwold.pzh.gov.pl/oldpage/epimeld/index_p.html
14. KOROUN. Inwazyjna choroba meningokokowa w Polsce w 2016 roku. www.koroun.edu.pl/pdf/ICHM2016.pdf
15. KOROUN. Inwazyjna choroba meningokokowa w Polsce. Wybrane dane. www.koroun.edu.pl/pdf/ICHM11-04.pdf
16. KOROUN. Inwazyjna choroba meningokokowa w Polsce w 2015 roku. www.koroun.edu.pl/pdf/ICHM_2015.pdf)
17. Bonanni P.: Rationale for adolescent vaccination. 55th Annual Meeting of ESPID, 2017
18. Vetter V., Baxter R., Denizer G. i wsp.: Routinely vaccinating adolescents against meningococcus: targeting transmission & disease. Expert Rev. Vaccines, 2016; 5: 641–658
19. Thompson M., Ninis N., Perera R. i wsp.: Clinical recognition of meningococcal disease in children and adolescents. Lancet, 2006; 367: 397–493
20. Christensen H., Hickmana M., Edmundsb W.J. i wsp.: Introducing vaccination against serogroup B meningococcal disease: an economic and mathematical modelling study of potential impact. Vaccine, 2013; 31: 2638–2646
21. Christensen H., Irving T., Koch J. i wsp.: Epidemiological impact and cost-effectiveness of universal vaccination with Bexsero® to reduce meningococcal group B disease in Germany. Vaccine, 2016; 34: 3412–3419
22. Christensen H., Trotter C.L.: Modelling the cost-effectiveness of catch-up MenB (Bexsero) vaccination in England. Vaccine, 2017; 35: 208–211
23. Hepkema H., Pouwels K.B., van der Ende A. i wsp.: Meningococcal serogroup A, C, W135 and Y conjugated vaccine: a cost-effectiveness analysis in the netherlands. PLOS ONE, 2013; 5: e65036
24. Marcello Tirani M., Meregaglia M., Melegaro A.: Health and economic outcomes of introducing the new menb vaccine (bexsero) into the italian routine infant immunisation programme. PLOS ONE, 2015 (doi:10.1371/journal.pone.0123383)
25. Lecocq H., Du Chatelet I., Taha M.K. i wsp.: Epidemiological imact and cost-effectivenes of introducing vaccination against serogroup B meningococcal disease in France. Vaccine, 2016; 34: 2240–2250
26. McNanara A.L, Topaz N., Wang X. i wsp.: High risk for invasive meningococcal disease among patients receiving eculizumab (Soliris) despite receipt of meningococcal vaccine. MMWR, 2017; 66: 734–737
27. ACIP. Vaccines to prevent meningococcal disease, Resolution No. 10/16–3. www.cdc.gov