Od Redakcji: Artykuł jest zmodyfikowaną wersją opracowania, które pierwotnie ukazało się w Med. Prakt. Szczep. 4/2020, uwzględniającą szczepienia przeciwko COVID-19.
Jak cytować: Matkowska-Kocjan A., Grażyńska E.: Szczepienia ochronne u pacjentów z zaburzeniami krzepnięcia. Med. Prakt., 2021; 4: nn–nn
Skróty: ACIP – Advisory Committee on Immunization Practices, ChPL – charakterystyka produktu leczniczego, COVID-19 (coronavirus disease) – choroba spowodowana przez SARS-CoV-2, i.m. – domięśniowo, PCV-13 – skoniugowana szczepionka przeciwko pneumokokom, s.c. – podskórnie, WZW – wirusowe zapalenie wątroby
Szczepienia osób z chorobami przewlekłymi często budzą wątpliwości lekarzy praktyków. Naturalne jest to, że wielu lekarzy się zastanawia, czy pacjentów z daną jednostką chorobową można szczepić bez ograniczeń, czy jednak należy odroczyć podanie któregoś preparatu lub podać go, zachowując szczególną ostrożność. Czy należy zmienić preparat lub drogę podania szczepionki, a może ułożyć indywidualny kalendarz szczepień? Wśród wielu chorób przewlekłych szczególne miejsce w wakcynologii zajmują choroby przebiegające z zaburzeniami krzepnięcia krwi, które wiążą się z ryzykiem krwawienia po wstrzyknięciu szczepionki i jego następstw. W niniejszym artykule przedstawiono przegląd aktualnych wytycznych dotyczących wykonywania szczepień u osób z zaburzeniami krzepnięcia w odniesieniu do specyfiki realizacji szczepień w warunkach polskich.
Szczepienia ochronne u pacjentów z hemofilią
Z punktu widzenia problematyki szczepień ochronnych najistotniejszym wrodzonym zaburzeniem krzepnięcia jest hemofilia. Hemofilia A (niedobór czynnika VIII) i hemofilia B (niedobór czynnika IX) są sprzężone z płcią i występują u płci męskiej (ew. kobiet homozygotycznych pod względem zmutowanego genu), natomiast hemofilia C (niedobór czynnika XI) jest dziedziczona autosomalnie recesywnie (występuje niezwykle rzadko).1 Wiek rozpoznania hemofilii zwykle zależy od wcześniejszego występowania choroby w rodzinie. U pacjentów z dodatnim wywiadem rodzinnym w kierunku hemofilii oraz u dzieci matek będących nosicielkami zmutowanego genu hemofilię potwierdza się lub wyklucza już w wieku noworodkowym bądź niemowlęcym. Dzięki temu postępowanie profilaktyczne można rozpocząć na wczesnym etapie życia. Natomiast gdy hemofilia ma charakter sporadyczny (jest wynikiem mutacji de novo, którą się stwierdza u 20–30% pacjentów z hemofilią2), rozpoznanie ustala się w późniejszym wieku, po wystąpieniu objawów skłaniających do rozpoczęcia diagnostyki w kierunku zaburzeń krzepnięcia.
Leczenie polega na substytucji brakującego czynnika krzepnięcia. W zależności od stopnia niedoboru czynnika (skorelowanego z ciężkością przebiegu choroby) oraz indywidualnych uwarunkowań (aktywność ruchowa, historia krwawień itd.) koncentraty czynników krzepnięcia stosuje się profilaktycznie i/lub „na żądanie”, w przypadku planowania aktywności związanej ze zwiększonym ryzykiem urazu oraz po urazie. Po rozpoznaniu hemofilii można również podjąć inne działania profilaktyczne w celu zmniejszenia ryzyka krwawień i ich powikłań. Należy do nich odpowiednie wykonywanie szczepień ochronnych.
Czy pacjenci z hemofilią mogą być szczepieni bez ograniczeń?
Hemofilia nie stanowi przeciwwskazania do szczepień ochronnych, dlatego pacjenci z tym rozpoznaniem powinni realizować szczepienia obowiązkowe i zalecane zgodnie z ogólnym kalendarzem szczepień. Nie należy opóźniać wykonywania szczepień ochronnych, nawet w przypadku ciężkich postaci hemofilii. Należy pamiętać, że choroba ta ma charakter przewlekły, co się wiąże z koniecznością wizyt w placówkach medycznych i – co za tym idzie – z narażeniem na kontakt z chorobami zakaźnymi. Rozpoznanie hemofilii należy zatem traktować wręcz jako wskazanie do rozszerzenia kalendarza szczepień ochronnych o wszelkie uzasadnione szczepienia zalecane.3 Podkreśla się wskazania do rutynowego stosowania szczepień przeciwko grypie, pneumokokom, a także wirusowemu zapaleniu wątroby (WZW) typu A i typu B u wszystkich osób z hemofilią.4
Jaką drogą należy podawać szczepionki pacjentom z hemofilią?
U chorych na hemofilię domięśniowe (i.m.) wstrzyknięcie szczepionki wiąże się z ryzykiem krwawienia domięśniowego i jego długofalowych następstw. Powszechnie wiadomo, że u pacjentów z tej grupy o wiele bezpieczniejsze są szczepionki podawane drogą podskórną (s.c.). Autorzy ostatnio opublikowanych wytycznych włoskich uznali, że niezależnie od nasilenia hemofilii preferowana jest droga s.c. (a nie i.m.).3 Problemem jest jednak brak rejestracji wielu szczepionek do wstrzyknięć s.c. Co więcej, producenci niektórych z nich wręcz podkreślają, że nie należy ich podawać tą drogą (p. tab.; to zastrzeżenie dotyczy także wszystkich zarejestrowanych aktualnie szczepionek przeciwko COVID-19).
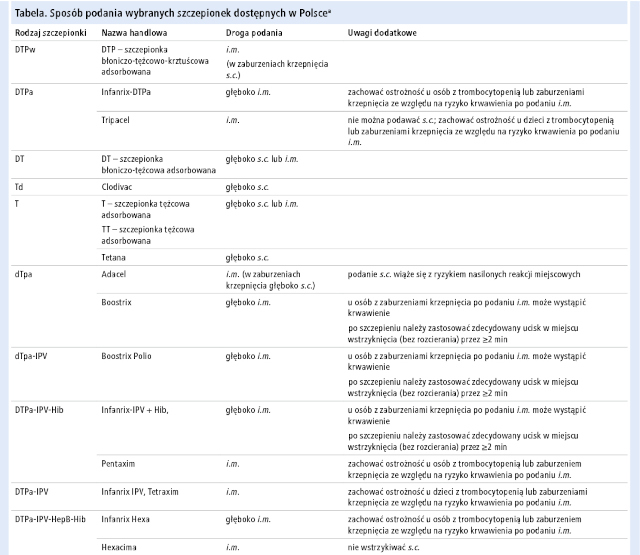
Przegląd wytycznych dotyczących szczepień ochronnych u pacjentów z hemofilią pozostawia pewien niedosyt, ponieważ jak dotąd nie sformułowano mocnych zaleceń dotyczących wyboru optymalnej drogi iniekcji szczepionek w odniesieniu do ich rejestracji. Wynika to z braku wystarczających danych potwierdzających odpowiednią immunogenność preparatów zarejestrowanych do podania wyłącznie i.m. po zmianie drogi podania na s.c. Takie badania opublikowano tylko dla niektórych szczepionek (skoniugowanej 23-walentnej szczepionki przeciwko pneumokokom [PPSV-23], WZW typu A i B, inaktywowanej szczepionki przeciwko polio [IPV], komponentu błoniczego i tężcowego w szczepionce przeciwko błonicy, tężcowi i krztuścowi z komponentem bezkomórkowym [DTaP]).5-9 Niektóre powszechnie stosowane preparaty, zwłaszcza wysoce skojarzone, nie były nigdy badane pod tym kątem i są zarejestrowane wyłącznie do podania i.m. Ale – odwracając sytuację – nie ma również obecnie dowodów na to, że droga s.c. jest mniej immunogenna od i.m.3
W tabeli wymieniono drogi podania szczepionek stosowanych w Polsce, zalecane w charakterystykach produktu leczniczego (ChPL). Z analizy tych danych wynika, że u dzieci z hemofilią przez pierwsze 2 lata życia można stosować wyłącznie szczepionki podawane s.c., dzięki wykorzystaniu preparatów nieskojarzonych lub nisko skojarzonych: szczepionki przeciwko błonicy, tężcowi i krztuścowi z komponentem całokomórkowym (DTPw), przeciwko Haemophilus influenzae typu b (Hib), IPV, przeciwko WZW typu B, 13-walentnej skoniugowanej szczepionki przeciwko pneumokokom (PCV-13) oraz przeciwko odrze, śwince i różyczce (MMR). Pojawiają się jednak wątpliwości, co zrobić, gdy dziecko ma przeciwwskazania do podania szczepionki z całokomórkowym komponentem krztuścowym i wskazane jest zastosowanie preparatu bezkomórkowego, żaden z nich bowiem nie został zarejestrowany do podania s.c. Zasadnicze jest tymczasem pytanie, czy zamiast wielu wstrzyknięć s.c., które również mogą się wiązać z pewnym ryzykiem krwawienia, nie lepiej wykonać jedną iniekcję i.m. preparatu wysoce skojarzonego po odpowiednim przygotowaniu i zabezpieczeniu pacjenta. A może warto pozarejestracyjnie (off-label) podać s.c. preparat wysoce skojarzony?
Intuicyjnie stosowanie preparatów wysoce skojarzonych u dzieci z hemofilią wydaje się bardziej racjonalne niż wielokrotne wykonywanie wkłuć w celu podania szczepionek nieskojarzonych. Tym bardziej, że takie rozwiązanie powszechnie stosuje się na świecie – w większości krajów wysoko rozwiniętych wszystkie szczepienia u niemowląt i małych dzieci są z definicji realizowane preparatami wysoce skojarzonymi typu „5 w 1” lub „6 w 1” (a preparaty nieskojarzone są niedostępne lub trudno dostępne). Polska jest wręcz wyjątkiem (np. wśród krajów Unii Europejskiej) w kwestii prowadzenia szczepień obowiązkowych przede wszystkim preparatami nieskojarzonymi. W związku z tym autorzy wytycznych zachodnich w ogóle nie poruszają problemu wyboru preparatu (nieskojarzony vs wysoko skojarzony). Należy podkreślić, że polski program szczepień ochronnych nie przewiduje refundacji szczepionek wysoce skojarzonych dla pacjentów z rozpoznaniem hemofilii, ale dzieciom z chorobami hematologicznymi przysługuje refundacja na szczepionkę PCV-13, którą w tej grupie należy podawać w schemacie 3+1, tak jak w grupach ryzyka. Zgodnie z zapisami w ChPL szczepionkę tę można podawać s.c., co zapewnia dodatkowy komfort personelowi wykonującemu szczepienie.10
Amerykański Advisory Committee on Immunization Practices (ACIP) stoi na stanowisku, że pacjentom z zaburzeniem krzepnięcia można podać szczepionkę i.m., jeśli tego wymagają, o ile lekarz prowadzący uzna takie postępowanie za wystarczająco bezpieczne.11
Na podstawie przeglądu zaleceń oraz po uwzględnieniu faktu, że w codziennej praktyce spotykamy się z sytuacjami, których nie uwzględniono w wytycznych, w ramce 1 przedstawiamy proponowane zasady wyboru drogi podania szczepionki u pacjentów z zaburzeniami krzepnięcia (odnoszą się one także do szczepienia pacjentów z tej grupy przeciwko COVID-19).
Ramka 1. Zasady wyboru drogi podania szczepionki u pacjentów z zaburzeniami krzepnięcia
- Jeśli możliwe są 2 drogi podania (s.c. lub i.m.), u pacjenta z hemofilią zawsze należy wybierać drogę s.c.
- Jeśli szczepionka optymalna dla pacjenta jest zarejestrowana wyłącznie do podania i.m. i nie istnieją dodatkowe przesłanki przemawiające przeciwko takiemu postępowaniu u danego pacjenta, szczepionkę należy podać i.m., stosując odpowiednią technikę szczepienia (p. ramka 2 i podrozdz. „Technika wykonania szczepień…”).
- Jeśli szczepionka optymalna dla pacjenta jest zarejestrowana wyłącznie do podania i.m., ale istnieją dodatkowe przesłanki przemawiające przeciwko takiemu postępowaniu (np. u pacjenta wystąpiły już krwawienia domięśniowe mimo zastosowania odpowiedniej profilaktyki, po wcześniejszym szczepieniu i.m. obserwowano istotne powikłania miejscowe, według hematologa prowadzącego ryzyko związane z domięśniowym podaniem szczepienia przewyższa w danej sytuacji potencjalne korzyści itp.), należy rozważyć pozarejestracyjne podanie preparatu s.c. (w przypadku dziecka po przedyskutowaniu problemu z jego rodzicami/opiekunami i uzyskaniu ich zgody). Aktualnie nie dotyczy to szczepień przeciwko COVID-19.
Ramka 2. Technika wykonania wstrzyknięcia domięśniowego u pacjentów z zaburzeniami krzepnięcia
- Rozważyć podanie czynnika krzepnięcia w ciągu 24 godz. przed szczepieniem (dotyczy tylko pacjentów z hemofilią).
- 5 min przed wykonaniem wstrzyknięcia można przyłożyć okład z lodu w miejscu wkłucia.
- Użyć najcieńszej igły (zazwyczaj 25–27 G).
- Po wykonaniu wstrzyknięcia zastosować ucisk w miejscu wkłucia przez ≥2 min (bez pocierania i rozmasowywania).
- Poinformować pacjenta i/lub jego opiekunów o możliwości wystąpienia powikłań (krwiak, ocieplenie, zaczerwienienie) i konieczności skontaktowania się z lekarzem prowadzącym w takim przypadku.
- W razie wystąpienia bólu lub gorączki lekiem pierwszego wyboru powinien być paracetamol (należy unikać stosowania niesteroidowych leków przeciwzapalnych [kwas acetylosalicylowy, ibuprofen, naproksen i in.] ze względu na ryzyko krwawienia).
Technika wykonania szczepień domięśniowych u pacjentów z hemofilią i praktyczne zalecenia
Eksperci World Federation of Hemophilia w wytycznych z 2012 roku12 dotyczących opieki nad pacjentami z hemofilią zalecają, by osoby z zaburzeniami krzepnięcia krwi szczepić, ale szczepionkę najlepiej podawać s.c., a nie i.m., chyba że zastosowano osłonowo wlew koncentratu czynnika krzepnięcia. Jeśli konieczna jest iniekcja i.m., zaleca się, aby:
- najlepiej wykonać ją krótko po podaniu czynnika krzepnięcia
- na 5 minut przed wykonaniem iniekcji przyłożyć lód w miejscu wkłucia
- używać najcieńszych dostępnych igieł (zazwyczaj 25–27 G)
- po wykonaniu wstrzyknięcia zastosować ucisk przez 5 minut.
Opublikowane rok później zalecenia Medical and Scientific Advisory Council (MASAC) of the National Hemophilia Foundation13 precyzują czas wykonania szczepienia w odniesieniu do podania czynnika krzepnięcia. Zgodnie z nimi szczepienie i.m. należy wykonać w ciągu doby po podaniu czynnika krzepnięcia. Skrócono również proponowany czas ucisku po wykonaniu iniekcji do ≥2 minut i podkreślono, że miejsca szczepienia nie powinno się pocierać. Autorzy zaleceń zwrócili również uwagę na:
- edukację pacjenta/jego opiekunów po kątem wystąpienia możliwych powikłań (krwiak, ocieplenie, zaczerwienienie) oraz konieczność skontaktowania się z lekarzem prowadzącym w przypadku ich wystąpienia
- wybór odpowiedniego leku w razie wystąpienia bólu lub gorączki; zaleca się stosowanie paracetamolu i unikanie – ze względu na potencjalne ryzyko krwawienia – niesteroidowych leków przeciwzapalnych (takich jak kwas acetylosalicylowy, ibuprofen, naproksen i in.).
W 3. edycji wytycznych World Federation of Hemophilia z 2020 roku zalecenia dotyczące szczepień nieznacznie zmieniono, wydłużając ucisk po wstrzyknięciu i.m. do 10 min.4
Eksperci włoscy, którzy w 2019 roku dokonali przeglądu piśmiennictwa dotyczącego szczepień u pacjentów z hemofilią, opublikowali wytyczne będące konsensusem ustalonym na podstawie głosowania członków grupy. Autorzy poparli zalecenia dotyczące rutynowego stosowania okładów z lodu przed wykonaniem szczepienia i po nim, uciskania miejsca wstrzyknięcia oraz używania igieł o jak najmniejszej średnicy.3 Bardzo interesujące jest jednak to, że nie ustalono stanowiska w kwestii zasadności podawania koncentratu czynnika krzepnięcia przed wykonaniem szczepienia. Analiza danych wykazała, że nie ma danych naukowych uzasadniających takie postępowanie, a zalecenie to ma charakter uznaniowy i racjonalny.14 Wynika ono z trudności w realizacji badań z randomizacją, które mogłyby jednoznacznie rozstrzygnąć to zagadnienie (hemofilia występuje bardzo rzadko i trudno zebrać wystarczającą grupę do zbadania problemu, który ma już swoje praktyczne rozwiązanie).
Grupa Robocza do spraw Hemostazy Polskiego Towarzystwa Hematologów i Transfuzjologów w stanowisku z dnia 7 stycznia 2021 roku podkreśliła, że postępowanie przygotowawcze przed szczepieniem zależy od ciężkości skazy krwotoczne. Pacjenci z wrodzonymi skazami krwotocznymi o ciężkim przebiegu mogą wymagać podania koncentratu czynnika krzepnięcia lub desmopresyny przed szczepieniem. Koncentrat czynnika krzepnięcia należy podać w dniu szczepienia. Procedurę można wykonać w domu pacjenta (pacjent lub opiekun zaświadcza pisemnie o przyjęciu koncentratu czynnika krzepnięcia), w Ośrodku Leczenia Hemofilii lub gabinecie zabiegowym podstawowej opieki zdrowotnej (lekarz lub pielęgniarka potwierdza przetoczenie koncentratu czynnika krzepnięcia). Autorzy tego stanowiska proponują, aby u chorych na hemofilię A otrzymujących w profilaktyce emicizumab szczepienie i.m. wykonać po upływie 48 godzin od otrzymania ostatniej dawki leku.15
Zalecenia dotyczące wykonywania szczepień w innych chorobach przebiegających z zaburzeniami krzepnięcia nie różnią się istotnie od tych, które dotyczą hemofilii (z wyjątkiem profilaktycznego stosowania koncentratu czynnika krzepnięcia, co jest swoiste dla tej choroby). Jak już wspomniano, ACIP stoi na stanowisku, że pacjentom z zaburzeniem krzepnięcia można podać szczepionkę i.m., jeśli tego wymaga, o ile lekarz prowadzący uzna takie postępowanie u danego pacjenta za wystarczająco bezpieczne11 (dotyczy to wszelkich zaburzeń krzepnięcia). Podobnie jak w hemofilii należy użyć igły o najmniejszej średnicy, po zakończeniu wstrzyknięcia zastosować ucisk oraz poinformować rodziców/opiekunów o możliwości krwawienia. Niektórzy autorzy zalecają, aby u pacjentów z chorobą von Willebranda szczepionki podawać w mięsień udowy (ma znacznie większą masę niż mięsień naramienny), wykonując podczas jednej wizyty maksymalnie jedno wstrzyknięcie w danej okolicy anatomicznej.16
Szczepienia u osób przyjmujących leki przeciwkrzepliwe
Przed podjęciem decyzji o podaniu szczepionki należy ustalić przewidywany czas trwania terapii. Jeśli podawanie leków przeciwkrzepliwych (np. warfaryny lub heparyny drobnocząsteczkowej) zaplanowano na określony i stosunkowo krótki czas (np. leczenie ostrej choroby), należy opóźnić szczepienie do czasu jego zakończenia. Powodem opóźnienia szczepienia najczęściej jest sama choroba podstawowa (ostra lub zaostrzenie choroby przewlekłej) stanowiąca czasowe przeciwwskazanie.
U pacjentów na stałe przyjmujących leki przeciwkrzepliwe wymagających podania szczepionki oraz u osób potrzebujących pilnego szczepienia (np. poekspozycyjnego) w trakcie czasowego przyjmowania leku należy uwzględnić wyniki badań układu krzepnięcia w celu oceny bezpieczeństwa wstrzyknięcia. Należy zrezygnować ze szczepienia i.m., jeśli INR wynosi >3,0 w ostatnim okresowym rutynowym pomiarze (dotyczy pacjentów leczonych warfaryną lub innym antagonistą witaminy K) lub aktywność anty-Xa mierzona po 4 godzinach od podania ostatniej dawki heparyny drobnocząsteczkowej wynosi >0,5 j./ml. Profilaktyczne stosowanie heparyny drobnocząsteczkowej u chorych unieruchomionych nie wymaga oceny aktywności anty-Xa i nie jest przeciwwskazaniem do szczepienia i.m., w tym przeciwko COVID-19.17,18
Badania naukowe nie potwierdzają hipotezy, że szczepienia ochronne wpływają na parametry krzepnięcia u pacjentów leczonych przewlekle warfaryną.19,20
W stanowisku dotyczącym szczepienia przeciwko COVID-19 u pacjentów w trakcie leczenia przeciwzakrzepowego oraz osób z zaburzeniami krzepnięcia British Society for Haematology zaleciło, aby postępować według podanych wyżej zasad kwalifikacji i stosować zmodyfikowaną technikę szczepienia i.m., a ponadto stwierdziło, że:
- pacjentów przyjmujących profilaktycznie lek przeciwpłytkowy (kwas acetylosalicylowy lub klopidogrel) w monoterapii można bez obaw szczepić i.m.
- u pacjentów, którzy są w trakcie leczenia podtrzymującego doustnymi bezpośrednimi inhibitorami czynnika Xa (np. apiksabanem, rywaroksabanem, edoksabanem, dabigatranem), heparyną drobnocząsteczkową lub fondaparynuksem, w dniu szczepienia i.m. można na wszelki wypadek podać lek dopiero po szczepieniu.20
Piśmiennictwo:
1. Gajewski K.: Hemofilia. www.mp.pl/170 465 (dostęp: 1.12.2020)2. Żbikowski P., Matysiak M., Łaguna P., C´wikła J.: Hemophilic arthropathy – pathogenesis, clinical symptoms and diagnostic possibilities. J. Trans. Med., 2010; 3: 19–26
3. Santagostino E., Riva A., Cesaro S. i wsp.; the HEVA Study Group: Consensus statements on vaccination in patients with haemophilia – results from the Italian haemophilia and vaccinations (HEVA) project. Haemophilia, 2019; 25: 656–667
4. Srivastava A., Santagostino E., Dougall A. i wsp.: WFH Guidelines for the management of hemophilia panelists and co-authors. WFH guidelines for the management of hemophilia. 3rd edition. Haemophilia, 2020; 26: 1–158
5. Ragni M.V., Lusher J.M., Koerper M.A. i wsp.: Safety and immunogenicity of subcutaneous hepatitis A vaccine in children with haemophilia. Haemophilia, 2000; 6: 98–103
6. Gazengel C., Courouce A.M., Torchet M.F. i wsp.: Use of HBV vaccine in hemophiliacs. Scand. J. Haematol., 1984; 40: 323–328
7. Janco R.L.: Immunogenicity of subcutaneous hepatitis B vaccine in hemophiliacs. J. Pediatr., 1985; 107 (2): 316
8. Zanetti A.R., Mannucci P.M., Tanzi E. i wsp.: Hepatitis B vaccination of 113 hemophiliacs: lower antibody response in anti-LAV/HTLV-III-positive patients. Am. J. Hematol., 1986; 23: 339–345
9. Schaefer B.A., Gruppo R.A., Mullins E.S. i wsp.: A pilot study and review of the literature. Haemophilia, 2017; 23: 904–909
10. Komunikat Głównego Inspektora Sanitarnego z dnia 26 października 2020 r. w sprawie Programu Szczepień Ochronnych na rok 2021. Dz. Urz. Min. Zdr., poz. 90
11. General best practice guidelines for immunization: best practices guidance of the advisory committee on immunization practices (ACIP). www.cdc.gov/vaccines/hcp/acip-recs/general-recs/special-situations.html (dostęp: 1.12.2020)
12. Srivastava A., Brewer A.K., Mauser-Bunschoten E.P. i wsp.: Guidelines for the management of hemophilia. Haemophilia, 2013; 19(1): e1-47. doi: 10.1111/j.1365–2516.2012.02 909.x
13. MASAC: Recommendations on Administration of Vaccines to Individuals with Bleeding Disorders. www.hemophilia.org/healthcare-professionals/guidelines-on-care/masac-documents/masac-document-221-recommendations-on-administration-of-vaccines-to-individuals-with-bleeding-disorders (dostęp: 1.12.2020)
14. Platokouki H., Fischer K., Gouw S.C. i wsp.: Vaccinations are not associated with inhibitor development in boys with severe haemophilia A. Haemophilia, 2018; 24: 283–290 15. Stanowisko z dnia 07.01.2021 r. w sprawie szczepień przeciw wirusowi SARS-CoV-2 u chorych na hemofilię i pokrewne skazy krwotoczne Grupy Roboczej do spraw Hemostazy Polskiego Towarzystwa Hematologów i Transfuzjologów. https://www.mp.pl/szczepienia/artykuly/wytyczne/257328 (dostęp: 23.03.2021)
16. Indiana Hemophilia & Thrombosis Center: Additional VWD treatment therapies. www.ihtc.org/vwd-additional-therapies (dostęp: 1.12.2020)
17. Australian immunisation handbook: Vaccination for people with bleeding disorders. https://immunisationhandbook.health.gov.au/vaccination-for-special-risk-groups/vaccination-for-people-with-bleeding-disorders (dostęp: 1.12.2020)
18. British Society for Haematology: COVID-19 vaccines in patients with haematological disorders. https://b-s-h.org.uk/media/19236/haematology-covid-19-v11-vaccination-statement-13121-clean.pdf (dostęp: 23.03.2021)
19. Jackson M.L., Nelson J.C., Chen R.T. i wsp.: Vaccine Safety Datalink investigators. Vaccines and changes in coagulation parameters in adults on chronic warfarin therapy: a cohort study. Pharmacoepidemiol. Drug Saf., 2007; 16: 790–796
20. MacCallum P., Madhani M., Mt-Isa S., Ashby D.: Lack of effect of influenza immunisation on anticoagulant control in patients on long-term warfarin. Pharmacoepidemiol. Drug Saf., 2007; 16: 786–789