SPECJALNIE dla „Medycyny Praktycznej – Szczepienia”

|
dr hab. n. med. Maria Korzeniewska-Koseła profesor Instytutu Gruźlicy i Chorób Płuc, Zakład Epidemiologii i Organizacji Walki z Gruźlicą, Instytut Gruźlicy i Chorób Płuc w Warszawie, ORCID: 0000-0001-7693-9012 |

|
prof. dr hab. n. med. Jacek Wysocki specjalista chorób zakaźnych i pediatrii. Kierownik Katedry i Zakładu Profilaktyki Zdrowotnej na Wydziale Nauk o Zdrowiu Uniwersytetu Medycznego im. Karola Marcinkowskiego w Poznaniu |
Skróty: EOG – Europejski Obszar Gospodarczy, ZOMR – zapalenie opon mózgowo-rdzeniowych, HIV – ludzki wirus niedoboru odporności, MDR-TB – gruźlica wielolekooporna, NOP – niepożądany odczyn poszczepienny, PNG – prątki niegruźlicze, PT – próba tuberkulinowa, UE – Unia Europejska, WHO – Światowa Organizacja Zdrowia
Punkt widzenia pulmonologa ftyzjatry
Światowa Organizacja Zdrowia (WHO) szacuje, że w 2016 roku na gruźlicę zachorowało 10,4 mln osób, w tym milion dzieci do lat 14. Liczba zachorowań na gruźlicę wielolekooporną, wywołaną przez prątki oporne na izoniazyd i ryfampicynę (MDR-TB), wynosi natomiast 490 000. Gruźlica jest jedną z częstszych przyczyn zgonów na świecie.
Epidemiologia gruźlicy
W 2017 roku w Polsce odnotowano 5787 zachorowań na gruźlicę (o 657 mniej niż w 2016 r.), a zapadalność wyniosła 15,1 na 100 000 osób. Współczynnik zapadalności na gruźlicę był tym większy, im starsza była grupa wiekowa, ale tylko do wieku 45–64 lat, i wynosił od 1,2 na 100 000 dzieci do 14. roku życia do 25,6 na 100 000 osób w wieku 45–64 lat. Zapadalność u osób w wieku ≥65 lat wynosiła 22,6 na 100 000. Zgłoszono 68 zachorowań na gruźlicę wśród dzieci do 14. roku życia, które stanowiły 1,2% ogółu przypadków, i 69 wśród młodzieży w wieku 15–19 lat (zapadalność 3,6/100 000). Zapadalność na gruźlicę płuc potwierdzoną bakteriologicznie wynosiła 10,6 na 100 000. Chorzy na gruźlicę płuc potwierdzoną w badaniu bakteriologicznym stanowili 73,4% ogółu chorych na gruźlicę płuc, a chorzy na gruźlicę płuc, u których prątki stwierdzono także w bakterioskopii – 44,7% (2472 chorych, współczynnik 6,4/100 000). MDR-TB rozpoznano u 44 chorych, w tym u 12 cudzoziemców. Przypadki MDR-TB stanowiły 1,2% zachorowań ze znanymi wynikami lekowrażliwości prątków. W 2016 roku gruźlica była przyczyną zgonu 543 osób. Współczynnik umieralności był taki sam jak w ciągu 3 wcześniejszych lat (1,4/100 000).
W 2016 roku w 30 krajach Unii Europejskiej (UE) i Europejskiego Obszaru Gospodarczego (EOG) na gruźlicę zachorowały 58 994 osoby. 45% tej liczby stanowili chorzy z Polski, Rumunii i Wielkiej Brytanii (z samej Rumunii 23,1%). Zapadalność na gruźlicę w UE/EOG wynosiła średnio 11,4 przypadków na 100 000 ludności (szacunkowa zapadalność na świecie – 140/100 000). W 20 krajach UE/EOG zapadalność na gruźlicę wynosiła <10 na 100 000 (najmniejsza w Islandii – 1,8/100 000; największa w Rumunii – 68,9/100 000). Dzieci <15 lat stanowiły 4,3% wszystkich chorych, których wiek był znany. Cudzoziemcy stanowili największy odsetek wśród chorych na gruźlicę na Malcie i Cyprze (>90%), w Szwecji (89,8%) i Norwegii (88,3%), a najmniejszy w Bułgarii, Chorwacji i na Litwie (<1%). W krajach UE/EOG chorzy na MDR-TB stanowili 3,7% wszystkich chorych z dostępnymi wynikami lekowrażliwości prątków. Najwięcej przypadków MDR-TB odnotowano na Łotwie i Litwie oraz w Estonii (10,4–20,3%).
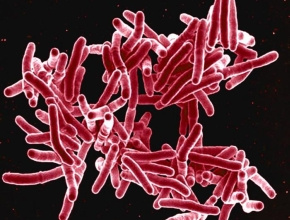
Gruźlicę u ludzi wywołują prątki Mycobacterium tuberculosis, które za pośrednictwem krwi i chłonki mogą się szerzyć z miejsca pierwotnej zmiany w płucach do innych części ciała. Objawy gruźlicy różnią się istotnie w zależności od wieku chorego, jego statusu immunologicznego oraz lokalizacji choroby i jej ciężkości. Prątki gruźlicy mogą też zostać zatrzymane w makrofagach i pozostawać w tkankach gospodarza w stadium utajonym. W populacji ogólnej w aktywną postać choroby przechodzi tylko 5–15% utajonych zakażeń. Reaktywacja następuje w ciągu kilku miesięcy lub nawet wiele lat po zakażeniu. Utajone zakażenie prątkiem gruźlicy jest stanem przetrwałej odpowiedzi immunologicznej na stymulację antygenami M. tuberculosis, bez jakichkolwiek zjawisk wskazujących na aktywną chorobę. Można je wykryć za pomocą próby tuberkulinowej (PT) lub testów IGRA opartych na pomiarze wydzielania interferonu gamma (IFN-γ). Wcześniejsze szczepienie BCG i zakażenie prątkami niegruźliczymi (PNG) zmniejsza swoistość PT. Większą swoistością charakteryzują się natomiast testy IGRA, które nie wykazują reakcji krzyżowych z prątkami BCG.
W przypadku zakażenia większe prawdopodobieństwo zachorowania na gruźlicę dotyczy dzieci do 5. roku życia niż pozostałych osób. Do grupy największego ryzyka rozwoju choroby należą dzieci do 1. roku życia, u których wynosi ono 40–60%. Gruźlica u dzieci występuje zwykle w ciągu roku od zakażenia. Liczne zachorowania u dzieci wskazują, że w danej społeczności stale dochodzi do transmisji zakażenia prątkiem gruźlicy.
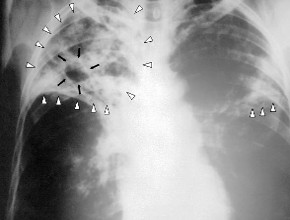
U małych dzieci rozsiew krwiopochodny prowadzi do ciężkiej postaci gruźlicy pierwotnej, w tym do prosówki gruźliczej i gruźliczego zapalenia opon mózgowo-rdzeniowych (ZOMR). U niemowląt gruźlica płuc może się rozwinąć szybko po zakażeniu i przyjąć postać ciężkiego zapalenia płuc. Z piśmiennictwa wynika, że dzieci do 5 lat mogą ulec zakażeniu nawet podczas krótkiego, okazjonalnego kontaktu z wysoce zakaźnym chorym na jamistą postać gruźlicy płuc.
Kolejną grupę zwiększonego ryzyka zachorowania na gruźlicę stanowią nastolatki. Młodociani chorują na szybko postępującą gruźlicę płuc z jamami i dodatnim wynikiem bakterioskopii plwociny.
Historia szczepień BCG
Szczepienia profilaktyczne są skutecznym sposobem zapobiegania chorobom zakaźnym i doprowadziły do eliminacji niektórych takich chorób. Gruźlica, która może pozostawać w stadium utajenia, jest trudniejsza do zwalczenia. Szczepionka BCG, choć skuteczna w niektórych populacjach, nie doprowadziła do eliminacji gruźlicy.
Szczepionka BCG zawiera żywe, atenuowane szczepy Mycobacterium bovis, które w pierwotnej postaci wywoływały gruźlicę u bydła. Prątki użyte do wytworzenia szczepionki pobrano w 1908 roku od chorej na gruźlicę krowy, które następnie francuscy naukowcy z Instytutu Pasteura w Lille – Calmette i Guérin – poddali atenuacji. Szczep przesiewano co 3 tygodnie przez około 13 lat. W tym czasie doszło do wielu zmian w genomie prątków bydlęcych i do zmniejszenia ich wirulencji. Powstały mutant otrzymał nazwę prątka BCG. Szczepionkę po raz pierwszy podano doustnie w 1921 roku niemowlęciu, w którego rodzinie wystąpiły zachorowania na gruźlicę, uzyskując dobry skutek. Do 1924 roku szczep wyjściowy utrzymywano w Instytucie Pasteura w Paryżu, a następnie rozprowadzono do wielu laboratoriów na świecie. Po latach szczepy z różnych laboratoriów przestały być identyczne, chociaż wprowadzono procedury ograniczające mutacje genetyczne. Nawet szczep z laboratorium paryskiego nie jest już taki sam jak ten wytworzony przez Calmette’a i Guérina. Różne własności immunogenne szczepionek wyprodukowanych z prątków BCG wyhodowanych w poszczególnych krajach mają charakter stały. Rozróżniamy podszczep francuski, duński, brazylijski, rosyjski, a także podszczep Kopenhaga, Praga, Rio de Janeiro, Chicago, Goeteborg i Madras. Nie ma danych wskazujących, że różnice genetyczne między szczepami mają wpływ na skuteczność BCG. Nie ma też zaleceń, aby w szczepionce stosować określony szczep.
W Polsce pierwsze szczepienia przeprowadzono w 1926 roku (wg innych danych dostępne były już w 1924 r.). Produkcję szczepionki z podszczepu brazylijskiego Moreau i masowe szczepienia rozpoczęto natomiast w 1955 roku.
Bezpieczeństwo szczepionki BCG
Od 1921 roku szczepieniom BCG poddano ponad 4 miliardy osób. Wiadomo, że ryzyko powikłań jest małe oraz że szczepionka BCG jest bezpieczna. Niepożądane odczyny poszczepienne (NOP) występują względnie rzadko i w zdecydowanej większości przypadków nie stanowią zagrożenia dla zdrowia i życia szczepionych. Reakcje niepożądane częściej wywołują szczepy duńskie i Pasteur.
Obecnie szczepionkę BCG podaje się we wstrzyknięciu śródskórnym. U około 95% zaszczepionych osób w miejscu wstrzyknięcia rozwija się odczyn w postaci krosty, która może ulec owrzodzeniu. Zmiana znika po 2–5 miesiącach, pozostawiając powierzchowną bliznę. Taki przebieg gojenia uznaje się za prawidłowy. U 1–2% zaszczepionych rozwija się zapalenie okolicznych węzłów chłonnych (czasami w postaci ropnej), które ustępuje samoistnie po kilku miesiącach.
Do ciężkich miejscowych NOP zalicza się powstanie ropnia w miejscu wstrzyknięcia, rozległe owrzodzenie spowodowane zwykle przypadkowym podaniem szczepionki podskórnie lub ropne zapalenie węzłów chłonnych. Ciężkie NOP występują rzadko. W 1,56–4,29 przypadków na milion podanych dawek rozwija się rozsiana choroba wywołana przez BCG. Powikłanie to dotyczy głównie dzieci z pierwotnymi niedoborami odporności komórkowej oraz zakażonych ludzkim wirusem niedoboru odporności (HIV). Istnieją obawy, że szczepionka BCG podana niemowlętom zakażonym HIV przyspiesza progresję choroby.
WHO zaleca, aby na terenach o dużym rozpowszechnieniu zakażenia HIV wstrzymać się z podaniem szczepionki do czasu wyjaśnienia, czy niemowlę jest zakażone HIV, co można ustalić w 6. tygodniu życia. W czasie oczekiwania na wynik badania w kierunku HIV dziecko jest narażone na zakażenie prątkiem gruźlicy i zachorowanie na gruźlicę.
Skuteczność szczepionki BCG
Wyniki badań wskazują, że szczepionka BCG chroni przed zachorowaniami na gruźlicę rozsianą i gruźlicze ZOMR. Największą skuteczność obserwowano u noworodków i dzieci z ujemnym wynikiem PT (ryzyko względne [RR] odpowiednio: 0,10 [95% CI: 0,01–0,77] oraz 0,08 [95% CI: 0,03–0,25]).
Udowodniono również, że BCG zmniejsza ryzyko zachorowania na gruźlicę płuc, ale stopień ochrony zależy od populacji. W badaniu przeprowadzonym w Wielkiej Brytanii w latach 50. XX wieku ochrona u nastolatków wynosiła 80%. W podobnym badaniu przeprowadzonym w Stanach Zjednoczonych nie potwierdzono jednak efektywności szczepienia, co sprawiło, że władze amerykańskie zdecydowały nie wprowadziać powszechnych szczepień BCG. Natomiast w innym badaniu obejmującym Indian północnoamerykańskich potwierdzono długotrwałą skuteczność szczepionki. Dla kontrastu, w badaniu przeprowadzonym w latach 50. XX wieku, obejmującym dużą grupę osób z południowych Indii, nie potwierdzono skuteczności szczepionki w ochronie przed płucną postacią gruźlicy.
W metaanalizie 18 badań z randomizacją skuteczność BCG w zapobieganiu zachorowaniom na gruźlicę płuc u osób zaszczepionych w okresie niemowlęcym wynosiła 59% (RR: 0,41 [95% CI: 0,29–0,58]). W badaniach, w których szczepionkę BCG podawano w dzieciom z ujemnym wynikiem PT, ochrona przed gruźlicą płuc wynosiła 74% (RR: 0,26 [95% CI: 0,18–0,37]). Natomiast w badaniach, w których nie sprawdzano wyniku PT przed szczepieniem, przeciętna ochrona przed zachorowaniem na gruźlicę płuc była zmniejszona, ponieważ mogły w nich uczestniczyć dzieci już zakażone prątkiem gruźlicy lub eksponowane na PNG.
Efektywność szczepień BCG jest mniejsza w krajach, w których panuje gorący klimat, i położonych bliżej równika, co może wynikać z większej ekspozycji na PNG w klimacie tropikalnym. Ekspozycja na prątki środowiskowe wywołuje wrażliwość tuberkulinową i zapewne jakiś poziom odporności, która może chronić przed gruźlicą. Szczepionka BCG nie jest zdolna zwiększyć poziomu odporności ponad ten, jaki uzyskuje się w wyniku zakażenia PNG (działanie maskujące). Inną możliwością jest blokowanie działania szczepionki przez ekspozycję na PNG. BCG jest „żywą” szczepionką i zawarte w niej prątki muszą się namnażać, aby szczepienie działało ochronnie. Zakażenie PNG, wywołując jakiegoś stopnia odporność, może hamować wzrost BCG i redukować efekt szczepionki (działanie blokujące). Być może oba mechanizmy – maskujący i blokujący – występują jednocześnie, wpływając na efekt szczepienia, zwłaszcza na obszarach o dużym rozpowszechnieniu PNG.
Trwałość ochrony
Ochronne działanie szczepionki BCG może się utrzymywać przez wiele lat. Ostatnio autorzy brytyjscy wykazali, że efekt ochronny szczepionki przeciwko wszystkim postaciom gruźlicy, podanej dzieciom w wieku szkolnym, utrzymywał się przez 20 lat. W populacji zamieszkującej północne regiony Stanów Zjednoczonych, którą zaszczepiono w wieku niemowlęcym, działanie ochronne BCG utrzymywało się przez 60 lat.
W badaniu obejmującym osoby urodzone w Norwegii, uczestniczące w powszechnym programie szczepień BCG realizowanym w latach 1962–1975, które miały wówczas 12–50 lat, wykazano, że efekt zapobiegający gruźlicy utrzymywał się przez 30–40 lat (obserwację zakończono w 2011 r.).
Skuteczność w zapobieganiu zakażeniom prątkiem gruźlicy
Dostępność testów IGRA, które umożliwiają odróżnienie zakażenia prątkiem gruźlicy od odpowiedzi wywołanej BCG lub ekspozycją na PNG, umożliwiła przeprowadzenie badań oceniających, czy szczepienie BCG zmniejsza ryzyko zakażenia prątkiem gruźlicy. Wykazano, że rzeczywiście chroni ono nie tylko przed aktywną postacią choroby, ale także przed samym zakażeniem prątkiem gruźlicy. Dzieci zaszczepione BCG, na co wskazywała obecność blizny poszczepiennej, nie tylko rzadziej chorowały na gruźlicę, ale także rzadziej osiągały dodatni wynik testu IGRA. Ryzyko zakażenia u dzieci szczepionych było o 39% mniejsze niż u dzieci nieszczepionych (ryzyko zachorowania o 49% mniejsze). Analiza badań dotyczących zachorowań na gruźlicę u dzieci do lat 16 z kontaktu z osobami prątkującymi wykazała, że szczepienie BCG uchroniło 27% dzieci przed zakażeniem prątkiem gruźlicy, a 71% przed zachorowaniem.
Kiedy należy podać szczepionkę BCG?
Zgodnie z zaleceniami WHO w krajach o dużej zapadalności na gruźlicę należy podawać pojedynczą dawkę szczepionki BCG wszystkim zdrowym noworodkom, bezpośrednio po urodzeniu. Jeśli nie można zaszczepić noworodka przy narodzinach, należy to zrobić przy najbliższej okazji, zanim dojdzie do ekspozycji na prątki gruźlicy. WHO zaleca także jednoczesne podanie szczepionki BCG i przeciwko wirusowemu zapaleniu wątroby typu B, ponieważ takie postępowanie jest bezpieczne. Niektórzy uważają, że opóźnienie szczepienia może poprawiać działanie szczepionki związane z większą dojrzałością układu immunologicznego. Badania odpowiedzi immunologicznej nie potwierdzają jednak słuszności tego poglądu. WHO nie zaleca rewakcynacji, ponieważ nie ma jednoznacznych dowodów, że takie postępowanie zapewnia dodatkową ochronę, a zwiększa ryzyko NOP.
Stanowisko innych krajów
W pierwszej połowie XX wieku w Europie powszechnie stosowano szczepienia BCG. Obecnie w krajach o małej zapadalności na gruźlicę szczepionkę BCG stosuje się selektywnie, jedynie w grupach ryzyka. Taką grupę stanowią na przykład imigranci z krajów o dużej zapadalności na gruźlicę, dzieci zamieszkujące w regionach, w których istnieje gorsza sytuacja epidemiologiczna gruźlicy, oraz z rodzin, w których wystąpiły przypadki choroby (p. Med. Prakt. Szczepienia 3/2018, s. 15–20 – przyp. red.). Szczepienie BCG może też zapewniać jakiegoś stopnia ochronę przed gruźlicą personelowi służby zdrowia, osobom z kontaktu z chorym na gruźlicę wielolekooporną oraz wyjeżdżającym do krajów o dużym rozpowszechnieniu gruźlicy.
Jako pierwsza w Europie od powszechnych szczepień BCG odstąpiła Czechosłowacja (po badaniach w latach 1961–1972), a potem Szwecja (w 1975 r.). W krajach, w których powszechne szczepienia BCG zamieniono na selektywne, obserwowano przejściowe zwiększenie liczby zachorowań na ciężkie postacie gruźlicy, zwłaszcza na gruźlicze ZOMR.
Kiedy można zrezygnować z powszechnych szczepień BCG?
Z powszechnych szczepień BCG można zrezygnować, gdy spełnione jest jedno z trzech kryteriów (p. „Punkt widzenia pediatry” – przyp. red.), takich jak:
- zapadalność na gruźlicę płuc z dodatnim wynikiem bakterioskopii plwociny wynosi ≤5 na 100 000 w 3 poprzedzających latach
- liczba zachorowań na gruźlicze ZOMR u dzieci <5 lat wynosi <1 przypadek na 10 mln osób z całej populacji w ciągu poprzednich 5 lat
- przeciętne roczne ryzyko zakażenia prątkiem gruźlicy wynosi ≤0,1%.
W 2017 roku w Polsce zapadalność na gruźlicę płuc u osób z dodatnim wynikiem badania bakterioskopowego plwociny wynosiła 6,4 na 100 000, a roczne ryzyko zakażenia obliczone metodą Karola Styblo – 0,13%. W latach 2013–2017 na gruźlicze ZOMR zachorowało 2 dzieci (1 w 1. rż. i 1 w wieku 3 lat).
W decyzji trzeba również uwzględnić, że szczepienie BCG może mieć nieswoisty efekt ochronny przed innymi zakażeniami, co zapewne ma większe znaczenie w krajach rozwijających się (natomiast w badaniu z randomizacją przeprowadzonym w Danii nie stwierdzono wpływu BCG m.in. na wskaźnik hospitalizacji ogólnej oraz ryzyko chorób infekcyjnych, p. Med. Prakt. Szczepienia 4/2016, s. 18–21 – przyp. red.).
Podsumowanie
BCG jest jedyną dostępną obecnie szczepionką zabezpieczającą dzieci przed rozsiewem krwiopochodnym prątków i w konsekwencji przed ciężkimi klinicznymi postaciami gruźlicy, w tym przed gruźliczym ZOMR. Wyniki badań z randomizacją wskazują, że szczepionka BCG chroni także przed gruźlicą płuc, zwłaszcza jeśli podano ją w okresie noworodkowym lub dzieciom w wieku szkolnym z ujemnym wynikiem PT. W niektórych populacjach ochrona utrzymuje się co najmniej przez 20 lat. W Polsce notuje się pojedyncze zgony dzieci z powodu gruźlicy. W latach 2012–2015 nie odnotowano żadnego zgonu dziecka z tej przyczyny. W ciągu ostatnich 5 lat nie stwierdzono żadnego przypadku prosówki u małych dzieci i 2 zachorowania na gruźlicze ZOMR u dzieci <5. roku życia. Dane te można uznać za potwierdzenie skuteczności szczepionki BCG i wskazanie do kontynuacji szczepień powszechnych. Istnieją również dowody, że BCG chroni także przed zakażeniem prątkiem gruźlicy.
Punkt widzenia pediatry
Pierwsze szczepienie, z którym spotykają się rodzice noworodka w Polsce, to szczepienie BCG podawane już w pierwszych dniach życia przed wypisaniem dziecka z oddziału noworodkowego do domu. To bardzo wczesne podanie szczepionki, krążące w internecie opinie o jej rzekomej nieskuteczności i dużym ryzyku NOP, a także informacje o rezygnacji wielu krajów z powszechnego szczepienia BCG sprawiają, że niektórzy rodzice mają wątpliwości co do celowości podawania BCG i nie wyrażają zgody na jej użycie. Przekonujących argumentów na konieczność jej stosowania w Polsce często nie mają także sami lekarze. Z tych względów opinia profesor Marii Korzeniewskiej-Koseły przedstawiona w pierwszej części artykułu jest bardzo wartościowa i potrzebna.
Argumenty przeciwko rezygnacji z powszechnych szczepień
Epidemiologia gruźlicy
Dane epidemiologiczne przytoczone na wstępie wskazują, że gruźlica nadal stanowi realne zagrożenie w naszym kraju, a przede wszystkim, że w naszym otoczeniu są osoby, które mogą stanowić źródło zakażenia. Proponując, wzorem innych krajów UE/EOG, rezygnację z powszechnych szczepień przeciwko gruźlicy, koniecznie trzeba porównać dane epidemiologiczne – czy dzieci w tamtych krajach mają taką samą szansę na kontakt z osobą prątkującą czy to ryzyko jest istotnie mniejsze? Dodatkową trudność sprawia fakt, że wskaźniki zapadalności na gruźlicę w Polsce są bardzo zróżnicowane w poszczególnych województwach. Na przykład w 2016 roku najmniejszy wskaźnik zapadalności odnotowano w województwie wielkopolskim (8,1/100 000), a największy w województwie mazowieckim (24,3/100 000). Jak widać, największy wskaźnik był aż 3-krotnie większy od najmniejszego, co bardzo utrudnia zaproponowanie jednolitej w całym kraju modyfikacji programu szczepień BCG.
Autorka przytoczyła w artykule zalecenia WHO dotyczące warunków rezygnacji z powszechnych szczepień BCG. Polska obecnie jest bliska spełnienia tylko kryterium liczby zachorowań na gruźlicze ZOMR u dzieci <5. roku życia, natomiast nie spełnia dwóch pozostałych. Wyraźnie widać, że wskaźniki epidemiologiczne istotnie się poprawiają, ale nie osiągnęły jeszcze oczekiwanych wartości.
Tylko grupy ryzyka?
Pojawiają się sugestie, aby zamienić model powszechnych szczepień noworodków przeciwko gruźlicy w Polsce na szczepienie dzieci z grup ryzyka. Taki pomysł rodzi jednak pytanie, czy wiadomo, które środowiska stanowią grupy ryzyka zachorowania na gruźlicę w Polsce? Jednoznacznie można tylko wskazać rodziny, w których są osoby chore na gruźlicę lub ją przechorowały. W krajach, w których większość chorych stanowią emigranci (np. na Malcie i Cyprze, w Szwecji i Norwegii), można dużo łatwiej wskazać takie zagrożone środowiska niż w Polsce. W 2016 roku zachorowania wśród cudzoziemców w Polsce stanowiły tylko 1,4% (92 przypadki, w tym 30 u obywateli Ukrainy). Podobnie jest z współwystępowaniem gruźlicy i zakażenia HIV, które często obserwuje się w wielu krajach UE, a w Polsce rzadko (w 2016 r. gruźlica była chorobą wskaźnikową tylko u 17 chorych na AIDS).
Analizując obecny model szczepień BCG w naszym kraju, warto zwrócić uwagę, że w Polsce, w porównaniu z innymi krajami UE/EOG, dzieci stanowią mały odsetek chorych (w 2016 r. 1,6 vs 4,3%). Przy zapadalności na gruźlicę w całej populacji większej niż w krajach UE/EOG, zapadalność w grupie wiekowej 0–14 lat jest w naszym kraju mniejsza niż w krajach UE/EOG (1,8/100 000 vs 3,1/100 000). Jest to istotny argument przemawiający za tym, że przyjęty w Polsce model zapobiegania gruźlicy u dzieci jest bardzo skuteczny.
Aspekty techniczne
Do rozważenia pozostają także pewne aspekty praktyczne szczepień przeciwko gruźlicy. Obecnie szczepienia te wykonują przede wszystkim pielęgniarki na oddziałach noworodkowych, które posiadają duże doświadczenie w tym zakresie. Szczepionkę BCG, w odróżnieniu od większości innych szczepionek, podaje się śródskórnie, co wymaga dobrego opanowania techniki takich wstrzyknięć. Według dostępnych danych NOP po BCG występują rzadko. W 2016 roku w sumie zanotowano <400 NOP po podaniu tej szczepionki, przy czym najczęściej było to powiększenie okolicznych węzłów chłonnych (180 przypadków), zmiany miejscowe w postaci krosty ropnej, owrzodzenia oraz ropnie podskórne (odpowiednio: 90,18 i 87 przypadków). Rzadkie występowanie zmian miejscowych może wynikać z dobrego opanowania techniki szczepienia przez pielęgniarki oddziałów noworodkowych. Ten argument przemawia także za pozostawieniem wykonywania szczepień BCG właśnie na tych oddziałach.
Problem ciężkich niedoborów odporności
Bardzo ciężkim powikłaniem szczepienia przeciwko gruźlicy może być uogólnione zakażenie prątkiem BCG, które występuje przede wszystkim u noworodków z pierwotnymi zaburzeniami odporności (głównie z ciężkim, złożonym niedoborem odporności – SCID) oraz zakażonych HIV. W Polsce w 2016 roku zgłoszono tylko 1 taki przypadek na 382 000 urodzeń. Niektórzy sugerują, aby w celu poprawy bezpieczeństwa dzieci opóźnić podanie szczepionki BCG. Takie postępowanie może być uzasadnione w krajach, w których często dochodzi do wertykalnego zakażenia dzieci wirusem HIV, gdzie szczepionkę BCG należałoby podać dopiero po wykluczeniu zakażenia HIV u noworodka. Zalecenie takie znajduje się także w polskim PSO, chociaż należy zaznaczyć, że w 2016 roku zanotowano tylko 1 przypadek zakażenia niemowlęcia od HIV-dodatniej matki.
Kwalifikacja do szczepienia BCG u noworodków opiera się przede wszystkim na dobrze zebranym wywiadzie rodzinnym dotyczącym występowania SCID lub innych ciężkich pierwotnych niedoborów odporności komórkowej, zakażeń inwazyjnych, posocznic lub nagłych zgonów w przebiegu zakażeń u najbliższych krewnych. Trudno określić, po jakim okresie obserwacji można wykluczyć zaburzenia odporności, ale należy podkreślić, że największe znaczenie ma ochrona najmłodszych dzieci przed gruźlicą, która w tej grupie wiekowej ma najcięższy przebieg.
Podsumowanie
Przedstawione w artykule dane wskazują, że sytuacja epidemiologiczna gruźlicy w Polsce systematycznie się poprawia. Jesteśmy coraz bliżej chwili, kiedy będziemy mogli zrezygnować z powszechnych szczepień dzieci, chociaż obecnie decyzja ta byłaby przedwczesna. Konieczne będzie opracowanie zaleceń dotyczących szczepień w wybranych grupach ryzyka, tak aby nie pogorszyć małych wartości wskaźników zapadalności na gruźlicę, jakie udało się osiągnąć do tej pory w Polsce.
Piśmiennictwo:
1. Korzeniewska-Koseła M. (red.): Gruźlica i choroby układu oddechowego w Polsce w 2017 r. Warszawa, Instytut Gruźlicy i Chorób Płuc, 20182. European Centre for Disease Prevention and Control/WHO Regional Office for Europe. Tuberculosis surveillance and monitoring in Europe 2018–2016 data. Stockholm, European Centre for Disease Prevention and Control, 2018
3. Dara M., Acosta C.D., Rusovich V. i wsp.: Bacille Calmette-Guérin vaccination: the current situation in Europe. Eur. Respir. J., 2014; 43: 24–35
4. BCG vaccines: WHO position paper – February 2018. World Health Organization. Weekly Epidemiological Record, 2018; 93 (8): 73–96
5. Dockrell H.M., Smith S.G.: What have we learnt about BCG vaccination in the last 20 years? Front. Immunol., 2017; 8: 1134
6. Mangtani P., Abubakar I., Ariti C. i wsp.: Protection by BCG vaccine against tuberculosis: a systemic review of randomized controlled trials. Clin. Infect. Dis., 2014; 58: 470–480
7. Szczuka I.: Zapobieganie gruźlicy. (W:) Krakówka P., Rowińska-Zakrzewska E. (red.): Gruźlica. Podręcznik dla studentów medycyny. Warszawa, PZWL, 1988: 263–273
8. Szczuka I.: Bezpieczeństwo szczepień BCG – niepożądane odczyny poszczepienne. Część I. Postacie powikłań. System nadzorowania. Przegl. Epidemiol., 2002; 56: 1–13
9. Szczepienia ochronne w Polsce w 2015 roku. Warszawa, PZH, GIS, 2016
10. Roy A., Eisenhut M., Harris R.J. i wsp.: Effect of BCG vaccination against Mycobacterium tuberculosis infection in children: systemic review and meta-analysis. BMJ, 2014; 349: g4643
11. Baily G.V.: Tuberculosis prevention trial, Madras. Indian J. Med. Res., 1980; 72 (supl.): 1–74
12. Aronson N.E., Santosham M., Comstock G.W. i wsp.: Long-term efficacy of BCG vaccine in American Indians and Alaska Natives: a 60-year follow-up study. JAMA, 2004; 291: 2086–2091
13. Mangtani P., Nguipdop-Djomo P., Keogh R.H. i wsp.: The duration of protection of school-aged BCG vaccination in England: a population-based case-control study. Int. J. Epidemiol., 2018; 47: 193–201
14. Nguipdop-Djomo P., Heldal E., Rodrigues L.C. i wsp.: Duration of BCG protection against tuberculosis and change in effectiveness with time since vaccination in Norway: a retrospective population-based cohort study. Lancet. Infect. Dis., 2016; 16: 219–226
15. Jones G. H. Szczepienie. (W:) Davis P.D.O, Lalvani A., Thillai M. (red): Gruźlica. Podręcznik klinicysty. MediPage, 2018: 187–198
16. Eisenhut M., Paranjothy S., Abubakar I. i wsp.: BCG vaccination reduces risk of infection with Mycobacterium tuberculosis as detected by gamma interferon release assay. Vaccine, 2009; 27: 6116–6120
17. Criteria for discontinuation of vaccination programmes using Bacille Calmett-Guerin (BCG) in countries with a low prevalence of tuberculosis. A statement of the International Union Against Tuberculosis and Lung Disease. Tuber. Lung Dis., 1994; 75: 179–181
18. Komunikat Głównego Inspektora Sanitarnego z dnia 31 października 2017 r. w sprawie Programu Szczepień Ochronnych na rok 2018. Dz. U. Ministra Zdrowia, poz. 108
19. Korzeniewska-Koseła M.: Gruźlica w Polsce w 2016 roku. Przegl. Epidemiol., 2018; 72: 189–205
20. Szczepienia Ochronne w Polsce w 2016 roku. Narodowy Instytut Zdrowia Publicznego – Państwowy Zakład Higieny–Zakład Epidemiologii, Główny inspektora Sanitarny – Departament Zapobiegania oraz Zwalczania Zakażeń i Chorób Zakaźnych u Ludzi, Warszawa, 2017
21. www.stat.gov.pl
22. Szmulik K., Zakrzewska K., Niedźwiedzka-Stadnik M., Rosińska M.: Zakażenia HIV i zachorowania na AIDS w Polsce w 2016 roku. Przegl. Epidemiol., 2018; 72: 175–187