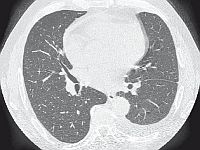
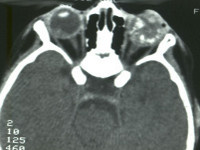
W kontrolnej TK nie stwierdzono jednak regresji zmian, pojawiły się natomiast cechy włóknienia płuc (ryc. 3).
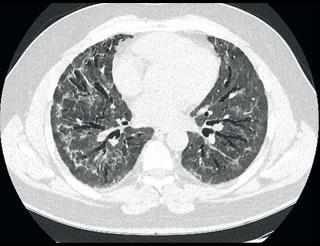
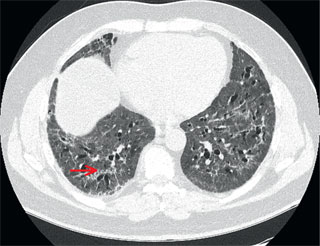
Z uwagi na ciężkość zaburzeń wentylacji oraz zmiany widoczne w TK po konsultacji pulmonologicznej oraz omówieniu
leczenia z chorym i za jego zgodą do leczenia dołączono pirfenidon (poza wskazaniami rejestracyjnymi). Rozpoczęto
stopniowe zmniejszanie dawki GKS p.o..
Z uwagi na utrzymującą się niewydolność oddechową oraz duże ryzyko zakrzepowo-zatorowe kontynuowano profilaktykę
przeciwzakrzepową. Zalecono ponadto pilne rozpoczęcie rehabilitacji oddechowej i ruchowej w warunkach domowych.
Komentarz
Pirfenidon dołączono do leczenia ze względu na radiologiczne cechy rozpoczynającego się włóknienia płuc. Lek ten
stosuje się w leczeniu idiopatycznego włóknienia płuc u dorosłych oraz innych chorób przebiegających z postępującym
włóknieniem miąższu płuc. Trwają badania nad jego skutecznością w zespole pokowidowym (post-COVID-19). Badania te
opierają się na hipotezie, według której końcowa ścieżka włóknienia płuc jest wspólna dla różnych chorób
śródmiąższowych płuc przebiegających z włóknieniem; istnieje więc potencjalny wspólny patomechanizm i nadzieja,
że leki przeciwwłóknieniowe wpłyną również na zmiany po COVID-19. Opublikowano wyniki jednego badania z randomizacją, w którym nie stwierdzono istotnych korzyści klinicznych z takiego leczenia, ale stwierdzono
zmniejszenie stężenia markerów zapalnych i potwierdzono bezpieczeństwo leczenia w tej grupie chorych. Kolejne
badania z randomizacją są w toku. Opublikowano ponadto pojedyncze doniesienia opisujące poprawę kliniczną pod
wpływem tej terapii.
Powikłania zakrzepowo-zatorowe COVID-19 mogą występować nawet 3 miesiące po ostrej fazie choroby, a ryzyko jest
wielokrotnie większe niż w populacji ogólnej. U omawianego chorego dodatkowo zwiększały je niewydolność oddechowa
i znacznie ograniczona ruchomość, dlatego przez cały czas kontynuowano profilaktykę przeciwzakrzepową.
Zespół pokowidowy: po 12 tygodniach od początku choroby
Opis przypadku cd.
W 4. miesiącu utrzymywania się objawów (102. dzień) pacjent zgłosił się na kolejną kontrolę do poradni
pulmonologicznej. Skarżył się na wciąż utrzymującą się umiarkowaną duszność, bardzo uciążliwy kaszel (bardziej
nasilony niż podczas zakażenia) oraz przewlekłe, nasilone zmęczenie. Spoczynkowe SpO2 wahało się w przedziale 83%-88%. W gazometrii stwierdzono utrzymującą się całkowitą niewydolność oddechową. Badania czynnościowe
płuc wykazały poprawę (tab. 1 - 102. dzień objawów). Kontynuowano leczenie pirfenidonem przez kolejne 10 dni, a po
40 dniach stosowania ostawiono go z powodu kosztów przerastających możliwości finansowe (lek stosuje się poza
wskazaniami, więc nie jest refundowany) oraz braku ewidentnej skuteczności klinicznej. Kontynuowano NIV i profilaktykę przeciwzakrzepową.
Na kolejną wizytę chory zgłosił się 2 miesiące później, po 3-tygodniowej rehabilitacji oddechowej na oddziale
rehabilitacyjnym, gdzie stosowano rehabilitację dostosowaną do stanu pacjenta. Po rehabilitacji zgłaszał znaczną
poprawę samopoczucia oraz lepszą tolerancję wysiłku. Ustąpiła hiperkapnia i możliwe było zakończenie NIV. Chory
używał koncentratora tlenu tylko podczas wysiłku.
Ponadto mężczyzna skarżył się nadal na suchy, napadowy kaszel. Z tego powodu kilka tygodni wcześniej włączono
budezonid w nebulizacji, który spowodował zmniejszenie nasilenia kaszlu. SpO2 wynosiło 93%, w gazometrii
nie obserwowano cech niewydolności oddechowej. W badaniach czynnościowych wykonanych w 164. dniu od zachorowania
stwierdzono poprawę czynności płuc (tab. 1). Po raz pierwszy możliwe było wykonanie testu 6-minutowego marszu
(6-MWT), w którym stwierdzono krótki dystans marszu i spadek SpO2 podczas wysiłku. Odstawiono GKS
p.o., którego dawkę wcześniej stopniowo zmniejszano (lek stosowano łącznie przez ok. 3 mies.).
Komentarz
Programy rehabilitacji oddechowej u chorych po COVID-19 obejmują m.in. treningi wytrzymałościowe, ćwiczenia: oddechowe, efektywnego kaszlu, ogólnousprawniające, na wolnym powietrzu, a także oklepywanie klatki piersiowej, drenaż ułożeniowy, treningi marszowe, balneoterapię i treningi relaksacyjne. Skuteczność rehabilitacji ocenia się przez porównanie wyników badań (m.in. 6-MWT, skala nasilenia duszności, spirometria, ocena funkcjonalna w skali Barthel) przeprowadzanych na początku oraz na końcu pobytu na oddziale. W omawianym przypadku rehabilitacja przyniosła bardzo dobre efekty.
Opis przypadku cd.
Na wizycie kontrolnej 2,5 miesiąca później pacjent zgłaszał dobre samopoczucie, nie potrzebował już przenośnego
koncentratora tlenu, który wcześniej stosował przy każdej aktywności. W badaniach czynnościowych płuc obserwowano
dalszą poprawę (tab. 1 - 244. dzień objawów).
Podczas badania podmiotowego z chorym lekarz pogłębił wywiad w kierunku objawów bezdechu sennego. Pacjent nie
zgłaszał wcześniej objawów tej choroby (należy pamiętać, że przez długi czas stosowano NIV znoszącą objawy OBS),
jednak lekarz dopytując go, dowiedział się, że mężczyzna aktualnie chrapie w nocy i budzi się bardzo zmęczony. Z tego powodu zlecono badanie polisomnograficzne.
Kolejna planowa wizyta odbyła się 2,5 miesiąca później. Pacjent czuł się dobrze, zgłaszał znaczną poprawę kondycji
fizycznej. W badaniu podmiotowym nad polami płucnymi stwierdzono szmer pęcherzykowy z trzeszczeniami u podstawy obu
płuc. Na podstawie wyników badania polisomnograficznego rozpoznano ciężki obturacyjny bezdech senny z towarzyszącymi
spadkami saturacji do 66%. Chory został zakwalifikowany do próby wdrożenia leczenia wspomaganiem oddychania stałym
dodatnim ciśnieniem oddechowym (CPAP) i oceny jego skuteczności. Zalecono mu ponadto zmniejszenie masy ciała.
Komentarz
Obraz kliniczny obturacyjnego bezdechu sennego można podzielić na objawy występujące w ciągu dnia (nadmierna senność,
poranny ból głowy, związany z hipoksemią i hiperkapnią w czasie snu, zaburzenia pamięci i koncentracji, osłabienie
libido) oraz występujące w nocy (m.in. chrapanie, bezdechy, nocne poty, uczucie duszności lub dławienia się podczas
snu).
Obturacyjny bezdech senny rozpoznaje się na podstawie wyniku polisomnografii oraz oceny obecności objawów według
kryteriów AASM:
- ≥15 epizodów oddechowych (bezdech, spłycenie oddychania, przebudzenie związane z wysiłkiem oddechowym) na godzinę snu, niezależnie od obecności objawów klinicznych
- ≥5 epizodów oddechowych na godzinę snu z 1 z objawów (nadmierna senność dzienna, przebudzenia z uczuciem zatrzymania oddechu, głośne chrapanie).
Ciężki OBS może powodować senność dzienną, nawet w sytuacjach, które wymagają dużej koncentracji (rozmowa, kierowanie pojazdem), pogarsza jakość życia pacjentów, zwiększa ryzyko nadciśnienia tętniczego i innych chorób układu krążenia.
Opis przypadku cd.
Podczas kolejnej wizyty obserwowano dalszą, stopniową poprawę wydolności wysiłkowej oraz wyraźną poprawę w badaniach czynnościowych płuc (tab. 1 - badanie w 328. dniu). W TK klatki piersiowej stwierdzono dalsze utrzymywanie się niepełnej powietrzności miąższu płuc, poszerzenia oskrzeli oraz zmian sugerujących zwłóknienie - ryc. 4. Pacjent dobrze tolerował leczenie CPAP - podawał, że lepiej się wysypia w nocy i czuje się mniej zmęczony. Chory nadal pozostaje pod opieką poradni pulmonologicznej.
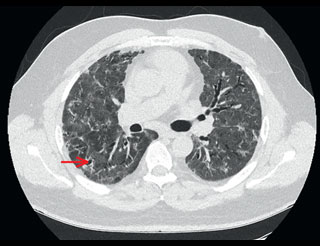
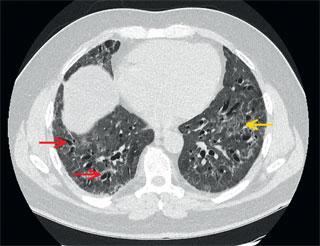
Piśmiennictwo:
1. Agencja Oceny Technologii Medycznych i Taryfikacji: Farmakoterapia COVID-19 - aktualizacja. Wersja 2.9 Data ukończenia - 14.10.2021 r. https://www.aotm.gov.pl/covid-19/zalecenia-w-covid-19/2. Agencja Oceny Technologii Medycznych i Taryfikacji: Przegląd doniesień naukowych dla glikokortykosteroidów (GKS) wziewnych w leczeniu COVID-19. Wersja 1.0. Data ukończenia 27.04.2021 r. https://www.aotm.gov.pl/covid-19/zalecenia-w-covid-19/
3. RECOVERY Collaborative Group; Horby P.,Lim W.S., Emberson J.R. i wsp.: Dexamethasone in hospitalized patients with Covid-19. N. Engl. J. Med., 2021; 384: 693-704
4. Prado Jeronimo C.M., Leao Farias M.E., Almeida Val F.F. i wsp.: Methylprednisolone as adjunctive therapy for patients hospitalized with coronavirus disease 2019 (COVID-19; Metcovid): a randomized, double-blind, phase IIb, placebo-controlled trial. Clin. Infect. Dis., 2021; 72: e373-e381
5. Edalatifard M., Akhtari M., Salehi M. i wsp.: Intravenous methylprednisolone pulse as a treatment for hospitalised severe COVID-19 patients: results from a randomised controlled clinical trial. Eur. Respir. J., 2020; 56:2 002 808
6. Polak S.B., Van Gool I.C., Cohen D. i wsp.: Systematic review of pathological findings in COVID-19: a pathophysiological timeline and possible mechanisms of disease progression. Mod. Pathol., 2020; 33: 2128-2138
7. Hariri L.P., North C.M., Shih A.R. i wsp.: Lung histopathology in coronavirus disease 2019 as compared with severe acute respiratory sydrome and H1N1 influenza: a systematic review. Chest, 2020; S0012-3692(20)34 868-6
8. Myall K.J., Mukherjee B., Castanheira A.M. i wsp.: Persistent post-COVID-19 interstitial lung disease. An observational study of corticosteroid treatment. Ann. Am. Thorac. Soc., 2021; 18: 799-806
9. Antoniou K.M., Vasarmidi E., Russell A.M. i wsp.: European Respiratory Society statement on long COVID-19 follow up. Eur. Respir. J., 2022. doi: org/10.1183/13993003.02174-2021
10. Mandal S., Barnett J., Brill S.E. i wsp.; ARC Study Group: 'Long-COVID': a cross-sectional study of persisting symptoms, biomarker and imaging abnormalities following hospitalisation for COVID-19. Thorax, 2021; 76: 396-398
11. Ramacciotti E., Barile Agati L., Calderaro D. i wsp.: Rivaroxaban versus no anticoagulation for post-discharge thromboprophylaxis after hospitalisation for COVID-19 (MICHELLE): an open-label, multicentre, randomised, controlled trial. Lancet, 2022; 399: 50-59
12. Kory P., Kanne J.P.: SARS-CoV-2 organising pneumonia: has there been a widespread failure to identify and treat this prevalent condition in COVID-19? BMJ Open Respir. Res., 2020; 7: e000 724
13. De Oliveira Filho C.M., Vieceli T., de Fraga Basotto C. i wsp.: Organizing pneumonia: a late phase complication of COVID-19 responding dramatically to corticosteroids. doi: 10.1016/j.bjid.2021.101 541
14. Basarakodu K.R., Aronow W.S., Nair C.K. i wsp.: Differences in treatment and in outcomes between idiopathic and secondary forms of organizing pneumonia. Am. J. Ther., 2007; 14: 422-426. doi: 10.1097/01.pap.0000249905.63211.a1
15. Cordier J.F.: Organising pneumonia. Thorax, 2000; 55: 318-328
16. Antoniou K.M., Vasarmidi E., Russell A.-M. i wsp.: European Respiratory Society Statement on long COVID-19 follow-up. Eur. Respir. J., 2022. doi: 10.1183/13993003.02174-2021
17. Piotrowski W., Barczyk A., Chciałowski A. i wsp.: Statement of Polish Respiratory Society and Polish Society of Allergology on the treatment of pulmonary complications in patients after SARS-CoV-2 infection. Alergol. Pol. Pol. J. Allergol., 2021; 8: 101-129
18. Acat M., Yildiz Gulhan P., Oner S. i wsp.: Comparison of pirfenidone and corticosteroid treatments at the COVID-19 pneumonia with the guide of artificial intelligence supported thoracic computed tomography. Int. J. Clin. Pract., 2021; 75: e14961
19. Zhang F., Wei Y., He L. i wsp.: A trial of pirfenidone in hospitalized adult patients with severe coronavirus disease 2019. Chin. Med. J., 2021; December 01. doi: 10.1097/CM9.0000000000001614