Wstęp
Choroba Pompego (glikogenoza typu II, Pompe disease) to uwarunkowana genetycznie lizosomalna choroba spichrzeniowa spowodowana częściowym lub całkowitym niedoborem aktywności kwaśnej α-glukozydazy (GAA). Dziedziczona jest w sposób autosomalny recesywny. U osoby chorej występują dwie mutacje genu GAA kodującego kwaśną α-glukozydazę.
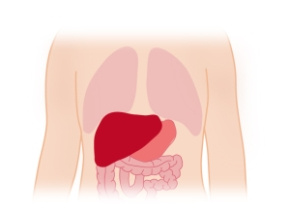
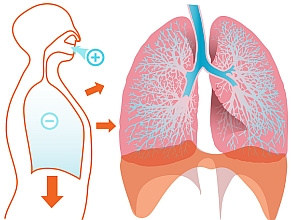
Kwaśna α-glukozydaza – należąca do hydrolaz lizosomalnych – uczestniczy w rozkładzie glikogenu do glukozy. W wyniku niedoboru tego enzymu postępuje akumulacja glikogenu w komórkach różnych tkanek, a w szczególności w mięśniach szkieletowych i w mięśniu sercowym, co ostatecznie prowadzi do upośledzenia ich funkcji.
Choroba Pompego należy do chorób rzadkich, czyli takich, których częstość występowania jest mniejsza niż 1 : 2000. Obecnie w Polsce zdiagnozowano kilkudziesięciu chorych na chorobę Pompego, jednak rzeczywista ich liczba jest prawdopodobnie wyższa. Wynika to z dużej różnorodności klinicznej poszczególnych przypadków i trudności z ustaleniem ostatecznego rozpoznania. Około 50 polskich pacjentów leczy się metodą enzymatycznej terapii zastępczej. U około 20 z nich chorobę zdiagnozowano we wczesnym dzieciństwie.
Obraz kliniczny choroby Pompego
Objawy kliniczne i wiek ich wystąpienia różnią się w zależności od stopnia zachowanej resztkowej aktywności kwaśnej α-glukozydazy. Postać niemowlęcą (klasyczna, infantile-onset Pompe disease) wywołuje całkowity lub prawie całkowity niedobór enzymu (aktywność <1%); postać o późnym początku wiąże się z częściowym niedoborem GAA (1–40%).
W postaci niemowlęcej choroby Pompego objawy pojawiają się przed 1. rokiem życia (średnio 4. miesiąc życia). U chorych niemowląt stwierdza się przerost mięśnia sercowego, kardiomegalię, zaburzenia rytmu serca, hepatomegalię, powiększenie języka. Uogólnione osłabienie mięśni oraz hipotonia prowadzą do opóźnionego rozwoju motorycznego oraz niewydolności oddechowej. Słaby przyrost masy ciała i wzrostu wiąże się z trudnościami z połykaniem i karmieniem. Nieleczona choroba prowadzi do zgonu, najczęściej pod koniec 1. roku życia.
Postać późna choroby Pompego (late-onset Pompe disease) z powodu wyższej resztkowej aktywności enzymu ma „łagodniejszy” fenotyp, ale mimo to znacząco wpływa na oczekiwaną długość i jakość życia chorych. Objawy mogą wystąpić w każdym wieku, od wczesnego dzieciństwa do późnej starości.
Najczęstszą prezentację choroby stanowi niedowład i zanik mięśni proksymalnych – głównie kończyn dolnych (zespół obręczowo-kończynowy). Chorzy mają trudności z chodzeniem, bieganiem, wchodzeniem po schodach, wstawaniem z pozycji siedzącej lub leżącej; stwierdza się objawy Gowersa i Trendelenburga. Wśród innych objawów obserwuje się osłabienie mięśni tułowia, mięśni przykręgosłupowych, pogłębioną lordozę lędźwiową czy skoliozę.
W przebiegu choroby dochodzi ponadto do postępującego osłabienia mięśni oddechowych. Dotyczy to zwłaszcza przepony, a na zaawansowanym etapie choroby także mięśni górnych dróg oddechowych oraz mięśni międzyżebrowych i brzusznych. Objawy, które zgłaszają pacjenci, to głównie męczliwość po niewielkim wysiłku fizycznym, duszność nasilająca się w pozycji leżącej, a także poranne bóle głowy, trudności w koncentracji spowodowane nocną hipowentylacją oraz obturacyjnym bezdechem sennym. Wraz z postępem choroby dochodzi do rozwoju przewlekłej niewydolności oddechowej, która jest główną przyczyną zgonu chorych z późną postacią choroby Pompego.
Pierwszą manifestację choroby stanowi ostra niewydolność oddechowa, najczęściej w przebiegu infekcji czy znieczulenia ogólnego.
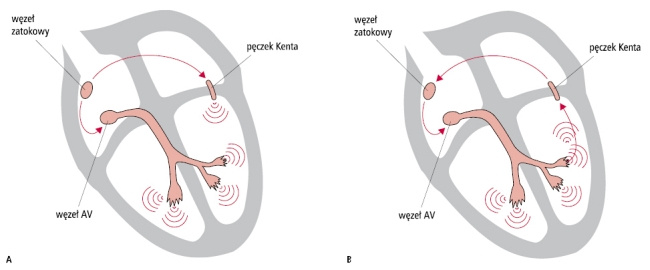
W późnej postaci choroby Pompego również dochodzi do zajęcia układu sercowo-naczyniowego, jednak kardiomiopatia przerostowa jest rzadkim objawem – częściej stwierdza się zaburzenia rytmu i przewodzenia.
Ze względu na gromadzenie się glikogenu w komórkach mięśni gładkich ścian naczyń krwionośnych u chorych obserwuje się większą skłonność do tworzenia tętniaków (wewnątrzczaszkowych oraz tętniaków aorty).
W badaniach laboratoryjnych stwierdza się zwiększenie stężeń transaminaz, dehydrogenazy mleczanowej oraz kinazy keratynowej (zwiększenie 15 × norma), co wiąże się z uszkodzeniem mięśni. Nieprawidłowe wyniki badań mogą być pierwszą i/lub jedyną manifestacją choroby Pompego, choć prawidłowe stężenie CK nie wyklucza rozpoznania późnej postaci choroby Pompego.
Rozpoznanie ułatwia wykonanie badania elektromiograficznego, w którym można stwierdzić cechy pierwotnego uszkodzenia mięśni, przy czym niekiedy zmiany obserwuje się jedynie w mięśniach przykręgosłupowych.
Diagnostyka i rozpoznanie choroby Pompego
Z powodu niejednorodności objawów, szczególnie u pacjentów z postacią późną, rozpoznanie choroby Pompego jest trudne. Objawy mogą sugerować występowanie innych miopatii, chorób neuronu ruchowego oraz zaburzeń łącza nerwowo-mięśniowego. W tabelach zestawiono objawy kliniczne choroby Pompego, a także najczęstsze choroby, które należy uwzględnić w diagnostyce różnicowej.
Rozpoznanie ustala się na podstawie stwierdzenia deficytu kwaśnej α-glukozydazy oraz wyniku badania molekularnego, potwierdzającego występowanie wariantów patogennych w obu allelach genu GAA.
Złoty standard diagnostyki stanowi ocena aktywności kwaśnej α-glukozydazy w leukocytach lub fibroblastach. Dostępny jest również test przesiewowy, wykonywany w celu oceny aktywności enzymu w suchej kropli krwi (dried blood spot testing – DBS), jednak ze względu na ryzyko wyniku fałszywie dodatniego test ten należy potwierdzić za pomocą badania molekularnego i/lub badania aktywności enzymu w leukocytach.
Większość pacjentów syntetyzuje pewną ilość niefunkcjonalnej α-glukozydazy; są to tzw. CRIM+ (syntetyzujący krzyżowo reagujący materiał immunologiczny – cross-reactive immunologic material). Niektórzy pacjenci w ogóle nie syntetyzują α-glukozydazy (CRIM–), co łączy się z cięższym przebiegiem choroby.
Biopsja mięśni jako wstępne badanie u osoby z dużym prawdopodobieństwem wystąpienia choroby Pompego nie jest zalecana. Jeśli wynik biopsji mięśnia sugeruje chorobę, należy wykonać badanie enzymatyczne lub badanie genetyczne. Ponadto ujemny wynik biopsji mięśnia nie wyklucza rozpoznania choroby Pompego.
Leczenie
W przeszłości leczenie choroby Pompego opierało się wyłącznie na opiece paliatywnej. Od kilku lat chorzy mogą być leczeni w ramach programu lekowego finansowanego przez Narodowy Fundusz Zdrowia. Terapia polega na podawaniu w warunkach szpitalnych syntetycznego enzymu – alglukozydazy α – w dawce 20 mg/kg masy ciała raz na dwa tygodnie, w infuzji dożylnej trwającej co najmniej 2 godziny.