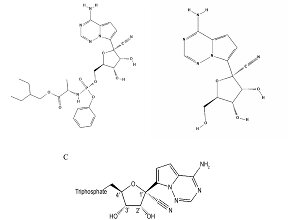
25 czerwca br. Komitet ds. Produktów Leczniczych Stosowanych u Ludzi (CHMP), zajmujący się z ramienia Europejskiej Agencji Leków (EMA) oceną naukową produktów leczniczych, zarekomendował przyznanie warunkowego pozwolenia na dopuszczenie do obrotu dla produktu leczniczego Veklury, zawierającego remdesiwir, przeznaczonego do leczenia zakażenia wirusem SARS-CoV-2. Remdesiwir jest pierwszym lekiem przyczynowym przeciwko SARS-CoV-2, zarekomendowanym do rejestracji w UE we wskazaniu COVID-19.
Wraz z publikacją swojego stanowiska EMA opublikowała również zaktualizowaną informację o leku dla personelu medycznego. Zgodnie z tym dokumentem redmesiwir podaje się dożylnie, jego stosowanie jest ograniczone do placówek opieki zdrowotnej, a pacjenci powinni być ściśle monitorowani. Wskazania: leczenie COVID-19 u dorosłych i młodzieży ≥12 lat o masie ciała ≥40 kg z zapaleniem płuc wymagającym dodatkowego podawania tlenu. Dawkowanie: należy rozpocząć od podania remdesiwiru pierwszego dnia w dawce 200 mg i.v., a następnie w dawce 100 mg i.v. przez kolejne co najmniej 4 dni, a jeśli nie zaobserwowano zadowalającej poprawy, leczenie należy kontynuować do 10 dni od podania pierwszej dawki.
Pozytywna ocena złożonego wniosku opierała się w dużej mierze na danych pochodzących z wieloośrodkowego badania klinicznego z randomizacją NIAID-ACTT-1 koordynowanego przez amerykański Narodowy Instytut Alergii i Chorób Zakaźnych (p. Remdesiwir w porównaniu z placebo u chorych na COVID-19 leczonych w szpitalu z powodu zapalenia dolnych dróg oddechowych – wstępne wyniki badania ACTT-1). Na ich podstawie EMA uznała, że bilans korzyści z leczenia i ryzyka niekorzystnych następstw jest dodatni u chorych na COVID-19 o ciężkim przebiegu, tzn. pacjentów z objawami zapalenia płuc wymagających tlenoterapii.
Kolejnym, ostatecznym krokiem w procedurze warunkowego dopuszczenia do obrotu preparatu remdesiwiru jest teraz decyzja Komisji Europejskiej, która według komunikatu EMA będzie wydana już na początku lipca. Warunkowe pozwolenie na dopuszczenie do obrotu będzie obowiązywało maksymalnie 1 rok, po upływie którego może zostać przedłużone. Może zostać również w każdym momencie przekształcone w „standardowe” pozwolenie na dopuszczenie do obrotu lub wycofane, zależnie od pojawiających się nowych danych naukowych. Podmiot odpowiedzialny będzie musiał przedłożyć do EMA sprawozdania końcowe z badań remdesiwiru do grudnia br., ale dodatkowe dane dotyczące jakości leku, a także ostateczne dane dotyczące śmiertelności z badań klinicznych muszą wpłynąć do agencji najpóźniej w sierpniu br. Po dopuszczeniu remdesiwiru do obrotu w UE ścisłe monitorowanie bezpieczeństwa leku będzie prowadzone według sporządzonego planu zarządzania ryzykiem, a kolejne dane dotyczące jego skuteczności i bezpieczeństwa stosowania, gromadzone na podstawie wciąż trwających badań i przesyłanych raportów dotyczących pacjentów leczonych poza badaniami klinicznymi, będą regularnie oceniane przez CHMP i Komitet ds. Oceny Ryzyka w ramach Nadzoru nad Bezpieczeństwem Farmakoterapii (PRAC).
Piśmiennictwo:
1. Komunikat prasowy EMA z dn. 25.06.2020 nt. wydania pozytywnej opinii dla wydania warunkowego pozwolenia na dopuszczenie do obrotu preparatu Veklury (remdesiwir): https://www.ema.europa.eu/en/news/first-covid-19-treatment-recommended-eu-authorisation [dostęp 26.06.2020]2. Stanowisko Komitetu ds. Produktów Leczniczych Stosowanych u Ludzi (CHMP) ws. wydania warunkowego pozwolenia na dopuszczenie do obrotu preparatu Veklury (remdesiwir): https://www.ema.europa.eu/en/documents/smop-initial/chmp-summary-positive-opinion-veklury_en.pdf [dostęp 26.06.2020]
3. Informacja o preparacie Veklury zaaprobowana przez Komitetu ds. Produktów Leczniczych Stosowanych u Ludzi (CHMP) na dzień 25.06.2020: https://www.ema.europa.eu/en/documents/other/veklury-product-information-approved-chmp-25-june-2020-pending-endorsement-european-commission_en.pdf [dostęp 26.06.2020]
4. Komunikat prasowy Narodowego Instytutu Alergii i Chorób Zakaźnych „NIH Clinical Trial Shows Remdesivir Accelerates Recovery from Advanced COVID-19” z dn. 29.04.2020: https://www.niaid.nih.gov/news-events/nih-clinical-trial-shows-remdesivir-accelerates-recovery-advanced-covid-19 [dostęp 26.06.2020]