Opracowali: Anna Bagińska, dr n. med. Jacek Mrukowicz
Skróty: ACTT – Adaptive COVID-19 Treatment Trial, ALT – aminotransferaza alaninowa, AST – aminotransferaza asparaginianowa, aRB – skorygowana korzyść względna, aHR – skorygowany hazard względny, CI – przedział ufności, COVID-19 (coronavirus disease) – choroba spowodowana przez SARS-CoV-2, eGFR – oszacowana wielkość przesączania kłębuszkowego, ECMO (extracorporeal membrane oxygenation) – pozaustrojowa oksygenacja przezbłonowa, ITT – analiza wyników w grupach wyodrębnionych zgodnie z zaplanowanym leczeniem, OR – iloraz szans, RCT – badanie z randomizacją, RT-PCR (reverse transcription polymerase chain reaction) – reakcja odwrotnej transkrypcji i reakcja łańcuchowa polimerazy, SARS-CoV-2 (severe acute respiratory syndrome coronavirus 2) – koronawirus zespołu ostrej niewydolności oddechowej 2
Metodyka: wieloośrodkowe RCT (73 szpitale w Stanach Zjednoczonych [79,8% chorych], Europie [15,3%] i Azji [4,9%]), próba podwójnie ślepa; analiza ITT
Populacja: 1063 dorosłych (wiek śr. 59 lat, mężczyźni 64%) chorych na COVID-19 (potwierdzoną metodą RT-PCR) hospitalizowanych z powodu zapalenia dolnych dróg oddechowych (w większości zapalenia płuc); choroby współistniejące: 0 u 21%, 1 u 27%, ≥2 u 52% (najczęściej nadciśnienie tętnicze – 50%, otyłość – 37%, cukrzyca typu 2 – 30% chorych); mediana czasu od pojawienia się objawów COVID-19 do randomizacji – 9 dni; nasilenie choroby w chwili kwalifikacji (ocena w 8-stopniowej skali, gdzie: 1 – chory niehospitalizowany, zdolny do zwykłej aktywności, 2 – chory niehospitalizowany, niezdolny do podejmowania codziennych aktywności lub wymagający tlenoterapii w warunkach domowych, 3 – chory hospitalizowany, niewymagający tlenoterapii ani specjalistycznej opieki medycznej z powodu COVID-19, np. hospitalizowany z powodów epidemiologicznych (izolacja), 4 – chory hospitalizowany, niewymagający tlenoterapii, ale wymagający specjalistycznej opieki medycznej, 5 – chory hospitalizowany, wymagający tlenoterapii, 6 – chory hospitalizowany, wymagający wysokoprzepływowej tlenoterapii donosowej lub nieinwazyjnej wentylacji mechanic znej, 7 – chory hospitalizowany, wymagający inwazyjnej wentylacji mechanicznej płuc lub ECMO, 8 – zgon): stopień 4 – 12%, 5 – 40%, 6 – 18%, 7 – 26%, brak danych na temat stopnia nasilenia choroby – 4% chorych
Interwencja: remdesiwir i.v. 200 mg w 1. dniu terapii, następnie 100 mg/d przez 9 dni
Kontrola: placebo przez 10 dni Wszyscy chorzy jednocześnie otrzymywali leczenie wspomagające zgodnie z lokalnymi wytycznymi postępowania z chorymi na COVID-19. W trakcie badania niedozwolone było stosowanie innych terapii eksperymentalnych oraz leków poza zarejestrowanymi wskazaniami (off-label), chyba że ich stosowanie zalecały wewnętrzne wytyczne szpitala, w którym leczono chorego.
Wyniki: p. tab. Objawy niepożądane występowały z podobną częstością w obu grupach. U chorych otrzymujących remdesiwir najczęściej obserwowano: niedokrwistość (7,9% vs 9,0% w grupie placebo), ostre uszkodzenie nerek, zmniejszenie eGFR lub zmniejszenie klirensu kreatyniny, lub zwiększenie stężenia kreatyniny we krwi (7,4% vs 7,3%), gorączkę (5,0% vs 3,3%), zwiększenie stężenia glukozy we krwi (4,1% vs 3,3%), zwiększoną aktywność ALT i/lub AST we krwi (4,1% vs 5,9%). Ciężkie objawy niepożądane wystąpiły u 114 z 521 chorych przyjmujących remdesiwir (21,1%) i u 141 z 522 chorych otrzymujących placebo (27,0%), a odsetek chorych, u których przerwano leczenie z powodu objawów niepożądanych lub wycofania zgody na udział w badaniu, był podobny w obu grupach (odpowiednio 9,2% vs 10,2%).
| Tabela. Remdesiwir w porównaniu z placebo u dorosłych chorych na COVID-19 hospitalizowanych z powodu zapalenia dolnych dróg oddechowych w okresie 29 dnia | |||
|---|---|---|---|
| Punkty końcowe | Remdesiwir | Placebo | |
| aRB (95% CI)c | |||
| czas do wyleczeniab, dni (mediana) | 11 | 15 | 1,31 (1,12–1,54) |
| aHR (95% CI)c | |||
| zgond (%) | 7,1 | 11,9 | 0,74 (0,5–1,1) |
| OR (95% CI) | |||
| zmniejszenie nasilenia chorobye | – | – | 1,50 (1,18–1,91) |
| chorzy z początkowym nasileniem choroby w stopniu 4 | |||
| RB (95% CI) | |||
| czas do wyleczeniab, dni (mediana) | 5 | 6 | 1,38 (0,94–2,03) |
| HR (95% CI) | |||
| zgond (%) | 1,5 | 2,5 | 0,46 (0,04–5,08) |
| OR (95% CI) | |||
| zmniejszenie nasilenia chorobye | – | – | 1,51 (0,76–3,00) |
| chorzy z początkowym nasileniem choroby w stopniu 5 | |||
| RB (95% CI) | |||
| czas do wyleczeniab, dni (mediana) | 7 | 9 | 1,47 (1,17–1,84) |
| HR (95% CI) | |||
| zgond (%) | 2,4 | 10,9 | 0,22 (0,08–0,58) |
| OR (95% CI) | |||
| zmniejszenie nasilenia chorobye | – | – | 1,31 (0,89–1,92) |
| chorzy z początkowym nasileniem choroby w stopniu 6 | |||
| RB (95% CI) | |||
| czas do wyleczeniab, dni (mediana) | 16 | 22 | 1,20 (0,79–1,81) |
| HR (95% CI) | |||
| zgond (%) | 15,2 | 14,7 | 1,12 (0,53–2,38) |
| OR (95% CI) | |||
| zmniejszenie nasilenia chorobye | – | – | 1,60 (0,89–2,86) |
| chorzy z początkowym nasileniem choroby w stopniu 7 | |||
| RB (95% CI) | |||
| czas do wyleczeniab, dni (mediana) | ON | 28 | 0,95 (0,64–1,42) |
| HR (95% CI) | |||
| zgond (%) | 11,3 | 14,1 | 1,06 (0,59–1,92) |
| OR (95% CI) | |||
| zmniejszenie nasilenia chorobye | – | – | 1,04 (0,64–1,68) |
|
a wyniki na dzień 28.04.2020 r. dla 1059 chorych (538 w grupie remdesiwiru i 521 w grupie
placebo), dla których dostępne były dane z częściowej lub pełnej obserwacji (4 chorych – 3 w grupie remdesiwiru i 1 w grupie placebo – nie uwzględniono w analizie z powodu braku jakichkolwiek danych po randomizacji) – w tym czasie 391 chorych w grupie eksperymentalnej i 340 chorych w grupie placebo ukończyło 29-dniowy okres obserwacji
b zdefiniowanego jako pierwszy dzień w ciągu 28 dni od randomizacji z nasileniem objawów w stopniu 1, 2 lub 3 w 8-stopniowej skali (opis – p. tekst [„Populacja”]) c z uwzględnieniem poprawki na wyjściowe nasilenie choroby w 8-stopniowej skali d w okresie 14 dni od randomizacji e zmniejszenie nasilenia choroby w 8-stopniowej skali (opis – p. tekst [„Populacja”], ocena w 15. dniu od randomizacji) ON – oszacowanie niemożliwe | |||
Wnioski
Wstępne wyniki badania ACTT-1 wskazują, że u dorosłych chorych na COVID-19 hospitalizowanych z powodu zapalenia dolnych dróg oddechowych o ciężkim przebiegu stosowanie remdesiwiru, w porównaniu ze stosowaniem placebo, skróciło czas do wyleczenia.
KOMENTARZ
prof. dr hab. n. med. Miłosz Parczewski1, dr n. med. Jacek Mrukowicz2
1 Klinika Chorób Zakaźnych, Tropikalnych i Nabytych Niedoborów Immunologicznych, Pomorski Uniwersytet Medyczny w Szczecinie
2 Polski Instytut Evidence Based Medicine, Kraków
Jak cytować: Parczewski M., Mrukowicz J.: Komentarz. W: Remdesiwir w porównaniu z placebo u chorych na COVID-19 leczonych w szpitalu z powodu zapalenia dolnych dróg oddechowych – wstępne wyniki badania ACTT-1. Med. Prakt., 2020; 6: nn–nn
Skróty: ACTT-1 – Adaptive COVID-19 Treatment Trial, aHR - skorygowany hazard względny, ARD – różnica bezwzględna ryzyka, CI - przedział ufności, COVID-19 (coronavirus disease) – choroba spowodowana przez SARS-CoV-2, ECMO (extracorporeal membrane oxygenation) – pozaustrojowa oksygenacja przezbłonowa, GKS – glikokortykosteroid(y), HR - hazard względny, MERS-CoV (Middle East respiratory syndrome coronavirus) – bliskowschodni zespół niewydolności oddechowej, NIH – National Institutes of Health, NNT - number needed to treat, OR - iloraz szans, RB - korzyść względna, SARS-CoV (severe acute respiratory syndrome coronavirus) – zespół ciężkiej ostrej niewydolności oddechowej, SpO2 – wysycenie hemoglobiny tlenem mierzone za pomocą pulsoksymetru
Nadal nie dysponujemy leczeniem przyczynowym COVID-19 o udowodnionej skuteczności, a postępowanie zalecane w wielu lokalnych wytycznych uwzględnia stosowanie terapii eksperymentalnych, często na podstawie danych in silico lub in vitro, niepełnych obserwacji lub badań klinicznych budzących wiele zastrzeżeń metodologicznych.1 Rodzi to słuszne obawy o skuteczność i bezpieczeństwo terapii, a każde nowe badanie kliniczne, szczególnie z użyciem placebo w grupie kontrolnej, rozpala zainteresowanie środowiska medycznego i pacjentów czekających z nadzieją na przełom w leczeniu COVID-19.
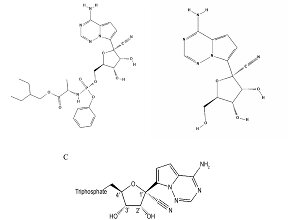
Remdesiwir (nazwa kodowa GS-5734) jest analogiem adenozyny, prolekiem ulegającym przekształceniu wewnątrz komórek do czynnego metabolitu o aktywności blokującej wirusową polimerazę RNA zależną od RNA, która jest konieczna do replikacji wielu wirusów RNA, w tym koronawirusów zespołu ciężkiej niewydolności oddechowej (SARS-CoV) i bliskowschodniego zespołu niewydolności oddechowej (MERS-CoV), co potwierdzono w badaniach in vitro i na zwierzętach.2-4 Opracowano ten lek pierwotnie w celu leczenia gorączki krwotocznej ebola, ale okazał się nieskuteczny podczas epidemii tej choroby w Demokratycznej Republice Konga w 2019 roku.5 Stwierdzono wówczas, że w postaci dożylnej był dobrze tolerowany.5 Na początku 2020 roku wykazano również, że remdesiwir hamuje replikację SARS-CoV-2 w hodowli komórek nabłonka błony śluzowej nosa lub oskrzeli oraz u małp nienaczelnych,6,7 co rozbudziło nadzieje na opracowanie skutecznej metody leczenia przyczynowego chorych na COVID-19.
Co wiedzieliśmy dotychczas o remdesiwirze w leczeniu chorych na COVID-19?
Pierwsze opisy przypadków i serii przypadków stosowania remdesiwiru w ramach programu rozszerzonego dostępu u chorych na COVID-19 sugerowały korzyść kliniczną u chorych w ciężkim stanie klinicznym.8 Na podstawie tych pierwszych danych, w sytuacji braku skutecznego swoistego leczenia przeciwwirusowego, remdesiwir uwzględniono w niektórych wytycznych opracowanych przez towarzystwa naukowe, w tym w zaleceniach Polskiego Towarzystwa Epidemiologów i Lekarzy Chorób Zakaźnych.9
W opublikowanych w drugiej połowie kwietnia br. wytycznych amerykańskich National Institutes of Health (NIH; p. także Med. Prakt. 5/2020: Leczenie COVID-19 – wytyczne National Institutes of Health (USA)) stwierdzono natomiast, że nie ma wystarczających danych klinicznych, na podstawie których można byłoby zalecić stosowanie albo niestosowanie remdesiwiru w leczeniu chorych na COVID-19, pozostawiając tym samym decyzję w indywidualnych przypadkach lekarzom (np. w ramach programu użycia humanitarnego).10 Natomiast wytyczne polskiej Agencji Oceny Technologii Medycznych i Taryfikacji były bardziej restrykcyjne – wobec braku wiarygodnych danych dotyczących skuteczności i bezpieczeństwa u chorych na COVID-19 nie zalecono rutynowego stosowania tego leku, ograniczając jego użycie do badań klinicznych.11
Wyniki pierwszego badania z randomizacją dotyczącego oceny remdesiwiru w leczeniu chorych na COVID-19 opublikowano w ostatnich dniach kwietnia br. w czasopiśmie „The Lancet”.12 Przeprowadzono je w Chinach, w 10 szpitalach w Wuhanie, obejmując nim dorosłych chorych na COVID-19 o ciężkim przebiegu, leczonych w szpitalu: 237 osób (randomizacja 2:1, 158 chorych otrzymało remdesiwir, 79 placebo) z potwierdzonym radiologicznie zapaleniem płuc, stosunkowo krótkim wywiadem chorobowym (<12 dni od pierwszych objawów), u których wyjściowo stwierdzono hipoksemię (wysycenie hemoglobiny tlenem zmierzone za pomocą pulsoksymetru [SpO2] <94% podczas oddychania powietrzem atmosferycznym lub stosunek ciśnienia parcjalnego tlenu we krwi tętniczej do frakcji tlenu wdychanego ≤300 mm Hg), a 82–83% z nich wymagało wyjściowo dodatkowego podawania tlenu. Remdesiwir stosowano przez 10 dni (pierwsza dawka 200 mg 1 × dz., następne 100 mg 1 × dz.), z możliwością podawania także innych leków przeciwwirusowych (lopinawir z rytonawirem – odpowiednio u 28% i 29% chorych; interferon α-2b – u 29% i 38% chorych) oraz glikokortykosteroidów (GKS; wyjściowo u odpowiednio 38% i 40% chorych, a w trakcie terapii u 65% i 68%). Poprawę kliniczną (zmniejszenie nasilenia choroby), ocenianą w 6-stopniowej skali klinicznej (1 – wypis ze szpitala; 6 – zgon), zdefiniowano jako zmniejszenie nasilenia choroby o ≥2 stopnie w stosunku do stanu wyjściowego lub wypis ze szpitala (jeśli nastąpił wcześniej), a obserwację chorych prowadzono przez 28 dni.
W badaniu nie wykazano, aby leczenie remdesiwirem znamiennie zmniejszyło ryzyko zgonu w ciągu 28 dni (odpowiednio 14% vs 13%; różnica bezwzględna ryzyka [ARD]: 1,1% [95% CI: od –8,1 do 10,3]), skróciło czas do uzyskania poprawy klinicznej (mediana: 21 vs 23 dni; HR: 1,23 [95% CI: 0,87–1,75]) lub zwiększyło szansę na zmniejszenie nasilenia choroby w 28. dniu (OR: 1,15 [95% CI: 0,67–1,96]). W podgrupie osób chorujących ≤10 dni przed rozpoczęciem leczenia zaobserwowano jednak trend w kierunku krótszego czasu do uzyskania poprawy klinicznej w grupie leczonej remdesiwirem (mediana: 18 vs 23 dni; HR: 1,52 [95% CI: 0,95–2,43]) oraz mniejszego ryzyka zgonu (11% vs 15%; ARD: –3,6% [95% CI: od –16,2 do 8,9]). Objawy niepożądane obserwowano z podobną częstością w obu grupach (66% vs 64%), ale leczenie remdesiwirem przerwano z powodu zdarzeń niepożądanych u 12% chorych (w porównaniu z 5% w grupie kontrolnej).