Tłumaczyła lek. Iwona Rywczak, redaktor „Medycyny Praktycznej – Szczepienia”
Skróty: ASD – zaburzenia ze spektrum autyzmu, HPV – ludzki wirus brodawczaka, MMR – szczepionka przeciwko odrze, śwince i różyczce, NOP – niepożądany odczyn poszczepienny, WZW – wirusowe zapalenie wątroby, ZGB – zespół Guillaina i Barrégo
Translated from Frank DeStefano, Heather Monk Bodenstab, Paul A. Offit; Principal Controversies in Vaccine Safety in the United States, Clinical Infectious Diseases, ciz135, https://doi.org/10.1093/cid/ciz135. Published by Oxford University Press. https://www.usa.gov/government-works
Streszczenie
Wątpliwości związane z bezpieczeństwem szczepień mogą doprowadzić do braku akceptacji takiej metody profilaktyki, zwiększając w ten sposób zapadalność na choroby, którym można zapobiegać poprzez szczepienia. W artykule podsumowano najważniejsze dane dotyczące kontrowersji wokół zagadnień związanych ze szczepieniami, do których należą: związek szczepionki MMR z autyzmem, tiomersal (środek konserwujący zawierający pochodną rtęci) a ryzyko zaburzeń neurorozwojowych, ZGB związany ze szczepieniem, szczepienia a choroby autoimmunizacyjne, bezpieczeństwo szczepionek przeciwko HPV, adiuwanty glinowe a choroby autoimmunizacyjne i inne zaburzenia oraz zbyt duża liczba szczepionek podanych we wczesnym okresie życia a zwiększenie ryzyka niekorzystnych następstw dla zdrowia i rozwoju dzieci. Wykazano, że szczepienie przeciwko grypie może nieznacznie zwiększać ryzyko wystąpienia ZGB, jednak jest ono mniejsze niż ryzyko ZGB po zakażeniu wirusem grypy. Poza tym dane z badań biologicznych i epidemiologicznych nie uzasadniają żadnej z omówionych w artykule wątpliwości na temat bezpieczeństwa szczepień.
Szczepienia ochronne są jednym z największych osiągnięć nowoczesnej medycyny i zdrowia publicznego. Dzięki opracowaniu bardzo skutecznych szczepionek i efektywnych programów szczepień udało się uodpornić istotny odsetek populacji, co z kolei pozwoliło zapobiec ogromnemu cierpieniu oraz wielu zgonom z powodu chorób, którym można zapobiegać poprzez szczepienia. Działanie to było tak skuteczne, że aktualnie wiele osób nigdy nie widziało niektórych chorób, ani nie spotkało się z nimi bezpośrednio. Stworzyło to warunki, w których na akceptację szczepień bardziej wpływa niepokój związany z możliwymi niepożądanymi odczynami poszczepiennymi (NOP). Obawy te przyczyniły się do zmniejszenia wskaźników wyszczepialności i nawrotu zachorowań, którym zapobiegamy dzięki szczepieniom. W niniejszym artykule podsumowano dane naukowe, które w opinii autorów najtrafniej odnoszą się do najważniejszych wątpliwości związanych ze szczepieniami (tab.), przede wszystkim pojawiających się w Stanach Zjednoczonych (ale także w Polsce, p. komentarz – przyp. red.). Artykuł nie jest kompleksowym przeglądem systematycznym danych o bezpieczeństwie szczepień. Nie omówiono w nim również znanych NOP, ani nie odniesiono się szczegółowo do metodyki, wiarygodności i ograniczeń opisanych badań.
| Tabela. Podsumowanie danych naukowych odnoszących się do wybranych wątpliwości na temat bezpieczeństwa szczepień | ||
|---|---|---|
| Problem | Zarzut | Dane naukowe |
| MMR a autyzm | MMR wywołuje autyzm | Pierwsze doniesienie sugerujące związek MMR z autyzmem wycofano z czasopisma, na łamach którego je opublikowało. Autyzm jest uwarunkowany genetycznie. Choroba zaczyna się rozwijać zanim dziecko osiągnie wiek, w którym zaleca się szczepienie MMR (12 mies.). W badaniach epidemiologicznych nie stwierdzono zwiększonego ryzyka autyzmu po szczepieniu MMR. |
| tiomersal | tiomersal – środek konserwujący zawierający związek rtęci obecny w niektórych szczepionkach, zwiększa ryzyko autyzmu i innych zaburzeń neurorozwojowych | Tiomersal zawiera etylortęć, która nie gromadzi się w organizmie przy kolejnych szczepieniach w ilości toksycznej. Pomimo wycofania tiomersalu ze szczepionek dla dzieci częstość występowania autyzmu nadal się zwiększa. W badaniach epidemiologicznych nie wykazano, aby podanie szczepionek zawierających tiomersal wiązało się ze zwiększonym ryzykiem autyzmu lub innych zaburzeń neurorozwojowych. |
| ZGB | szczepionki przeciwko grypie mogą być przyczyną ZGB | Zaobserwowano zwiększenie ryzyka po podaniu szczepionki przeciwko tzw. świńskiej grypie stosowanej w 1976 r. Wyniki badań dotyczących nowszych szczepionek przeciwko grypie sezonowej były zróżnicowane. W porównaniu ze szczepieniem, ryzyko ZGB jest większe po zakażeniu wirusem grypy. |
| autoimmunizacja | szczepionki mogą powodować przewlekłe choroby o podłożu autoimmunizacyjnym | Nie przedstawiono patomechanizmu, w jaki sposób szczepionki mogłyby wywołać chorobę autoimmunizacyjną. Wyniki badań epidemiologicznych nie potwierdzają hipotezy, że szczepionki są przyczyną chorób autoimmunizacyjnych. |
| bezpieczeństwo szczepionek przeciwko HPV | szczepienie przeciwko HPV może zwiększyć ryzyko różnych chorób, w tym autoimmunizacyjnych | W kilku dużych badaniach populacyjnych nie stwierdzono zwiększonego ryzyka chorób autoimmunizacyjnych lub chorób układu nerwowego po szczepieniu przeciwko HPV. W innych badaniach nie stwierdzono zwiększonego ryzyka przedwczesnej niewydolności jajników, zespołu tachykardii postawno-ortostatycznej lub kompleksowego zespołu bólu regionalnego. |
| glin | glin zawarty w szczepionkach może być przyczyną chorób autoimmunizacyjnych i innych zaburzeń, np. zespołu makrofagowego zapalenia mięśniowo-powięziowego | Stężenie glinu w surowicy po podaniu szczepionek zawierających glin jest znacznie mniejsze od wartości toksycznej. Nie stwierdzono zależności między stężeniem glinu we krwi lub włosach u niemowląt a przebytymi szczepieniami. Większa dawka adiuwantów zawierających glin podanych we wstrzyknięciu wiązała się z mniejszą zapadalnością na choroby autoimmunizacyjne. Nigdy nie ustalono, jakie objawy ogólnoustrojowe zespołu makrofagowego zapalenia mięśniowo-powięziowego są związane z solami glinu wykrywanymi w miejscu wstrzyknięcia. |
| zbyt dużo szczepionek w zbyt młodym wieku | podanie zbyt dużej liczby szczepionek we wczesnym okresie życia może przeciążyć układ odpornościowy i zwiększać ryzyko zaburzeń zdrowotnych oraz rozwojowych | Teoretycznie niemowlę może wytworzyć odpowiedź immunologiczną na 10 000 szczepionek podanych jednoczasowo. Szczepionki stosowane u dzieci nie powodują długotrwałych, dużych zmian w układzie odpornościowym. W badaniach epidemiologicznych nie stwierdzono zwiększonego ryzyka chorób lub zaburzeń rozwoju w zależności od liczby szczepionek lub antygenów szczepionkowych podanych we wczesnym okresie życia |
| HPV – ludzki wirus brodawczaka, ZGB – zespół Guillaina i Barrégo | ||
MMR a autyzm
Spekulacje, że szczepionka przeciwko odrze, śwince i różyczce (MMR) wywołuje autyzm były i nadal
są jedną z najbardziej szkodliwych kontrowersji
dotyczących bezpieczeństwa szczepień. W wielu
badaniach jednoznacznie udowodniono, że MMR
nie powoduje autyzmu, jednak niektórzy rodzice
nadal pytają o możliwy związek między tym
szczepieniem a autyzmem. Brak akceptacji szczepienia
MMR ze strony niektórych rodziców lub
większych grup społecznych doprowadził do ponownego
pojawienia się ognisk epidemicznych odry w Stanach Zjednoczonych i zwiększenia zachorowalności w Europie.
Sugestia, że MMR może być przyczyną autyzmu,
po raz pierwszy pojawiła się w artykule
opublikowanym w 1998 roku w czasopiśmie
„The Lancet”.1 Chociaż ostatecznie artykuł ten
usunięto z czasopisma z uwagi na nieprawidłowości w rekrutacji uczestników badania i finansowy
konflikt interesów,2 wątpliwości poruszone w tej
publikacji pozostały. W artykule opisano objawy
kliniczne u 12 dzieci z całościowym zaburzeniem
rozwoju (9 dzieci z autyzmem) oraz zaburzeniami
ze strony jelit (podejrzenie nieswoistego zapalenia
jelita grubego). Jedynym sugerowanym związkiem
ze szczepieniem MMR było zgłoszenie przez rodzica
lub lekarza zaostrzenia problemów behawioralnych w krótkim czasie po podaniu MMR u 8 dzieci.
Mimo swoich ograniczeń, publikacja przyciągnęła dużą uwagę mediów i opinii publicznej, czego skutkiem było zmniejszenie się wskaźników wyszczepialności
szczepionką MMR, szczególnie w Wielkiej Brytanii, a w dalszej kolejności nawrót
zachorowań na odrę i zgonów z tego powodu.
Autyzm jest zaburzeniem neurorozwojowym,
które w dużym stopniu zależy od czynników
genetycznych, a zaburzenia zaczynają się już w okresie prenatalnym. Zatem nie jest prawdopodobne,
aby ekspozycja po urodzeniu, w wieku
około 1 roku, kiedy na ogół podaje się MMR, mogła
wywołać autyzm. Niedługo po ukazaniu się artykułu w „The Lancet” opublikowano kilka badań
epidemiologicznych, w których nie potwierdzono
związku między autyzmem a szczepieniem MMR.
Pierwsze z nich ukazało się już w 1999 roku na łamach
„The Lancet”. W badaniu oceniono, czy wprowadzenie
szczepienia MMR w Wielkiej Brytanii w 1988 roku wpłynęło na zapadalność na autyzm.3
Autorzy nie stwierdzili nagłych zmian zapadalności
po rozpoczęciu programu szczepień, ani zależności
między otrzymaniem MMR a rozwojem
autyzmu. W badaniu retrospektywnym, w którym
wykorzystano dane z ewidencji ludności oraz z baz
systemu opieki zdrowotnej, analizą objęto wszystkie
dzieci (>500 000) urodzone w Danii w latach
1991–1998. Nie stwierdzono związku między wiekiem w momencie szczepienia MMR, czasem, jaki
upłynął od szczepienia lub datą wykonania szczepienia a rozwojem autyzmu.4 Z kolei w analizie
wykorzystującej główną bazę danych brytyjskich
placówek podstawowej opieki zdrowotnej porównano
pacjentów z autyzmem lub innym całościowym
zaburzeniem rozpoznanym w ciągu 28 lat z osobami w podobnym wieku, u których takich
zaburzeń nie stwierdzono. Nie stwierdzono związku
między MMR a ryzykiem autyzmu lub innego
całościowego zaburzenia rozwoju.5 W nieco później
opublikowanym badaniu oceniono, czy szczepienie
MMR jest czynnikiem ryzyka tylko u dzieci z grupy
zwiększonego ryzyka (p. Med. Prakt. Szczepienia 2/2015, str. 79–80 – przyp. red.).6 Badaniem
objęto około 100 000 dzieci, u których starszego
rodzeństwa rozpoznano zaburzenie ze spektrum
autyzmu (autism spectrum disorder – ASD). Autorzy
badania wyciągnęli wniosek, że szczepienie
MMR nie miało wpływu na zachorowanie u dzieci
zakwalifikowanych do grupy ryzyka ze względu
na rozpoznanie ASD u starszego rodzeństwa.
Zwiększonego ryzyka autyzmu po szczepieniu
MMR nie wykazano również w kilku innych badaniach,
które szczegółowo oceniła National Academy
of Medicine7 i uwzględniła w metaanalizie.8
Dane dobrej jakości wskazują więc, że MMR
nie wywołuje autyzmu.
Tiomersal a zaburzenia neurorozwojowe
Sugerowano, że tiomersal, środek konserwujący
zawierający związek rtęci, może zwiększać ryzyko
autyzmu. Rtęć jest naturalnym pierwiastkiem
obecnym w skorupie ziemskiej, powietrzu,
glebie i wodzie. Niektóre bakterie występujące w środowisku mogą zmieniać rtęć nieorganiczną w organiczną (metylortęć), która poprzez łańcuch
pokarmowy dostaje się do organizmów ryb, innych
zwierząt oraz ludzi i w przypadku dużego stężenia
wywołuje działanie neurotoksyczne. Opierając
się na standardach dla metylortęci, amerykański
Food and Drug Administration (FDA) stwierdził,
że ilość rtęci w szczepionkach podawanych
dzieciom do 6. miesiąca może przekraczać normy
bezpieczeństwa zalecane przez Environmental
Protection Agency w odniesieniu do metylortęci.
Należy jednak pamiętać, że tiomersal zawiera etylortęć, a nie metylortęć. Etylortęć ulega rozpadowi i wydaleniu z organizmu znacznie szybciej niż
metylortęć, dlatego prawdopodobieństwo akumulacji w ustroju człowieka i związanych z tym niekorzystnych
następstw jest znacznie mniejsze. Mimo
tego z programu szczepień dzieci obowiązującego w Stanach Zjednoczonych zapobiegawczo wycofano
szczepionki zawierające tiomersal. Aktualnie w Stanach Zjednoczonych jest dostępna tylko jedna
szczepionka zawierająca tiomersal jako środek
konserwujący – jest nią szczepionka przeciwko
grypie w fiolkach wielodawkowych (25 µg/dawkę
[niedostępna w Polsce; w Polsce jako konserwant
występuje tylko w DTPw – przyp. red.]). Powszechnie
dostępne są natomiast szczepionki przeciwko
grypie bez tiomersalu.
W metaanalizie kilku badań epidemiologicznych
nie wykazano zwiększonego ryzyka wystąpienia
autyzmu po szczepieniu preparatami zawierającymi
tiomersal.8 W dużym badaniu duńskim
oceniono zapadalność na autyzm w populacji dzieci
urodzonych w Danii w latach 1990–1996, które
otrzymały szczepionki zawierające tiomersal lub
takie same szczepionki, lecz bez tiomersalu. Zapadalność
na autyzm lub ASD nie różniła się znamiennie w obu grupach.9 W dużym badaniu kliniczno-kontrolnym
przeprowadzonym w Stanach
Zjednoczonych ekspozycja na tiomersal obecny w szczepionkach lub preparatach immunoglobulin
podanych w okresie prenatalnym (ciężarnej) lub
we wczesnym okresie życia dziecka nie zwiększyła
ryzyka ASD.10 Dostępne w Stanach Zjednoczonych
szczepionki zawierające tiomersal jako środek konserwujący
były ważne do 2003 roku (nie dotyczy
to wielodawkowych szczepionek przeciwko grypie) i od tego czasu nie są one już dostępne. Mimo to
liczba zachorowań na autyzm nadal się zwiększała w kolejnych latach.11 Na podstawie analizy dostępnych
danych Institute of Medicine (IOM) uznał, że
nie ma związku przyczynowego między tiomersalem
obecnym w szczepionkach a autyzmem.7
Odnosząc się do obaw związanych z autyzmem,
oceniono również, czy ekspozycja na tiomersal
może być przyczyną innych zaburzeń rozwojowych,
takich jak zaburzenia mowy lub trudności w uczeniu się. W badaniach nie stwierdzono
związku pomiędzy ekspozycją na tiomersal zawarty w szczepionkach a zaburzeniami neurorozwojowymi. W dużym badaniu brytyjskim oceniono zależność
między łączną dawką tiomersalu podaną w szczepionkach w pierwszych 6 miesiącach życia a różnymi parametrami rozwoju poznawczego oraz
behawioralnego w wieku 6–91 miesięcy, nie wykazując
niekorzystnego wpływu wczesnej ekspozycji
na tiomersal.12 Z kolei w amerykańskim badaniu
kohortowym dzieci w wieku 7–10 lat poddano
standaryzowanym testom w celu oceny związku
pomiędzy poziomem rozwoju neuropsychologicznego a ekspozycją na tiomersal w szczepionkach lub
preparatach immunoglobulin podanych w okresie
prenatalnym (ciężarnej), noworodkowym (0–28 dni) oraz pierwszych 7 miesięcy życia. Wyniki nie potwierdziły związku między narażeniem
na etylortęć we wczesnym okresie życia a zaburzeniami
neuropsychologicznymi w wieku 7–10 lat.13
Autorzy włoscy porównali natomiast rozwój neuropsychologiczny
dzieci, które 10 lat wcześniej losowo
przydzielono do dwóch grup otrzymujących
wraz ze szczepionkami różne dawki tiomersalu.
Chociaż wykazano kilka różnic, autorzy stwierdzili,
że mogą one być dziełem przypadku z uwagi
na dużą liczbę analiz statystycznych porównujących
poszczególne grupy (w zakresie kilkudziesięciu
parametrów – przyp. red.).14
Dostępne dane silnie przemawiają przeciwko
związkowi tiomersalu obecnego w szczepionkach
ze zwiększonym ryzykiem autyzmu lub innych
zaburzeń neurorozwojowych.
Szczepienia a zespół Guillaina i Barrégo
Zespół Guillaina i Barrégo (ZGB) jako możliwe
powikłanie szczepienia po raz pierwszy rozpoznano w Stanach Zjednoczonych w 1976 roku w okresie realizacji programu szczepień przeciwko
tzw. świńskiej grypie.15 Wtedy ryzyko ZGB
po tym szczepieniu szacowano na około 1/100 000 zaszczepionych osób. Od tego czasu związek pomiędzy szczepieniem przeciwko grypie a ZGB
jest ściśle monitorowany. Wyniki obserwacji są
zróżnicowane – w niektórych sezonach epidemicznych
stwierdzono zwiększenie ryzyka, a w innych
takiego wpływu nie wykazano. W metaanalizie
badań opublikowanych w latach 1981–2014 wykazano
1,4-krotnie większe względne ryzyko ZGB u osób zaszczepionych jakąkolwiek szczepionką
przeciwko grypie.16 W sezonach epidemicznych, w których zaobserwowano związek, ryzyko bezwzględne
wyniosło 1–2 dodatkowych zachorowań
na ZGB na milion zaszczepionych osób. Jednak w badaniach tych ryzyko oceniono w krótkim czasie
od szczepienia (zwykle w ciągu 42 dni). Zakażenie
wirusem grypy jest silniejszym czynnikiem
ryzyka ZGB niż szczepienie przeciwko grypie, dlatego w całym sezonie epidemicznym szczepienie
wiązało się ze zmniejszeniem ryzyka ZGB w wyniku
zapobiegania zachorowaniom na grypę.17
W badaniach oceniających inne szczepienia
stwierdzono, że szczepionki przeciwko: odrze,
śwince, różyczce (MMR), ludzkiemu wirusowi
brodawczaka (human papillomavirus – HPV), meningokokom
(skoniugowane), polio, pneumokokom,
ospie wietrznej, Haemophilus influenzae typu b
(Hib), wściekliźnie, tężcowi, błonicy, wirusowemu zapaleniu wątroby (WZW) typu A oraz WZW typu B nie zwiększają ryzyka wystąpienia ZGB.18
Podsumowując, w niektórych badaniach wykazano
związek pomiędzy ZGB a szczepieniem
przeciwko grypie, jednak ryzyko ZGB jest mniejsze
od ryzyka związanego z zakażeniem wirusem
grypy (p. Med. Prakt. Szczepienia 4/2013, str. 63 – przyp. red.).
Szczepienia a autoimmunizacja
Istnieją także obawy, że szczepienia mogą wywoływać
różne przewlekłe choroby autoimmunizacyjne.
Autoimmunizacja polega na wytworzeniu
odpowiedzi immunologicznej przeciwko własnym
antygenom. Od momentu urodzin działają mechanizmy
zapobiegające rozwojowi takiej odpowiedzi.
Układ odpornościowy zakłada powstawanie autoreaktywnych
limfocytów T i ma mechanizmy kontrolujące
ten proces. Nie opisano patomechanizmu, w jaki sposób szczepionki mogłyby się przyczyniać
do rozwoju chorób autoimmunizacyjnych.
W opublikowanych badaniach epidemiologicznych
oceniano związek między różnymi szczepionkami a chorobami przewlekłymi, o co najmniej
prawdopodobnym podłożu autoimmunizacyjnym. W rzetelnych badaniach epidemiologicznych
analizujących związek szczepionek stosowanych u niemowląt z cukrzycą typu 1 wykazano, że
szczepionka przeciwko odrze nie zwiększała ryzyka
zachorowania na cukrzycę. Inni autorzy nie
wykazali związku pomiędzy cukrzycą a szczepionkami
przeciwko gruźlicy (BCG), ospie prawdziwej,
tężcowi, krztuścowi, różyczce i śwince.19,20 W kilku
badaniach epidemiologicznych oceniono też,
czy szczepionki mogą wywoływać lub zaostrzać
przebieg stwardnienia rozsianego. W 2 dużych badaniach
kliniczno-kontrolnych nie zaobserwowano
związku pomiędzy szczepionką przeciwko WZW
typu B a stwardnieniem rozsianym.21,22 Nie wykazano
też, aby szczepionki przeciwko WZW typu B,
tężcowi lub przeciwko grypie zaostrzały przebieg
stwardnienia rozsianego.23 Jak opisano dalej, nie
potwierdzono też związku szczepionek przeciwko
HPV z chorobami autoimmunizacyjnymi.
Wyniki wielu badań wskazują, że szczepionki
nie zwiększają ryzyka wystąpienia chorób przewlekłych o możliwym podłożu autoimmunizacyjnym.
Bezpieczeństwo szczepionek przeciwko HPV
Szczepionki przeciwko HPV skupiły na sobie szczególną
uwagę mediów w związku z doniesieniami o różnych zdarzeniach niepożądanych, z których
wiele mogło mieć podłoże autoimmunizacyjne.
Szczegółowy nadzór prowadzony w Stanach Zjednoczonych i innych krajach przemawia jednak
za bezpieczeństwem szczepionek przeciwko HPV.
Najlepszej jakości dane na temat ryzyka wystąpienia
chorób autoimmunizacyjnych pochodzą między
innymi z dużego populacyjnego badania kohortowego
przeprowadzonego w Danii i Szwecji obejmującego
dziewczęta i kobiety, którym podano łącznie
>696 000 dawek 4-walentnej szczepionki przeciwko
HPV (HPV-4). Wyniki tego badania wskazują,
że szczepienie nie miało związku przyczynowego z różnymi chorobami autoimmunizacyjnymi i chorobami
układu nerwowego (p. Med. Prakt. Szczepienia
1/2014, s. 67–68 – przyp. red.).24 W dużym
badaniu kliniczno-kontrolnym przeprowadzonym
we Francji nie stwierdzono zwiększonego ryzyka
różnych zaburzeń autoimmunizacyjnych (pierwotnej
małopłytkowości immunologicznej [idiopathic
thrombocytopenic purpura – ITP], chorób demielinizacyjnych
ośrodkowego układu nerwowego,
ZGB, chorób zapalnych tkanki łącznej, cukrzycy
typu 1 i autoimmunizacyjnego zapalenia tarczycy)
po szczepieniu przeciwko HPV.25 W analizie
ogólnokrajowych danych ze Szwecji i Danii, obejmującej 4 miliony kobiet, w tym niemal 800 000
zaszczepionych HPV-4, nie wykazano zwiększonego
ryzyka stwardnienia rozsianego lub innej
choroby demielinizacyjnej po szczepieniu HPV-4
(p. Med. Prakt. Szczepienia 1/2015, s. 56 – przyp.
red.).26 Sugerowano również związek innych chorób
ze szczepionkami przeciwko HPV, jednak nie
znaleziono dowodów potwierdzających tę zależność.
Dotyczy to między innymi przedwczesnej
niewydolności jajników (p. Med. Prakt. Szczepienia
4/2018, s. 47–48 – przyp. red.),27 kompleksowego
zespołu bólu regionalnego i zespołu tachykardii
postawno-ortostatycznej.28
Dane pochodzące z różnych badań wskazują, że
szczepionki przeciwko HPV są bezpieczne.
Glin w szczepionkach
Glin w szczepionkach pełni rolę adiuwantu, który
ma wzmocnić odpowiedź immunologiczną. Sole
glinu są bezpiecznie stosowane jako adiuwanty
od lat 30. XX wieku. Obecnie glin zawierają
szczepionki przeciwko WZW typu B, WZW typu
A, błonicy i tężcowi, Hib oraz pneumokokom, natomiast
nie ma go w składzie „żywych” szczepionek
przeciwwirusowych, takich jak MMR, przeciwko
ospie wietrznej i rotawirusom. Badania wykazały,
że u dzieci szczepionych preparatami zawierającymi
glin stężenie glinu w surowicy jest znacznie
mniejsze od wartości toksycznej.29 Najlepszej jakości
dane na temat bezpieczeństwa glinu obecnego w szczepionkach stosowanych u dzieci pochodzą z niedawno opublikowanego badania obejmującego
dzieci w wieku 9–13 miesięcy, u których oznaczono
stężenie glinu we krwi i we włosach, a także przeanalizowano
historię szczepień oraz wyniki skal
oceny rozwoju poznawczego, ruchowego i rozwoju
mowy. Autorzy badania nie wykazali zależności
pomiędzy stężeniem glinu we krwi lub we włosach a przebytymi szczepieniami ani pomiędzy stężeniem
glinu we krwi a ogólnym poziomem rozwoju
dziecka.30
Szczególne obawy pojawiły się w odniesieniu
do możliwego związku adiuwantów glinowych z zespołem makrofagowego zapalenia mięśniowo-powięziowego
(macrophagic myofasciitis). Zaburzenie
to objawia się różnymi dolegliwościami
ogólnymi, a w badaniu wycinka mięśnia stwierdza
się bardzo małe obszary uszkodzenia zawierające
sole glinu.31 Nigdy jednak nie ustalono, jakie dolegliwości
ogólnoustrojowe są następstwem obecności
soli glinu w komórkach w miejscu wstrzyknięcia
szczepionki zawierającej glin.32
Shoenfeld i wsp. zaproponowali wyodrębnienie
tzw. zespołu autoimmunizacyjno-autozapalnego
wywołanego przez adiuwanty (autoimmune
autoinflammatory syndrome induced
by adjuvants – ASIA).33 Na razie zespół ten jest
jednak słabo opisany, obejmuje wiele nieswoistych i względnie częstych objawów (np. zmęczenie, bezsenność,
gorączkę).34 W badaniu, którym objęto
>18 000 pacjentów otrzymujących podskórnie
preparaty do alergenowej immunoterapii swoistej
zawierające adiuwanty glinowe w dużej dawce,
stwierdzono, że rzadziej zapadali oni na choroby
autoimmunizacyjne niż osoby z grupy kontrolnej.35
Aktualnie dostępne dane wskazują na bezpieczeństwo
adiuwantów glinowych zawartych w szczepionkach.
Zbyt dużo szczepionek w zbyt młodym wieku
Aktualny program powszechnych szczepień w Stanach Zjednoczonych uwzględnia 10 szczepionek
przeciwko 14 chorobom. Zgodie z nim
dzieci w pierwszych latach życia mogą otrzymać
do 26 dawek szczepionek w postaci wstrzyknięć, z których maksymalnie 5 można podać na jednej
wizycie. Niektórzy rodzice obawiają się, że zbyt
duża liczba szczepionek podanych w tak wczesnym
okresie życia może przeciążyć układ odpornościowy.
Biorąc pod uwagę liczbę krążących we krwi
limfocytów B, które produkują przeciwciała, liczbę
antygenów w szczepionkach, które otrzymuje
dziecko w pierwszych latach życia, oraz ilość przeciwciał,
jaka jest niezbędna do odpowiedzi na każdy
antygen, oszacowano, że niemowlę teoretycznie
może wytworzyć odpowiedź immunologiczną
na 10 000 szczepionek podanych podczas tej samej
wizyty.36 W badaniu oceniającym odpowiedź immunologiczną
na nieswoiste, nieszczepionkowe
bodźce u dzieci w wieku 3–5 lat, które otrzymały
wszystkie należne szczepienia lub nie były w ogóle
szczepione, stwierdzono, że szczepionki stosowane u dzieci nie powodują długotrwałych, dużych, niekorzystnych
zmian w układzie odpornościowym.37 W żadnym badaniu epidemiologicznym nie zaobserwowano
zwiększonego ryzyka chorób w zależności
od liczby szczepionek lub liczby antygenów
otrzymanych w dzieciństwie. W niedawno opublikowanym
badaniu amerykańskim nie wykazano
związku pomiędzy całkowitą liczbą antygenów lub
liczbą antygenów podanych w jednym dniu a ryzykiem
innych chorób infekcyjnych (tzn. innych
niż te, którym zapobiega szczepienie).38 W badaniu
oceniającym odległy wpływ na rozwój neuropsychologiczny u >1000 dzieci nie stwierdzono
zależności pomiędzy liczbą antygenów szczepionkowych podanych w okresie niemowlęcym a zaburzeniami rozwoju neuropsychologicznego w wieku
7–10 lat.39 I wreszcie, w dużym amerykańskim
badaniu kliniczno-kontrolnym oceniającym ekspozycję
na kumulacyjną dawkę antygenów w szczepionkach
lub maksymalną ekspozycję w jednym
dniu nie wykazano związku pomiędzy ekspozycją w pierwszych 2 latach życia a ryzykiem rozwoju
autyzmu lub różnych podtypów autyzmu.40
Układ odpornościowy niemowląt jest w pełni
zdolny do wytworzenia odpowiedzi na antygeny
zawarte w szczepionkach, a w badaniach nie wykazano
zwiększonego ryzyka niekorzystnych następstw
dla zdrowia w zależności od liczby szczepionek
lub zawartych w nich antygenów podanych
we wczesnym okresie życia.
Podsumowanie
W tym krótkim artykule podsumowano najbardziej trafne dane dotyczące niektórych częstych wątpliwości związanych z bezpieczeństwem szczepień, z którymi spotykają się lekarze podstawowej opieki zdrowotnej. Ponieważ celem tego artykułu nie był kompleksowy przegląd systematyczny, nie odniesiono się do wszystkich kontrowersji związanych z bezpieczeństwem szczepień, w tym wątpliwości podnoszonych w innych krajach. Nie omówiono również znanych NOP, które obecnie nie budzą szczególnych kontrowersji (np. anafilaksja po szczepieniu lub wgłobienie jelita po szczepieniu przeciwko rotawirusom). Autorzy mają nadzieję, że taki zwięzły format artykułu będzie przydatny dla zapracowanych lekarzy i pielęgniarek, a także innych osób zainteresowanych bezpieczeństwem szczepień. Bardziej szczegółowe informacje na temat tych i innych wątpliwości dotyczących bezpieczeństwa szczepień można znaleźć między innymi na stronach internetowych Vaccine Education Center utworzonych przez Children’s Hospital of Philadelphia (vaccine.chop.edu/safety-references) oraz Centers for Disease Control and Prevention (https://www.cdc.gov/vaccinesafety [p. także serwis https://www.mp.pl/szczepienia/ – przyp. red.]).
Oświadczenie: Stwierdzenia i wnioski przedstawione w tym artykule
reprezentują stanowisko autorów i nie stanowią jednocześnie
oficjalnego stanowiska Centers for Disease Control and Prevention.
Konflikt interesów: Żaden z autorów nie zgłosił potencjalnego
konfliktu interesów ani źródeł finansowania.
Piśmiennictwo:
1. Wakefield A.J., Murch S., Anthony A., et al.: RETRACTED: Ileal-lymphoid-nodular hyperplasia, non-specific colitis, and pervasive developmental disorder in children. Lancet, 1998; 351: 637–6412. Dyer C.: Lancet retracts Wakefield’s MMR paper. BMJ, 2010; 340: c696
3. Taylor B., Miller E., Farrington C.P., et al.: Autism and measles, mumps, and rubella vaccine: no epidemiological evidence for a causal association. Lancet, 1999; 353: 2026–2029
4. Madsen K.M., Hviid A., Vestergaard M., et al.: A population-based study of measles, mumps, and rubella vaccination and autism. N. Engl. J. Med., 2002; 347 (19): 1477–1482
5. Smeeth L., Cook C., Fombonne E., et al.: MMR vaccination and pervasive developmental disorders: a case-control study. Lancet, 2004; 364: 963–969
6. Jain A., Marshall J., Buikema A., et al.: Autism occurrence by MMR vaccine status among US children with older siblings with and without autism. JAMA, 2015; 313 (15): 1534–1540
7. Immunization Safety Review Committee. Immunization Safety Review. Vaccines and Autism Board of Health Promotion and Disease Prevention, Institute of Medicine (National Academy Press, Washington, DC, 2004)
8. Taylor L.E., Swerdfeger A.L., Eslick G.D.: Vaccines are not associated with autism: an evidence-based meta-analysis of case-control and cohort studies. Vaccine, 2014; 32: 3623–3629
9. Hviid A., Stellfeld M., Wohlfahrt J., et al.: Association between thimerosal-containing vaccine and autism. JAMA, 2003; 290: 1763–1766
10. Price C.S., Thompson W.W., Goodson B., et al.: Prenatal and infant exposure to thimerosal from vaccines and immunoglobulins and risk of autism. Pediatrics, 2010; 126: 656–664
11. Schechter R., Grether J.K.: Continuing increases in autism reported to California’s developmental services system: mercury in retrograde. Arch. Gen. Psychiatry, 2008; 65: 19–24
12. Heron J., Golding J., et al.: Thimerosal exposure in infants and developmental disorders: a prospective cohort study in the United Kingdom does not support a causal association. Pediatrics, 2004; 114 (3): 577–583
13. Thompson W.W., Price C., Goodson B., et al.: Early thimerosal exposure and neuropsychological outcomes at 7 to 10 years. N. Engl. J. Med., 2007; 357 (13): 1281–1292
14. Tozzi A.E., Bisiacchi P., Tarantino V., et al.: Neuropsychological performance 10 years after immunization in infancy with thimerosal-containing vaccines. Pediatrics, 2009; 123 (2): 475–482
15. Schonberger L.B., Bregman D.J., Sullivan-Bolyai J.Z., et al.: Guillain-Barre syndrome following vaccination in the National Influenza Immunization Program, United States, 1976–1977. Am. J. Epidemiol., 1979; 110: 105–123
16. Martin Arias L.H., Sanz R., Sainz M., Treceno C., Carvajal A.: Guillain-Barre syndrome and influenza vaccines: a meta-analysis. Vaccine, 2015; 33: 3773–3778
17. Vellozzi C., Iqbal S., Stewart B., Tokars J., DeStefano F.: Cumulative risk of Guillain-Barre syndrome among vaccinated and unvaccinated populations during the 2009 H1N1 influenza pandemic. Am. J. Public Health, 2014; 104: 696–701
18. Baxter R., Bakshi N., Fireman B., et al.: Lack of association of Guillain-Barre Syndrome with vaccinations. CID, 2013; 57 (2): 197–204
19. DeStefano F., Mullooly J.P., Okoro C.A., et al.: Childhood vaccinations, vaccination timing, and risk of type 1 diabetes mellitus. Pediatrics, 2001; 108: E112
20. Hviid A., Stellfeld M., Wohlfahrt J., Melbye M.: Childhood Vaccination and Type 1 Diabetes. N. Engl. J. Med., 2004; 350: 1398–1404
21. DeStefano F., Verstraeten T., Jackson L.A., et al.: Vaccinations and risk of central nervous system demyelinating diseases in adults. Arch. Neurol., 2003; 60: 504–509
22. Ascherio A., Zhang S.M., Hernan M.A., et al.: Hepatitis B vaccination and the risk of multiple sclerosis. N. Engl. J. Med., 2001; 344: 327–332
23. Confavreux C., Suissa S., Saddier P., et al.: Vaccinations and the risk of relapse in multiple sclerosis. N. Engl. J. Med., 2001; 344: 319–326
24. Arnheim-Dahlstrom L., Pasternak B., Svanstrom H., Sparen P., Hviid A.: Autoimmune, neurological, and venous thromboembolic adverse events after immunisation of adolescent girls with quadrivalent human papillomavirus vaccine in Denmark and Sweden: cohort study. BMJ, 2013; 347: f5906
25. Grimaldi-Bensouda L., Rossignol M., Kone-Paut I., et al.: Risk of autoimmune diseases and human papilloma virus (HPV) vaccines: six years of case-referent surveillance. J. Autoimmun., 2017; 19: 84–90
26. Scheller N.M., Svanstrom H., Pasternak B., et al.: Quadrivalent HPV Vaccination and Risk of Multiple Sclerosis and Other Demyelinating Diseases of the Central Nervous System. JAMA, 2015; 313 (1): 54–61
27. Naleway A.L., Mittendorf K.F., Irving S.A., et al.: Primary ovarian insufficiency and adolescent vaccination. Pediatrics, 2018; 142 (3): e20180943
28. European Medicines Agency Assessment Report. Human papilloma virus (HPV) vaccines. 11 November 2015; EMA/762033/2015 Pharmacovigilance Risk Assessment Committee (PRAC)
29. Mitkus R.J., King D.B., Hess M.A., et al.: Updated aluminum pharmacokinetics following infant exposures through diet and vaccination. Vaccine, 2011; 29: 9538–9543
30. Karwowski M.P., Stamoulis C., Wenren L.M., et al.: Blood and hair aluminum levels, vaccine history, and early infant development: a cross-sectional study. Acad. Pediatr., 2018; 18: 161–165
31. Gherardi R.K., Coquet M., Cherin P., et al.: Macrophagic myofasciitis lesions assess long-term persistence of vaccine-derived aluminium hydroxide in muscle. Brain, 2001; 124 (Pt 9): 1821–1831
32. Principi N., Esposito S.: Aluminum in vaccines: Does it create a safety problem? Vaccine, 2018; 36: 5825–5831
33. Shoenfeld Y., Agmon-Levin N.: ‘ASIA’ – autoimmune/inflammatory syndrome induced by adjuvants. J. Autoimmun., 2011; 36 (1): 4–8
34. Ameratunga R., Gills D., Gold M., et al.: Evidence refuting the existence of autoimmune/autoinflammatory syndrome induced by adjuvants (ASIA). J. Allergy Clin. Immunol. Pract., 2017; 5: 1551–1555
35. Linneberg A., Jacobsen R.K., Jespersen L., Abildstrom S.Z.: Association of subcutaneous allergen-specific immunotherapy with incidence of autoimmune disease, ischemic heart disease, and mortality. J. Allergy Clin. Immunol., 2012; 129: 413–419
36. Offit P.A., Quarles J., Gerber M.A., et al.: Addressing parents’ concerns: do multiple vaccines overwhelm or weaken the infant’s immune system? Pediatrics, 2002; 109 (1): 124–129
37. Sherrid A.M., Ruck C.E., Sutherland D., et al.: Lack of broad functional differences in immunity in fully vaccinated vs. unvaccinated children. Pediatr. Res., 2017; 81 (4): 601–608
38. Glanz J.M., Newcomer S.R., Daley M.F., DeStefano F., et al.: Association between estimated cumulative vaccine antigen exposure through the first 23 months of life and non-vaccine-targeted infections from 24 through 47 months of age. JAMA, 2018; 319 (9): 906–913
39. Iqbal S., Barile J.P., Thompson W.W, DeStefano F. Number of antigens in early childhood vaccines and neuropsychological outcomes at age 7-10 years. Pharmacoepidemiol Drug Saf. 2013; 22: 1263–1270
40. DeStefano F., Price C.S., Weintraub E.S. Increasing exposure to antibody-stimulating proteins and polysaccharides in vaccines is not associated with risk of autism. J. Pediatr. 2013; 163: 561–567
Komentarz
dr n. med. Jacek Mrukowicz
Redaktor naczelny „Medycyny Praktycznej – Szczepienia”, Polski
Instytut Evidence-Based Medicine w Krakowie
Autorzy komentowanego artykułu – uznani na świecie
eksperci od lat naukowo zajmujący się bezpieczeństwem
szczepień – w syntetycznej formie podsumowali aktualny
stan wiedzy na podstawie najistotniejszych badań klinicznych z grupą kontrolną, które przeprowadzono zgodnie z powszechnie przyjętą metodyką obiektywnej
analizy związków szczepień i zdarzeń niepożądanych.
Stworzyli zwięzłe kompendium podstawowych informacji
dla lekarzy praktyków, do wykorzystania w rozmowie z zaniepokojonymi rodzicami i pacjentami. Z artykułem
powinni się jednak zapoznać wszyscy pediatrzy, neonatolodzy,
lekarze rodzinni, położne i pielęgniarki, a także
specjaliści zdrowia publicznego i urzędnicy zajmujący się
programem szczepień ochronnych w Polsce.
Wiele badań cytowanych przez autorów artykułu szczegółowo
omawiano na łamach „Medycyny Praktycznej –
Szczepienia”. Zainteresowani szczegółami Czytelnicy
mogą skorzystać z wersji opracowanych w języku polskim (omówienia z komentarzami p. www.mp.pl/szczepienia/)
lub sięgnąć po oryginalne publikacje.
Bezpieczeństwo szczepień w erze globalizacji
Artykuł odnosi się do wątpliwości i zarzutów dyskutowanych w Stanach Zjednoczonych, jednak wszystkie
poruszone w nim problemy są aktualne także w Polsce. W dobie globalizacji, internetu i mediów społecznościowych
plotki o szczepieniach nie mają granic i rozchodzą
się w ciągu jednego do kilku dni po całym świecie. Z przeprowadzonej w 2012 roku przez UNICEF analizy polskiego
internetu wynika, że wśród plotek o szczepieniach dominowały 3 zagadnienia związane z: (1) „toksycznością”
szczepionek (m.in. sprawa zawartości tiomersalu, glinu i innych „toksycznych” dodatków) oraz brakiem potrzeby
szczepienia (aż 47%); (2) zdarzeniami niepożądanymi
po szczepieniu, w tym wynikającymi z hipotetycznego
„przeciążenia” układu odporności (28%); (3) zaburzeniami
rozwoju (m.in. autyzm, padaczka, zaburzenia neurorozwojowe
[15%]).1
Zdecydowana większość aktualnie stosowanych w Polsce szczepionek to produkty kilku globalnych producentów,
powszechnie używane w wielu krajach Unii
Europejskiej, Stanach Zjednoczonych, Kanadzie i innych
państwach na świecie. Wnioski z omówionych w artykule
badań znajdują więc praktyczne zastosowanie również u nas. Korzystamy w ten sposób dodatkowo z europejskich i północnoamerykańskich systemów nadzoru nad
bezpieczeństwem szczepień, które – dzięki ogromnym,
sprzężonym bazom danych – względnie szybko mogą
wykryć niepokojące sygnały o zwiększonej częstości
określonego zdarzenia niepożądanego po szczepieniu, a następnie w drugim etapie – metodą odpowiednich
badań epidemiologicznych – zweryfikować hipotezę o związku szczepienia (lub konkretnej szczepionki) z tym zdarzeniem niepożądanym.2,3 Jeśli hipoteza się
potwierdzi, w kolejnym etapie mogą także zdefiniować
najbardziej zagrożoną grupę pacjentów. To ważny argument w rozmowie z rodzicami dzieci i pacjentami zaniepokojonymi
pogłoskami, że „w Polsce właściwie nic
nie wiemy o NOP i bezpieczeństwie szczepień, bo nasz
system nie działa”.
Hierarchia dowodów w analizie związków przyczynowych
Kolejny zarzut, który często przewija się w opiniach
osób kontestujących bezpieczeństwo szczepień, dotyczy
„problemów metodologicznych” badań epidemiologicznych, a w związku z tym „generalnie małej wiarygodności”
tego rodzaju dowodów. Jako rzekomo bardziej wiarygodne
przedstawia się badania podstawowe (w tym
laboratoryjne, in vitro) wyjaśniające hipotetyczny patomechanizm
(dowody mechanicystyczne), pośrednio poparte
wybiórczo zestawianymi z nimi „w całość” opisami
przypadków i serii przypadków, argumentując „że każdy
człowiek jest inny, ... więc i odmiennie reaguje”. Tymczasem
dowody mechanicystyczne opierają się na mniej lub
bardziej prawdopodobnych hipotezach i teoriach patofizjologicznych
(czyli wyobrażeniach, jak to może działać w organizmie człowieka). W ogólnie przyjętej w wyjaśnianiu
związków przyczynowo-skutkowych hierarchii
tego typu dane są na samym początku (dole), albo – gdy
dotyczą wiarygodnego patomechanizmu, a wcześniejsze
mocne dowody epidemiologiczne wykazały, że ryzyko
zdarzenia jest rzeczywiście większe po szczepieniu – są
ostatnim stopniem na drodze do prawdy (ryc.).
Na szczęście wiemy, że – mimo pewnego zróżnicowania
reakcji między biologicznie odmiennymi, aczkolwiek
dającymi się zdefiniować grupami (subpopulacjami) pacjentów
– rządzą nimi pewne prawidłowości. To właśnie
odpowiednio zaplanowane badania epidemiologiczne są
powszechnie uznanym przez zdecydowaną większość
naukowców narzędziem wychwytywania takich prawidłowości
(związków) pomiędzy stosowaniem określonej
szczepionki a występowaniem zdarzeń niepożądanych
oraz – w razie ich stwierdzenia – dalszego wyjaśniania,
jaki one mają charakter (przyczynowo-skutkowy, przypadkowy,
powiązanie z rzeczywistym czynnikiem przyczynowym
itp.).4 Pozwalają także na badanie bardzo
dużych populacji, co jest konieczne do wykrycia bardzo
rzadko występujących potencjalnych zdarzeń niepożądanych.
Coraz częściej dostępne i coraz większe cyfrowe
bazy danych medycznych, a także rozwój komputerów o dużej mocy obliczeniowej ułatwiają takie badania i dostarczają nowych, mocnych dowodów w ocenie bezpieczeństwa
oraz skuteczności szczepień.
Nawet najlepiej zaplanowane badania epidemiologiczne
mają oczywiście swoje immanentne słabości i są narażone na różnego rodzaju błędy systematyczne,
ale dzięki przeprowadzaniu kilku różnych badań i analiz
według schematów odpornych na najistotniejsze z tych
błędów, a także dzięki różnym innym metodom kontroli
błędów systematycznych, wiarygodność zgodnych wyników
kilku badań klinicznych jest dużo większa (ryc.).
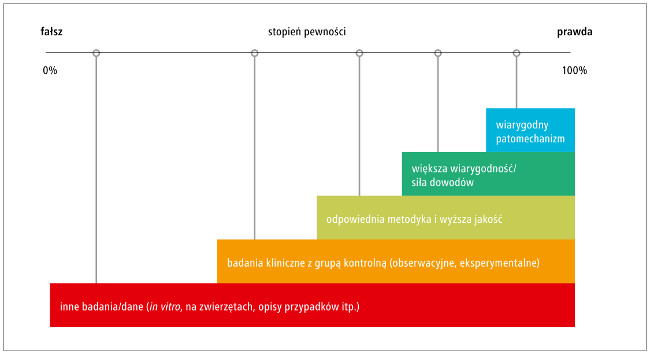
Ryc. Zasady wnioskowania o związkach przyczynowoskutkowych. Prawda i fałsz to nie system zero-jedynkowy, a szerokie spektrum zwiększającej się pewności w miarę gromadzenia większej liczby coraz bardziej wiarygodnych danych. Wiarygodne wyjaśnienie patomechanizmu jest dopiero ostatnim etapem, po wiarygodnym udokumentowaniu, że związek (powtarzalna prawidłowość) pomiędzy ekspozycją a skutkiem rzeczywiście istnieje.
Czego powinna nas uczyć historia kontrowersji wokół MMR?
Wspomniana w artykule historia MMR i autyzmu jest
doskonałą ilustracją problemów z publikacjami opartymi
wyłącznie na dowodach mechanicystycznych. Choć w samym głośnym artykule Wakefielda i wsp. z opisem
serii przypadków (później usuniętego z „The Lancet”) nie
było wzmianki, że przyczyną opisanych objawów u dzieci
mogło być szczepienie MMR, takie sugestie – lub wprost
wnioski – pojawiały się w wypowiedziach autora podczas
konferencji prasowych, wywiadów w mediach oraz
innych mniej lub bardziej formalnych spotkań. We wcześniejszych
publikacjach autor dowodził bowiem, że wykrył
obecność wirusa odry w wycinkach jelita grubego
chorych na chorobę Leśniowskiego i Crohna (czego nigdy
innym naukowcom stosującym prawidłowe metody nie
udało się potwierdzić), co było fundamentem jego hipotezy
(patomechanizmu), jak szczepienie MMR miało doprowadzać
do nieswoistego zapalenia jelita i autyzmu.5-7
Zarzut wobec MMR opierał się wyłącznie na wątpliwej,
słabo udokumentowanej hipotezie mechanicystycznej, a jednak – za sprawą tradycyjnych mediów, a później
internetu – zaczął żyć własnym życiem i do dziś zbiera
smutne żniwo, pomimo iż już w ciągu kilku lat od jego
nagłośnienia spójne dowody epidemiologiczne przemawiały
przeciwko tej hipotezie.7
W marcu 2019 roku, już po publikacji komentowanego
artykułu, ukazało się kolejne duże badanie kohortowe
duńskich autorów obejmujące populację 657 461 dzieci
urodzonych w latach 1999–2010, które obserwowano
średnio do >8. roku życia. Porównano w nim zapadalność
na autyzmu i zaburzenia ze spektrum autyzmu (z podziałem
na poszczególne rodzaje rozpoznań wg klasyfikacji
ICD-10) u dzieci zaszczepionych MMR (320 038 dzieci) i nieszczepionych tą szczepionką (31 619 dzieci), także z grupy ryzyka genetycznego, czyli rodzeństwa chorych
na autyzm.8 Autorzy
przeprowadzili bardzo szczegółowe analizy w zależności
od wielu czynników (oprócz obciążenia genetycznego,
m.in. inne wykonane szczepienia i liczba dawek),
nie znajdując żadnego związku między podaniem MMR i innych szczepionek zalecanych dla niemowląt a zachorowaniem
na autyzm. Ale czy te obserwacje zakończą
żywot plotki powtarzanej od niemal 21 lat?
Tiomersal i ... zmiana warty?
Tiomersal to związek o silnych właściwościach bakterio- i grzybobójczych dodawany w bezpiecznej dawce jako konserwant do niektórych szczepionek (w opakowaniach
wielodawkowych) w celu zapobiegania ich
skażeniu mikrobiologicznemu. Historia jego rzekomej
roli w etiologii autyzmu również zaczęła się od hipotez
mechanicystycznych opartych m.in. na doświadczeniach
in vitro przeprowadzonych w zupełnie niefizjologicznych
warunkach (m.in. w bardzo wysokiej temperaturze
niespotykanej u człowieka), ekstrapolacji informacji
dotyczących szkodliwości rtęci i metylortęci (mimo iż
tiomersal jest zupełnie innym związkiem chemicznym)
oraz dyskusji w mediach i zaangażowania polityków.9
Dodatkowo później przedstawiono także rzekome dowody
epidemiologiczne, które pochodziły z 3 publikacji
tych samych dwóch autorów i nie spełniały żadnego z 8
podstawowych kryteriów poprawności metodologicznej
(jakości, wiarygodności) stawianych epidemiologicznym
badaniom obserwacyjnym, w tym kryterium weryfikacji
ekspozycji i dawki tiomersalu faktycznie podanego w szczepionkach w dokumentacji lekarskiej dzieci.10
Tiomersal aktualnie znajduje się tylko w jednej ze stosowanych w Polsce szczepionek przeznaczonych dla dzieci w pierwszych latach życia – całokomórkowej szczepionce
przeciwko krztuścowi, błonicy i tężcowi (DTPw) polskiej
produkcji (w dawce 50 µg = 25 µg etylortęci/dawkę
DTPw) oraz w jej mniej skojarzonych pochodnych (DT).11
Wydaje się, że aktualnie w świetle spójnych i mocnych
dowodów epidemiologicznych przemawiających
za bezpieczeństwem szczepionek z tiomersalem u dzieci,
temperatura dyskusji wokół tego problemu zaczyna opadać. Z odwrotnym trendem możemy mieć do czynienia w przypadku glinu. Także i w tym przypadku narracja
jest jednak budowana według schematów opisanych
powyżej dla MMR i tiomersalu (dowody/hipotezy mechanicystyczne,
komentarze w mediach i internecie itp.),
włącznie z jego hipotetyczną rolą w etiologii autyzmu
(to najnowsza lansowana teoria). Lekarze powinni się
więc dobrze przygotować na coraz częstsze pytania i rozmowy na ten temat.
Jak rozmawiać o bilansie korzyści i ryzyka?
Decydującą rolę w podjęciu przez pacjentów i rodziców dzieci decyzji o szczepieniu nadal odgrywa zaufany lekarz, a często także pielęgniarka. Omówiony przez autorów komentowanego artykułu przykład związku zespołu Guillaina i Barrégo (ZGB) oraz szczepienia przeciwko grypie bardzo dobrze ilustruje zasadę, że – jeśli pacjenci mają mieć szansę na świadome podjęcie optymalnej decyzji – to o bezpieczeństwie szczepień i NOP należy rozmawiać tylko w kontekście podstawowych informacji o ryzyku zachorowania i konsekwencjach (w tym powikłaniach) choroby, której szczepienie zapobiega. Ryzyko ZGB po zachorowaniu na grypę jest bowiem kilkanaście razy większe niż po szczepieniu, a grypa występuje powszechnie.12 W dłuższej perspektywie (w tym przypadku cały sezon epidemiczny) ryzyko netto po szczepieniu jest mniejsze niż w razie rezygnacji z niego. Lekarz powinien umieć przedstawić rodzicom i pacjentom właśnie taką perspektywę, bo skupienie się wyłącznie na NOP przesłoni drugą stronę medalu, wypaczając obraz rzeczywistości.13,14 Wykazano, że rodzice, którzy mają rzetelne i aktualne informacje o chorobach, którym zapobiegają szczepienia, chętniej podejmują decyzję o szczepieniu swoich dzieci pomimo informacji o ryzyku ewentualnego NOP.13,14 Wielu wahających się rodziców do szczepienia dzieci przekonuje ostatecznie przykład lekarza, który z nimi nie tylko rozmawia o szczepieniach, ale też sam szczepi swoje dzieci, swoich bliskich i siebie zgodnie z zaleceniami, więc warto się taką informacją podzielić.14
Piśmiennictwo do komentarza:
1. Majewski S., Beger G.: Tracking antivaccination sentiment in Eastern European Social Media Networks. UNICEF, Division of Communication, Social and Civic Media Section. New York, 20132. Bonhoeffer J., Bentsi-Enchill A., Chen R.T. i wsp.: Guidelines for collection, analysis and presentation of vaccine safety data in pre- and postlicensure clinical studies. Vaccine, 2009; 27 (16): 2282–2288
3. Kramarz P.: Kompleksowe monitorowanie bezpieczeństwa szczepień. Med. Prakt. Szczep. 4/2012, s. 15–19 (www.mp.pl/szczepienia/specjalne/80836)
4. DeStefano F., Offit P., Fisher A.: Vaccine safety. (W:) Plotkin A.S., Orenstein A.W., Offit A.P. (red.): Vaccines. Wyd. 7, Elsevier, 2018: 1584–1600
5. Wakefield A.J., Pittilo R.M., Sim R. i wsp.: Evidence of persistent measles infection in Crohn’s disease. J. Med. Virol., 1993; 39: 345–353
6. Afzal M.A., Armitage E., Begley J. i wsp.: Absence of detectable measles virus genome sequence in inflammatory bowel disease tissues and peripheral blood lymphocytes. J. Med. Virol., 1998; 55: 243–249
7. Miller E.: Measles-Mumps-Rubella vaccine and the development of autism. Sem. Pediatr. Inf. Dis., 2003; 14 (3): 199–206
8. Hviid A., Hansen J.V., Frisch M., Melbye M.: Measles, mumps, rubella vaccination and autism: a nationwide cohort study. Ann. Intern. Med., 2019; doi: 10.7326/M18-2101
9. Offit. P.: Autism false prophets. Bad science, risky medicine, and the search for a cure. Columbia University Press, Nowy Jork, 2008 (ISBN: 978-0-231-14636-4)
10. Parker S.K., Todd J., Schwartz B., Pickering L.: Thimerosal-containing vaccines and autistic spectrum disorder: A critical review of published original data. Pediatrics, 2004; 114: 793–804
11. Mrukowicz J., Ściubisz M.: Czy szczepionki zawierają toksyczne składniki. www.mp.pl/szczepienia/ekspert/zagadnienia_rozne_ekspert/109630
12. Kwong J.C., Vasa P.P., Campitelli M.A. i wsp.: Risk of Guillain-Barré syndrome after seasonal influenza vaccination and influenza health-care encounters: a self-controlled study. Lancet, 2013; 13: 769–776
13. European Centre for Disease Prevention and Control. Let’s talk about protection – enhancing childhood vaccination uptake. Stockholm, ECDC, 2012 (https://ecdc.europa.eu/sites/portal/files/media/en/publications/Publications/lets-talk-about-protection-vaccination-guide.pdf)
14. Sobierajski T., Stryczyńska-Kazubska J., Małecka I., Mrukowicz J.: Medycy są z Marsa, a rodzice z… Facebooka. Czyli o sztuce skutecznej komunikacji w sprawie szczepień dzieci. Med. Prakt. Szczepienia WS 1/2018















