Skróty: DTPa – bezkomórkowa szczepionka przeciwko błonicy, tężcowi i krztuścowi, DTPw – całokomórkowa szczepionka przeciwko błonicy, tężcowi i krztuścowi
Mogłoby się wydawać, że powszechne szczepienia niemowląt przeciwko krztuścowi doprowadziły do wyeliminowania zachorowań na krztusiec w tej populacji. Niestety, nadal się je obserwuje. Warto się zatem dowiedzieć, jakie są prawdopodobne przyczyny tego zjawiska, ponieważ umożliwi to wdrożenie odpowiednich strategii zapobiegawczych.
Obraz kliniczny krztuśca u noworodków i młodych niemowląt
Pomimo postępu medycyny krztusiec u najmłodszych niemowląt ma ciężki przebieg. Choroba może nie wykazywać typowego trzyfazowego przebiegu (fazy nieżytowej, kaszlu napadowego, zdrowienia). Według klasycznego opisu opublikowanego w "Nelson Textbook of Pediatrics"[1] u niemowląt do 3. miesiąca życia:
1) faza nieżytowa trwa bardzo krótko i często nie jest zauważana
2) druga faza objawia się napadowymi problemami w oddychaniu w postaci "łapania" z trudem powietrza (gasp), krztuszenia się, a nawet bezdechu z zaczerwienieniem, zsinieniem twarzy pod wpływem różnych bodźców słuchowych, świetlnych, w czasie ssania, kąpieli lub przewijania; w tym okresie może również dochodzić do bardzo ciężkiego powikłania krztuśca – encefalopatii
3) okres rekonwalescencji trwa stosunkowo długo, a nadreaktywność oskrzeli utrzymuje się nawet kilkanaście miesięcy
4) opisywano także przypadki noworodkowego i wczesnoniemowlęcego krztuśca w postaci ciężkiego zapalenia oskrzelików i płuc[2] – wyniki badań autopsyjnych ujawniają w tych przypadkach zmiany martwicze w oskrzelikach, wewnątrzpęcherzykowe mikrokrwawienia i nacieki leukocytów w małych naczyniach tętniczych, żylnych, a także limfatycznych z obecnością wielu komórek Bordetella pertussis (obraz kliniczny odpowiadał ciężkiemu zapaleniu oskrzelików z nadciśnieniem płucnym).[3]
Epidemiologia
W Polsce powszechne szczepienia przeciwko krztuścowi szczepionką całokomórkową skojarzoną z anatoksyną tężcową i toksoidem błoniczym (DTPw) wprowadzono w latach 1960–1961 w odpowiedzi na epidemie krztuśca. W 1960 roku zanotowana prawie 100 000 zachorowań, a wskaźnik zapadalności wyniósł 300/100 000. Po blisko 20 latach realizacji programu szczepień, w 1989 roku w Polsce zanotowano łącznie 107 zachorowań na krztusiec, a zapadalność zmniejszyła się ponad 1000-krotnie do wartości 0,28/100 000. Było to możliwe dzięki bardzo skutecznej realizacji programu szczepień – 31 grudnia 2008 roku odsetek dzieci zaszczepionych przeciwko krztuścowi w 2. roku życia (a urodzonych w 2007 r.) wyniósł 99%.[4]
Mimo że szczepieniem przeciwkrztuścowym zarówno w Europie (szczepionką bezkomórkową – DTPa), jak i w Polsce (bezpłatnie szczepionką DTPw, a odpłatnie szczepionką DTPa) obejmuje się bardzo duży odsetek niemowląt, to nadal zdarzają się zachorowania wśród noworodków i młodych niemowląt.
Według oficjalnych danych z lat 1993–2004 w Stanach Zjednoczonych (National Notifiable Disease Surveillance System and the Supplemental Pertussis Surveillance System) liczba niemowląt do 2. miesiąca życia hospitalizowanych z powodu krztuśca utrzymywała się na podobnym poziomie. Natomiast dane z Nationwide Inpatient Sample and Kids' Inpatient Database wskazują, że wskaźnik ten jest 2–2,5 razy większy niż w przeszłości. W latach 2000–2003 z powodu krztuśca w Stanach Zjednoczonych hospitalizowano 2678 dzieci do ukończenia 1. roku życia, z czego 86% stanowiły niemowlęta do 3. miesiąca życia. Należy także wspomnieć, że aż 95% dzieci do 3. miesiąca życia wymagało sztucznej wentylacji.[5] Podkreśla się, że na krztusiec na ogół chorują niemowlęta nieszczepione lub nie w pełni zaszczepione. W Australii, pomimo dużego odsetka dzieci zaszczepionych szczepionką DTPa (95%), w 2001 roku hospitalizowano z powodu krztuśca 140 niemowląt (mediana wieku 8 tyg.); 69% z nich nie otrzymało ani jednej dawki szczepionki przeciwkrztuścowej. 6 W 68% przypadków do zarażenia doszło od jednego z rodziców (ryc.).[6]
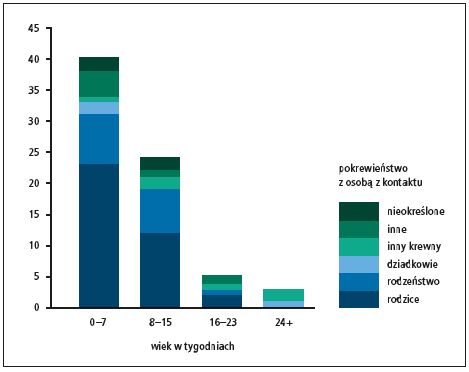
Ryc. Źródła zakażenia noworodków i młodych niemowląt w pierwszych tygodniach życia hospitalizowanych z powodu krztuśca (na podstawie 9. pozycji piśmiennictwa)
Dlaczego nie wszystkie małe dzieci są szczepione zgodnie z programem szczepień? Brakuje wiarygodnych danych pozwalających odpowiedzieć na to pytanie. Można przypuszczać, że odraczanie szczepień wiąże się z względnie dużą reaktogennością DTPw oraz zbyt liberalnym rozpoznawaniem przeciwwskazań do szczepienia przeciwko krztuścowi. W przypadku domniemanych przeciwwskazań do stosowania DTPw lub obaw dotyczących niepożądanych odczynów poszczepiennych często można zastosować DTPa. Przeszkodę mogą stanowić tylko możliwości finansowe rodziców, ponieważ szczepionka ta jest odpłatna. W takich sytuacjach niekiedy podejmuje się decyzję o odroczeniu szczepienia. W przypadku uzasadnionych względnych przeciwwskazań do podania DTPw (ale nie do szczepienia przeciwko krztuścowi) polski Program Szczepień Ochronnych daje możliwość bezpłatnego zastosowania DTPa. Znaczenie może mieć również nasilająca się działalność ruchów antyszczepionkowych. Obserwacje z Kolorado w Stanach Zjednoczonych wskazują, że dzieci, których rodzice odmawiali szczepień, były narażone na kilkunastokrotnie większe ryzyko zachorowania na krztusiec niż dzieci zaszczepione. Wykazano także, że odporność zbiorowiskowa (herd immunity) nie chroni w pełni przed zachorowaniami na krztusiec.[7]
W przypadku niemowląt i małych dzieci niekompletnie zaszczepionych zagrożenie stanowi kontakt z chorym na krztusiec przed wytworzeniem pełnej ochrony poszczepiennej (ryc.). Zwiększenie skuteczności programów kontroli krztuśca wymaga więc zastosowania dodatkowych strategii profilaktyki, ograniczających rezerwuar bakterii w populacji. Od początku lat 90. XX wieku w Polsce rejestruje się coraz więcej zachorowań na krztusiec, szczególnie u dzieci po 5. roku życia, u młodzieży i dorosłych. Przyczyną zwiększenia liczby zachorowań w tej grupie wiekowej może być zanikanie odporności poszczepiennej po kilku latach, a także pojawienie się mutacji szczepów Bordetella różniących się antygenowo od szczepów zastosowanych do produkcji szczepionki, w tym Bordetella parapertussis i Bordetella bronchoseptica. Podobną tendencję zaobserwowano w Niemczech, w innych krajach europejskich oraz w Stanach Zjednoczonych i Japonii.[8,9]
W Polsce w 2007 roku zgłoszono 1987 zachorowań na krztusiec, a w 2008 roku 2164 przypadki, zapadalność wynosiła zatem odpowiednio 5,21/100 000 i 5,68/100 000. Biorąc pod uwagę fakt, że hospitalizacji wymagała prawie połowa chorych (odpowiednio 47 i 41%), można przypuszczać, że dane epidemiologiczne dotyczące zachorowań na krztusiec są niedoszacowane.[4] Większość nowych zachorowań dotyczy dzieci po 5. roku życia i dorosłych, krztusiec przestał więc być typową chorobą małych dzieci. Należy zaznaczyć, że krztusiec u dotychczas zdrowych dzieci starszych i u dorosłych przebiega łagodniej niż u niemowląt i małych dzieci. Łagodniejszy przebieg krztuśca, przypominający inne powszechne zakażenia układu oddechowego (jednak często z długo utrzymującym się i męczącym kaszlem), sprawia, że często pozostaje on nierozpoznany, a chore osoby stanowią rezerwuar bakterii w populacji.
Jeżeli uda się zapobiec występowaniu krztuśca u starszych dzieci, młodzieży i dorosłych, to nie tylko zmniejszymy obciążenia zdrowotne w tej populacji, ale również – a może przede wszystkim – wyeliminujemy główne źródło zakażeń noworodków i małych niemowląt. Z tych powodów postuluje się wprowadzenie powszechnego szczepienia przeciwko krztuścowi młodzieży i dorosłych.[10]
Podsumowanie
W celu wyeliminowania zachorowań na krztusiec u niemowląt należy:
1) przede wszystkim zapewnić sprawne i kompletne szczepienie przeciwko krztuścowi całej populacji w tej grupie wiekowej
2) dodatkowo wprowadzić szczepienie przypominające przeciwko krztuścowi dla młodzieży i dorosłych w celu ograniczenia rezerwuaru bakterii w populacji oraz pośredniej ochrony dzieci, u których szczepienie jest przeciwwskazane lub u których ze względu na młody wiek jeszcze nie rozwinęła się pełna ochrona poszczepienna.
Piśmiennictwo
1. Long S.S.: Pertussis (Bordetella pertussis and Bordetella parapertussis). Kliegman, Berman, Jenson, Santon, Nelson Textbook of Pediatrics, 18/e Online, 2010
2. Nakamura A., Sakano T., Nakayama T. i wsp.: Neonatal pertussis presenting as acute bronchiolitis: direct detection of the Bordetella pertussis genome using loop-mediated isothermal amplification. Eur. J. Pediatr., 2009; 168: 347–349
3. Paddock C.D., Sanden G.N., Cherry J.D. i wsp.: Pathology and pathogenesis of fatal Bordetella pertussis infection in infants. Clin. Infect. Dis., 2008; 47: 328–338
4. Czarkowski M.P., Cielebak E ., Kondej B., Staszewska E .: Choroby zakaźne i zatrucia w Polsce w 2008 roku. Warszawa, Narodowy Instytut Zdrowia Publicznego Państwowy Zakład Higieny, Zakład Epidemiologii, Główny Inspektorat Sanitarny, Departament Przeciwepidemiczny, 2009
5. Cortese M.M., Baughman A.L., Hang R. i wsp.: Pertussis hospitalizations among infants in the United States, 1993 to 2004. Pediatrics, 2008; 121: 484–492
6. Elliott E., McIntyre P., Ridley G. i wsp.: National study of infants hospitalized with pertussis in the acellular vaccine era. Pediatr. Infect. Dis. J., 2004; 23: 246–252
7. Glanz J.M., McClure D.L., Magid D.J. i wsp.: Parental refusal of pertussis vaccination is associated with an increased risk of pertussis infection in children. Pediatrics, 2009; 123: 1446–1451
8. Hillebrand W., Beier D., Jansen E. i wsp.: The epidemiology of pertussis in Germany: past and present. BMC Infect. Dis., 2009; 9: 1–11
9. Kimura M., Kuno-Sakai H., Kunita N. i wsp.: Epidemiology of pertussis and studies on culture positive pertussis cases in Japan. Kansenshogaku Zasshi, 1996; 70: 19–28
10. Elliott E., Mcintyre P., Ridley G. i wsp.: National study of infants hospitalized with pertussis in the acellular vaccine era. Pediatr. Infect. Dis. J., 2004; 23: 246–252















