Konsultowała prof. dr hab. med. Waleria Hryniewicz, Zakład Epidemiologii i Mikrobiologii Klinicznej Narodowego Instytutu Leków w Warszawie
Skróty: ACIP – Advisory Committee on Immunization Practices, aOR – iloraz szans z uwzględnieniem poprawki na znane czynniki zakłócające, GKS – glikokortykosteroidy, IChP – inwazyjna choroba pneumokokowa, PCV – szczepionka skoniugowana przeciwko pneumokokom, POChP – przewlekła obturacyjna choroba płuc, PPSV-23 – 23-walentna polisacharydowa szczepionka przeciwko pneumokokom
Inwazyjna choroba pneumokokowa (IChP), tzn. bakteriemia, zapalenie opon mózgowo-rdzeniowych lub obecność Streptococcus pneumoniae w innej tkance lub w płynie ustrojowym jałowym w warunkach fizjologicznych, jest jedną z ważniejszych przyczyn zachorowań i zgonów w Stanach Zjednoczonych (także w Polsce – przyp. red.).1,2
Niniejszy dokument jest aktualizacją zaleceń amerykańskiego Komitetu Doradczego ds. Szczepień (Advisory Committee on Immunization Practices – ACIP) dotyczących zapobiegania IChP poprzez szczepienie 23-walentną polisacharydową szczepionką przeciwko pneumokokom (PPSV-23):
PPSV-23 jest skuteczna w zapobieganiu IChP i zapaleniu płuc, ale dostępne dane wskazują, że zapewniany przez nią poziom ochrony przed innymi rodzajami zakażeń pneumokokowych jest znacznie mniejszy.
Zaktualizowane zalecenia zawierają następujące zmiany w stosunku do wytycznych ACIP z 1997 roku:2
Zalecenie dotyczące podawania dawek przypominających (rewakcynacji) pacjentom z grup dużego ryzyka IChP (np. osobom bez śledziony lub z jej upośledzoną czynnością, osobom w stanie immunosupresji) pozostaje niezmienione.2 Wytyczne ACIP dotyczące profilaktyki IChP u niemowląt, dzieci i młodzieży do 18. roku życia włącznie poprzez stosowanie szczepionek skoniugowanych przeciwko pneumokokom (PCV) i/lub PPSV-23 opublikowano w osobnym dokumencie (podsumowanie: p. ramka 2. – przyp. red.).3 (...)
Streptococcus pneumoniae, inwazyjna choroba pneumokokowa i inne zakażenia pneumokokowe
Streptococcus pneumoniae (pneumokok) jest bakterią wywołującą choroby zarówno u dzieci, jak i dorosłych na całym świecie. Jest jednym z głównych zakaźnych czynników chorobotwórczych u małych dzieci. Wywołuje poważne zachorowania, prowadzące nawet do zgonu, także u osób w podeszłym wieku oraz u pacjentów (bez względu na wiek) obciążonych dodatkowymi czynnikami ryzyka medycznego. Pneumokok kolonizuje błonę śluzową górnych dróg oddechowych i może wywołać:
Przed wprowadzeniem powszechnych szczepień niemowląt przeciwko pneumokokom każdego roku w Stanach Zjednoczonych zakażenie pneumokokowe było przyczyną 3000 przypadków zapalenia opon mózgowo-rdzeniowych, 50 000 przypadków bakteriemii, 500 000 zachorowań na zapalenie płuc oraz 7 milionów przypadków – w zdecydowanej większości u dzieci – zapalenia ucha środkowego.4-7
Ciężkie zakażenie pneumokokowe jest następstwem rozsiewu bakterii drogą krwi lub ich penetracji do ośrodkowego układu nerwowego. Wyniki badań populacyjnych przeprowadzonych w Stanach Zjednoczonych przed wprowadzeniem programu powszechnych szczepień niemowląt przeciwko pneumokokom wskazywały, że wskaźnik zapadalności ogólnej na bakteriemię pneumokokową wynosił 1530/100 000/rok, a był znacznie większy wśród osób po 64. roku życia (5083/100 000/rok) oraz dzieci w pierwszych 2 latach życia (160/100 000/rok).8-12
U dorosłych 60–87% przypadków bakteriemii pneumokokowej towarzyszy zapaleniu płuc,13-15 natomiast u małych dzieci zazwyczaj nie udaje się zidentyfikować pierwotnego ogniska zakażenia. Oszacowano, że w Stanach Zjednoczonych przed wprowadzeniem powszechnych szczepień niemowląt przeciwko pneumokokom zachorowalność na pneumokokowe zapalenie opon mózgowo-rdzeniowych wynosiła 12/100 000/rok.16 Wskaźnik ten jest najwyższy u dzieci w wieku 6–24 miesięcy oraz osób po 64. roku życia. Ryzyko zachorowania u osób rasy czarnej jest 2-krotnie większe w porównaniu z rasą białą i latynoską. (...)
Streptococcus pneumoniae jest najczęstszą przyczyną pozaszpitalnego bakteryjnego zapalenia płuc, które głównie występuje u osób w wieku podeszłym i małych dzieci. Ze względu na niezadowalającą czułość i swoistość metod diagnostycznych dostępnych w rutynowej praktyce trudno jest dokładnie ocenić zapadalność na pneumokokowe zapalenie płuc. Niemniej oszacowano, że przed wprowadzeniem powszechnych szczepień niemowląt przeciwko pneumokokom w Stanach Zjednoczonych co roku występowało co najmniej 500 000 przypadków zachorowań, a pośród osób hospitalizowanych z powodu bakteryjnego zapalenia płuc zakażenie pneumokokowe odpowiadało za 25–35% przypadków.17-20 U dorosłych bakteriemia towarzyszy 10–25% zachorowań na pneumokokowe zapalenie płuc.18-21 (...)
Umieralność i śmiertelność
Oszacowano, że przed erą powszechnych szczepień niemowląt i małych dzieci przeciwko pneumokokom ciężkie zakażenia pneumokokowe co roku były w Stanach Zjednoczonych przyczyną zgonu 40 000 osób.4,5,22 To największa liczba pośród wszystkich chorób bakteryjnych, którym można zapobiegać poprzez szczepienia.23 Prawie 50% tych zgonów można byłoby zapobiec poprzez szczepienia. Śmiertelność jest największa u chorych na pneumokokowe zapalenie opon mózgowo-rdzeniowych i chorych z bakteriemią pneumokokową, a największe współczynniki umieralności z powodu zakażeń pneumokokowych notuje się u osób w podeszłym wieku oraz pacjentów obciążonych dodatkowymi czynnikami ryzyka medycznego (np. niektóre choroby przewlekle – p. dalej). U dzieci zgon z powodu zakażenia pneumokokowego zdarza się względnie rzadko, z wyjątkiem: 1) chorych na zapalenie opon mózgowo-rdzeniowych; 2) pacjentów z niedoborem odporności; 3) pacjentów po usunięciu śledziony z ciężką (piorunującą) bakteriemią pneumokokową. Pomimo odpowiedniego leczenia antybiotykami oraz nowoczesnych metod intensywnej terapii śmiertelność w przebiegu bakteriemii pneumokokowej u dorosłych wynosi 15–20%, a u osób w podeszłym wieku aż 30–40%.8-10,16,24-26 W jednym z opublikowanych badań śmiertelność z powodu bakteriemii pneumokokowej u dorosłych mieszkańców ubogich dzielnic miejskich, hospitalizowanych z tego powodu, oceniono na 36%.15
Zmiana epidemiologii po wprowadzeniu powszechnych szczepień niemowląt przeciwko pneumokokom
Od czasu wprowadzenia w Stanach Zjednoczonych w 2000 roku programu powszechnych szczepień niemowląt i małych dzieci 7-walentną szczepionką skoniugowaną przeciwko pneumokokom (PCV-7), znacznie zmniejszyły się wskaźniki zapadalności i umieralności z powodu IChP, także – w wyniku pośredniego efektu tzw. odporności zbiorowiskowej – wśród osób w starszych grupach wiekowych nie objętych szczepieniem, w tym po 65. roku życia (w Polsce szczepienie niemowląt i dzieci przeciwko pneumokokom nie jest obowiązkowe i powszechne – przyp. red.).27 Dane z programu aktywnego nadzoru epidemiologicznego nad zakażeniami bakteryjnymi Centers for Disease Control and Prevention (Active Bacterial Core surveillance [ABCs] – więcej informacji na stronie: http://www.cdc.gov/abcs/index.html) wskazują, że do 2007 roku zapadalność ogólna na IChP w całej populacji zmniejszyła się o 45% (z 24,4 do 13,5/100 000/rok) w porównaniu z latami 1998–1999 poprzedzającymi wprowadzenie programu powszechnych szczepień małych dzieci PCV-7.27 Wśród osób w wieku 18–49 lat, 50–64 lat oraz po 65. roku życia zapadalność zmniejszyła się odpowiednio o 40%, 18% i 37%. Ta redukcja w 87–92% była wynikiem ograniczenia liczby przypadków wywołanych zakażeniem pneumokokiem należących do typu serologicznego, który uwzględniono w PCV-7.27 Pomimo istotnych bezpośrednich i pośrednich efektów programu powszechnych szczepień małych dzieci szczepionką PCV-7, IChP nadal jest ważną przyczyną chorobowości i zgonów. Oszacowano, że w Stanach Zjednoczonych w 2009 roku wystąpiło ogółem 43 500 zachorowań na IChP i 5000 zgonów z tego powodu, ale aż 84% przypadków IChP i niemal wszystkie zgony dotyczyły dorosłych.1
Istnieje nadzieja, że dodatkowy efekt pośredni w postaci redukcji zachorowań u dorosłych będzie wynikiem pełnego wdrożenia rozpoczętego w Stanach Zjednoczonych w 2010 roku programu powszechnych szczepień niemowląt i małych dzieci skoniugowaną szczepionką 13-walentną (PCV-13).3 Trudno jednak przewidzieć wielkość tego efektu.3 W 2008 roku pneumokoki należące do typów serologicznych uwzględnionych w PCV-13 wywołały u osób w wieku 18–49 lat, 50–64 lat oraz po 65. roku życia odpowiednio 53%, 49% i 44% przypadków IChP zgłoszonych w Stanach Zjednoczonych, natomiast te uwzględnione w PPSV-23 odpowiednio 78%, 76% i 66% (ryc. 1.).
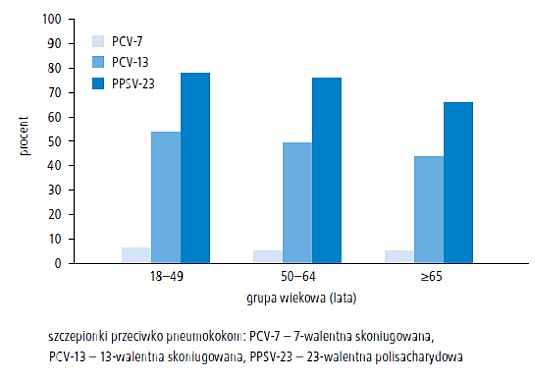
Ryc. 1. Odsetek. zachorowań na inwazyjną chorobę pneumokokową (IChP) u dorosłych w Stanach Zjednoczonych (w 2008 r., 8 lat po wprowadzeniu powszechnych szczepień niemowląt i małych dzieci PCV-7) w zależności od wieku wywołanych przez typy serologiczne pneumokoka uwzględnione w trzech różnych rodzajach szczepionek przeciwko pneumokokom (PCV-7, PCV-13, PPSV-23) na podstawie danych z programu aktywnego nadzoru epidemiologicznego nad zakażeniami bakteryjnymi Centers for Disease Control and Prevention
Czynniki ryzyka inwazyjnej choroby pneumokokowej
Zapadalność na choroby wywołane przez pneumokoki różni się w poszczególnych grupach demograficznych, i jest największa wśród niemowląt, małych dzieci (tzn. do 5. rż., a zwłaszcza do 2. rż. – przyp. red.) oraz u osób w podeszłym wieku (po 65. rż. – przyp. red.). Ryzyko zakażenia pneumokokowego i jego powikłań jest również zwiększone w każdym wieku u osób z dodatkowymi czynnikami ryzyka wynikającymi ze stanu ich zdrowia (niektóre choroby przewlekłe, wady; p. tab. 1).2 Cukrzycy zazwyczaj towarzyszy upośledzenie czynności układu sercowo-naczyniowego i/lub nerek, co zwiększa ryzyko ciężkiego zakażenia pneumokokowego. Ryzyko IChP jest największe wśród pacjentów z wrodzonymi lub nabytymi niedoborami odporności (w tym m.in. z nieprawidłowymi mechanizmami obrony nieswoistej, zakażeniem ludzkim wirusem niedoboru odporności [HIV]) oraz z czynnościowym lub anatomicznym brakiem śledziony (np. w niedokrwistości sierpowatokrwinkowej, we wrodzonym braku śledziony lub po jej wycięciu).28 Pacjenci z tej ostatniej grupy mają upośledzony mechanizm eliminacji bakterii otoczkowych z krwi, co zwiększa ryzyko piorunującej posocznicy pneumokokowej, obarczonej dużą śmiertelnością. Przed erą powszechnego profilaktycznego stosowania penicyliny, dzieci z niedokrwistością sierpowatokrwinkową 600 razy częściej chorowały na pneumokokowe zapalenie opon mózgowo-rdzeniowych niż ich rówieśnicy z prawidłową czynnością śledziony.22
Tabela 1. Wskazania ze względu na stan zdrowia do szczepienia dziecia po 24. miesiącu życia i dorosłych przeciwko pneumokokom 23-walentną szczepionką polisacharydową (PPSV-23)
| Grupa ryzyka | Choroba przewlekła lub inny czynnik ryzyka |
| osoby immunokompetentne | przewlekłe choroby sercab (z wyjątkiem nadciśnienia tętniczego)
przewlekłe choroby płucc cukrzyca wyciek płynu mózgowo-rdzeniowegod wszczepiona proteza ślimaka choroba alkoholowa przewlekłe choroby wątroby (w tym marskość) palenie papierosów |
| brak śledziony (anatomiczny lub czynnościowy)e | niedokrwistość sierpowatokrwinkowa i inne hemoglobinopatie
wrodzony lub nabyty brak śledziony (w tym stan po wycięciu śledziony) dysfunkcja śledziony |
| niedobory odpornoście | wrodzone i nabyte niedobory odpornościf
zakażenie HIV przewlekła niewydolność nerek zespół nerczycowy białaczki, chłoniaki (w tym chłoniak Hodgkina), szpiczak mnogi inne nowotwory złośliwe w stadium uogólnienia choroby wymagające leczenia immunosupresyjnego (w tym długotrwałego stosowania glikokortykosteroidów ogólnie lub radioterapii) przeszczepienie narządu miąższowego |
|
a Dzieci do ukończenia 5. rż. należy najpierw zaszczepić szczepionką skoniugowaną przeciwko
pneumokokom (PCV) zgodnie z aktualnymi zaleceniami, a dopiero w drugim etapie podać im
PPSV-23.
b w tym zastoinowa niewydolność serca i kardiomiopatie c w tym przewlekła obturacyjna choroba płuc, rozedma, astma (w każdym przypadku u dorosłych, a u dzieci w wieku od 24. mż. do 18. rż., gdy leczona doustnymi GKS w dużej dawce) d w wyniku wad wrodzonych czaszki, złamania kości czaszki, zabiegu neurochirurgicznego (może być przyczyną nawracającego pneumokokowego zapalenia opon mózgowo-rdzeniowych) e zaleca się drugą dawkę PPSV-23 po 5 latach od pierwszej f w tym zależne od limfocytów B (niedobory humoralne) lub T (niedobory komórkowe), niedobory składowych układu dopełniacza (zwłaszcza C1, C2, C3 lub C4) i zaburzenia fagocytozy (z wyjątkiem przewlekłej choroby ziarniniakowej) | |
W Stanach Zjednoczonych odsetek chorych na IChP, u których występowały predysponujące czynniki zdrowotne, zwiększył się od lat 1998–1999 do 2006–2007 z 52% do 59% w populacji w wieku 18–64 lat, a z 69% do 81% u osób po 64. roku życia. Ten trend sugeruje, że osoby, które ze względu na stan zdrowia znajdują się w grupie ryzyka IChP, nie skorzystały z pośredniej ochrony przed zakażeniem oferowanej w ramach programu powszechnych szczepień niemowląt i małych dzieci szczepionką PCV-7 w równie istotnym stopniu, jak osoby względnie zdrowe.27
Astma
Szacuje się, że 7,3% dorosłych Amerykanów choruje na astmę. Wyniki badania kliniczno-kontrolnego przeprowadzonego w stanie Tennessee wykazały, że w populacji dorosłych w wieku 18–49 lat IChP występuje częściej u chorych na astmę niż u osób bez astmy (iloraz szans z uwzględnieniem poprawki na znane czynniki zakłócające [aOR]: 2,4 [95% CI: 1,8–3,3]).29 Wśród chorych na astmę o dużym ryzyku* IChP występowała niemal 2 razy częściej niż u chorych na astmę o małym ryzyku.6 W badaniu tym zachorowania na IChP identyfikowano czynnie metodą populacyjnego nadzoru epidemiologicznego połączonego z czynnym nadzorem nad wynikami badań w laboratoriach mikrobiologicznych, a rozpoznanie astmy weryfikowano w bazie danych oddziału ubezpieczalni zdrowotnej (Medicaid) w Tennessee.29 Natomiast w badaniu przeprowadzonym w kohorcie emerytowanych wojskowych w starszym wieku (śr. 53 lata), ryzyko hospitalizacji z powodu pneumokokowego zapalenia płuc u chorych na astmę nie było większe niż u osób bez astmy lub przewlekłej obturacyjnej choroby płuc (POChP), których dobrano pod względem wieku, płci oraz regionu zamieszkania.30 Wskaźnik hospitalizacji z powodu pneumokokowego zapalenia płuc u chorych na POChP oszacowany w tym samym badaniu był natomiast znamiennie większy niż w grupie kontrolnej. Należy jednak pamiętać, że odróżnienie POChP od astmy staje się trudniejsze wraz z postępującym wiekiem pacjentów, dlatego nie można w tym badaniu wykluczyć nieprawidłowego zaklasyfikowania chorych.
Palenie papierosów
Badania wykorzystujące metodę populacyjnego nadzoru epidemiologicznego przeprowadzone przed wprowadzeniem szczepień PCV-7 zgodnie wykazywały, że palacze stanowią prawie połowę przypadków IChP u uprzednio zdrowych dorosłych osób.31 W latach 2001–2003 w Stanach Zjednoczonych wśród chorych na IChP w wieku 18–64 lat aż 53% paliło papierosy (program aktywnego nadzoru epidemiologicznego nad zakażeniami bakteryjnymi Centers for Disease Control and Prevention; dane nieopublikowane). W wieloośrodkowym, populacyjnym badaniu kliniczno-kontrolnym, w którym przypadki IChP identyfikowano w programie aktywnego nadzoru epidemiologicznego nad zakażeniami bakteryjnymi, ryzyko IChP wśród aktywnych palaczy w wieku 18–64 lat bez niedoboru odporności było 4-krotnie większe niż ryzyko w grupie kontrolnej osób, które nigdy nie paliły (aOR: 4,1 [95% CI: 2,4–7,3]).32 Zaobserwowano również znamienną zależność ryzyka IChP od liczby papierosów oraz paczek papierosów wypalonych w ciągu życia.32 Późniejsze badania potwierdziły, że palenie zwiększa ryzyko IChP także w innych grupach osób, w tym wśród pacjentów z niedoborami odporności.33
Oporność na antybiotyki
W Stanach Zjednoczonych, podobnie jak w innych krajach świata, coraz częściej pojawiają się szczepy pneumokoka oporne na antybiotyki.34,35 W niektórych rejonach nawet 35% izolatów wykazuje umiarkowany (najmniejsze stężenie hamujące [MIC]: 0,1–1,0 µg/ml) lub wysoki (MIC: >=2,0 µg/ml) poziom oporności na penicylinę.11,36,37 Wiele szczepów pneumokoka opornych na penicylinę jest również oporna na inne leki przeciwbakteryjne (np. erytromycynę, kotrimoksazol, cefalosporyny o poszerzonym zakresie działania). Wysoki poziom oporności na penicylinę i oporność na wiele leków często bardzo utrudnia leczenie zakażeń pneumokokowych, a wybór empirycznej terapii przeciwbakteryjnej u chorych z podejrzeniem pneumokokowego zapalenia opon mózgowo-rdzeniowych, zapalenia płuc czy zapalenia ucha środkowego staje się coraz większym wyzwaniem.38 Leczenie zakażeń wywołanych przez oporne bakterie może wymagać drogich alternatywnych leków przeciwbakteryjnych i przedłużonej hospitalizacji, co zwiększa koszty leczenia. Nie wiadomo natomiast dokładnie jaki jest wpływ antybiotykooporności na umieralność. Problem z narastającą opornością na leki przeciwbakteryjne jest dodatkowym argumentem przemawiającym za koniecznością szczepień w zapobieganiu zakażeniom pneumokokowym.
23-walentne szczepionki polisacharydowe przeciwko pneumokokom
Szczepionki polisacharydowe przeciwko pneumokokom są w użyciu od lat 70. ubiegłego wieku (najpierw 14-walentne, potem 23-walentne od lat 80.). Dostępne aktualnie PPSV-23 zawierają oczyszczone antygeny polisacharydowe otoczki pneumokoków 23 najczęściej wywołujących zachorowania typów serologicznych: 1, 2, 3, 4, 5, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20, 22F, 23F, 33F (tab. 2. – przyp. red.). W jednej dawce (0,5 ml) znajduje się 25 µg każdego z 23 antygenów rozpuszczonych w fizjologicznym roztworze soli, z dodatkiem 0,25% fenolu jako konserwanta. Szczepionki nie zawierają adiuwantów, ani tiomersalu (pochodna etylortęci, środek konserwujący o działaniu przeciwbakteryjnym i przeciwgrzybiczym).
Immunogenność PPSV-23
Polisacharydowe antygeny otoczki pneumokoka stymulują powstawanie serotypowo swoistych przeciwciał opsonizacyjnych, które ułatwiają fagocytozę i zabijanie bakterii przez leukocyty oraz inne komórki żerne. W ciągu 23 tygodni po szczepieniu u co najmniej 80% zdrowych, młodych dorosłych pojawia się swoista odpowiedź serologiczna (serokonwersja lub co najmniej 2-krotne zwiększenie stężenia swoistych przeciwciał).39 Zaobserwowano jednak istotne różnice w poziomie odpowiedzi wobec poszczególnych z 23 typów pneumokoka.
Swoiste przeciwciała w surowicy po podaniu PPSV-23 pojawiają się również u osób w podeszłym wieku oraz pacjentów z marskością alkoholową wątroby, chorych na POChP, a także na cukrzycę typu I.21,22,39 Niemniej jednak, zarówno stężenie swoistych przeciwciał, jak i odsetek pacjentów odpowiadających wytworzeniem swoistej odpowiedzi przeciwko poszczególnym typom serologicznym pneumokoka, mogą być w tych grupach mniejsze, w porównaniu ze zdrowymi, młodymi dorosłymi. Natomiast osoby po ukończeniu 2. roku życia bez śledziony (brak anatomiczny [wycięcie] lub czynnościowy [np. niedokrwistość sierpowatokrwinkowa]) zazwyczaj odpowiadają na szczepienie PPSV-23 podobnie jak ich zdrowi rówieśnicy.39
U chorych z niedoborem odporności odpowiedź serologiczna na szczepienie PPSV-23 jest zwykle znacznie upośledzona lub się wcale nie pojawia. Stężenie swoistych przeciwciał w surowicy po szczepieniu chorych na białaczkę, chłoniaka lub szpiczaka mnogiego jest znamiennie mniejsze niż u osób immunokompetentnych. Podobne zjawisko zaobserwowano u chorych z przewlekłą niewydolnością nerek wymagającą dializoterapii, po przeszczepieniu nerki lub z zespołem nerczycowym.22 Z kolei u pacjentów z chłoniakiem Hodgkina odpowiedź serologiczna jest lepsza, gdy PPSV-23 podano przed usunięciem śledziony, radioterapią lub chemioterapią (jednak podczas chemioterapii stężenie swoistych przeciwciał może się znamiennie zmniejszyć, a odpowiedź na szczepienia jest znacznie upośledzona).41
Upośledzona odpowiedź serologiczna na szczepienie PPSV-23 występuje także u chorych z zespołem nabytego niedoboru odporności (AIDS).42,43 Zmniejszenie stężenia swoistych przeciwciał w surowicy koreluje ze stopniem immunosupresji; niektorzy bezobjawowi nosiciele HIV lub pacjenci jedynie z uogólnionym powiększeniem węzłów chłonnych zadowalająco odpowiadają na podanie PPSV-23.44 Odpowiedź jest natomiast znamiennie osłabiona u zakażonych HIV z liczbą limfocytów CD4+ <500/µl w porównaniu z pacjentami HIV- -dodatnimi, u których ta liczba jest większa lub osobami HIV-ujemnymi.45
Polisacharydy otoczkowe bakterii stymulują wytwarzanie swoistych przeciwciał głównie na drodze niezależnej od limfocytów T, dlatego immunogenność tych antygenów u dzieci w pierwszych 2 latach życia jest generalnie bardzo słaba i nierówna.
Tabela 2. 23-walentne, polisacharydowe szczepionki przeciwko pneumokokom (PPSV-23) dostępne w Polscea
| Nazwa | Producent | Postać | Skład | Tiomersal |
| Pneumo 23 | Sanofi Pasteur | roztwór do wstrzykiwań i.m. lub s.c. | dawka (0,5 ml) zawiera po 0,025 mg oczyszczonego polisacharydu każdego z 23 serotypówb Streptococcus pneumoniae (1 strzykawka 0,5 ml) | nie zawiera |
| Pneumovax 23 | Merck Sharp & Dohme | roztwór do wstrzykiwań i.m. lub s.c. | dawka (0,5 ml) zawiera po 0,025 g wielocukru otoczkowego 23 serotypówb Streptococcus pneumoniae (1 fiol. 0,5 ml) | nie zawiera |
| a od Reakcji; opracowano na podstawie: Indeks leków Medycyny Praktycznej. Kraków, Wydawnictwo Medycyna Praktyczna, 2010
b Zawiera antygeny pneumokoków następujących typów serologicznych: 1, 2, 3, 4, 5, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20, 22F, 23F, 33F i.m. – domięśniowo, s.c. – podskórnie | ||||
Niepożądane odczyny poszczepienne
Zasadniczo szczepionki polisacharydowe przeciwko pneumokokom są uznawane za bezpieczne i dobrze tolerowane, co potwierdzają obserwacje od czasu ich wprowadzenia do praktyki (koniec lat 70. XX wieku). Około 50% osób zaszczepionych PPSV-23 może się skarżyć na łagodne dolegliwości w miejscu wstrzyknięcia (np. ból, zaczerwienie, obrzęk), które zazwyczaj ustępują samoistnie do 48 godzin. Umiarkowane objawy ogólne (np. gorączka, ból mięśni) lub cięższe reakcje miejscowe (naciek i stwardnienie) zdarzają się bardzo rzadko. Wstrzyknięcie śródskórne może spowodować ciężki odczyn miejscowy, dlatego nie jest to właściwa droga podania tej szczepionki. Choć po PPSV-23 opisywano także ciężkie reakcje ogólne (np. anafilaksja), to są one niezwykle rzadkie.21,22 W metaanalizie 9 badań z randomizacją polisacharydowych szczepionek przeciwko pneumokokom, w których oceniano również ich bezpieczeństwo i tolerancję, miejscowe odczyny poszczepienne zaobserwowano u co najwyżej 1/3 z 7531 zaszczepionych osób, natomiast nie zanotowano gorączki ani reakcji anafilaktycznych.46 Po PPSV nie obserwowano zaburzeń neurologicznych (np. zespołu Guillaina i Barre'go), ani zgonów związanych przyczynowo z podaniem szczepionki. Wstępne dane wykazały natomiast, że PPSV może wywołać przemijające nasilenie replikacji HIV, ale znaczenie kliniczne tego zjawiska nie jest znane.47 Inne badanie nie potwierdziło tych obserwacji,48 nie zanotowano także niekorzystnego wpływu szczepienia PPSV-23 na czas przeżycia chorych z HIV.47,48
Skuteczność i efektywność PPSV-23
Badania skuteczności i efektywności PPSV-23 obejmujące osoby z grup, w których zaleca się szczepienie przeciwko pneumokokom, dały sprzeczne wyniki w odniesieniu do zapobiegania zachorowaniom na pneumokokowe zapalenie płuc bez towarzyszącej bakteriemii.49 Większość wyników tych badań zgodnie wskazuje jednak, że szczepienie zmniejsza ryzyko IChP wśród zdrowych młodych dorosłych oraz w ogólnej populacji osób w wieku starszym. Badania obserwacyjne wskazywały na skuteczność wobec IChP wahającą się od około 50 do 80% wśród osób w starszym wieku bez zaburzeń odporności oraz u dorosłych chorych na niektóre choroby przewlekłe bez względu na wiek, uzasadniając zalecenie stosowania PPSV-23 w profilaktyce IChP.49 Nie wykazano jednak efektywności tej szczepionki u pacjentów z niedoborami odporności i u osób w bardzo podeszłym wieku (opublikowane niedawno wyniki nowego badania z randomizacją przeprowadzonego w Japonii wśród osób w wieku średnio około 85 lat potwierdziły, że szczepienie PPSV-23 znacznie zmniejszyło ryzyko pneumokokowego zapalenia płuc i hospitalizacji oraz zgonu z powodu zapalenia płuc [p. Med. Prakt. 9/2010] – przyp. red.). Niedawny przegląd systematyczny 15 badań z randomizacją i 7 badań obserwacyjnych skuteczności i efektywności PPSV-23 wykazał – na podstawie metaanalizy 10 badań z randomizacją – że szczepienie zmniejsza ryzyko IChP o 74% (95% CI: 56–85).50 Metaanaliza 7 badań obserwacyjnych dała natomiast wynik 52% (95% CI: 39–63).50 Inna metaanaliza, którą objęto tylko 6 badań z randomizacją, wykazała natomiast, że skuteczność PPSV-23 w profilaktyce bakteriemii pneumokokowej wynosi zaledwie 10%, a przedział ufności jest bardzo szeroki (95% CI: od –77 do 54).51 Duża różnica w wynikach obu cytowanych metaanaliz może wynikać z zakwalifikowania innych badań.
Zasady podawania PPSV-23
PPSV-23 należy wstrzykiwać domięśniowo lub podskórnie (jedna dawka to 0,5 ml). Można ją podawać podczas tej samej wizyty razem ze szczepionką przeciwko grypie (osobne wstrzyknięcie w drugie ramię), co nie zwiększa ryzyka niepożądanych odczynów poszczepiennych i nie upośledza odpowiedzi immunologicznej na szczepienie.52,53
Zalecenia dotyczące szczepienia dorosłych osób PPSV-23
Na posiedzeniach w czerwcu i październiku 2008 roku ACIP przyjął nowe i zmienione zalecenia dotyczące stosowania PPSV-23 w celu zapobiegania IChP u dorosłych do ukończenia 64. roku życia. ACIP uznał astmę za niezależny czynnik ryzyka IChP i zalecił jej dodanie do wskazań do szczepienia PPSV-23 obok innych przewlekłych chorób układu oddechowego (np. POChP, rozedmy; p. tab. 1). Tym samym ACIP zalecił, aby osoby w wieku 19–64 lat chore na astmę otrzymały jedną dawkę PPSV-23 (p. ramka 1).
|
Ramka 1. Aktualne zalecenia ACIP dotyczące szczepienia dorosłych
osób przeciwko pneumokokom 23-walentną szczepionką polisacharydową
(PPSV-23)
Szczepienie PPSV-23 (1 dawka) zaleca się: Jedną dawkę przypominającą (>=5 lat po pierwszej) zaleca się tylko: Nie zaleca się podawania więcej niż 2 dawek PPSV-23. |
ACIP zgodził się, że osoby palące papierosy znajdują się w grupie znamiennie zwiększonego ryzyka IChP, dlatego zalecił, aby każdego palącego w wieku 19–64 lat zaszczepić jedną dawką PPSV-23 i pouczyć, jak porzucić nałóg (p. ramka 1). (...)
PPSV-23 należy podać co najmniej 2 tygodnie przed planowanym wycięciem śledziony lub rozpoczęciem radioterapii albo chemioterapii (nie zaleca się szczepienia PPSV-23 w trakcie takiego leczenia). Zaleca się także, aby osoby HIV-dodatnie zaszczepić PPSV-23 jak najszybciej po potwierdzeniu zakażenia HIV.
Wszystkim osobom należy natomiast podać PPSV-23 w wieku 65 lat.** Osoby szczepione wcześniej PPSV-23 ze względu na wskazania związane ze stanem zdrowia (tab. 1) powinny otrzymać drugą dawkę szczepionki w wieku 65 lat lub później, jeśli od pierwszego szczepienia minęło 5 lat (ryc. 2). Osobom szczepionym po 64. roku życia zaleca się tylko jedną dawkę PPSV-23. Jeśli wcześniejszy stan uodpornienia przeciwko pneumokokom nie jest znany, należy podać jedną dawkę PPSV-23 (ryc. 2).
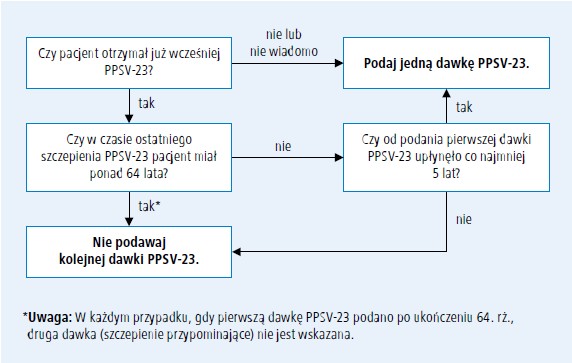
Ryc. 2. Algorytm podejmowania decyzji o szczepieniu 23-walentną szczepionką polisacharydową (PPSV-23) osób po 64. rż.
Dawki przypominające
Zalecenia ACIP dotyczące podawania dawki przypominającej nie zmieniły się od 1997 roku.2 Dla większości osób, którym ACIP zaleca szczepienie PPSV-23, nie proponuje się rutynowo dawki przypominającej.
Podanie drugiej dawki PPSV-23 zaleca się po upływie 5 lat od pierwszej dawki szczepienia osobom w wieku do 64 lat bez śledziony (w tym także z tzw. brakiem czynnościowym) oraz pacjentom z niedoborem odporności (tab. 1). ACIP nie zaleca wielokrotnych dawek przypominających ze względu na niewystarczające dane odnośnie do korzyści klinicznych, zwłaszcza stopnia i trwałości ochrony poszczepiennej oraz bezpieczeństwa takiego postępowania.
Poradnictwo antynikotynowe
Porzucenie nałogu palenia papierosów zmniejsza ryzyko zachorowania na IChP. W 1 badaniu wykazano, że ryzyko to zmniejszało się prawie o 14% każdego roku po zaprzestaniu palenia, a w ciągu 13 lat powracało do poziomu obserwowanego u osób nigdy niepalących.32 ACIP podkreśla, że poradnictwo dotyczące porzucenia nałogu palenia papierosów powinno stanowić stały element planu leczenia każdego palacza, bez względu na jego historię szczepień. Towarzystwa naukowe, takie jak Infectious Diseases Society of America oraz American Thoracic Society, także zalecają takie postępowanie wraz ze szczepieniem przeciwko pneumokokom (PPSV-23) każdemu palaczowi hospitalizowanemu z powodu pozaszpitalnego zapalenia płuc.54 (...)
Zalecenia dotyczące podawania PPSV-23 dzieciom z grup ryzyka
Od 1997 roku ACIP zaleca stosowanie PPSV-23 także u tych dzieci po ukończeniu 2. roku życia, które ze względu na stan zdrowia są szczególnie narażone na ciężkie zakażenia pneumokokowe (tab. 1).2 W 2010 roku do grup ryzyka dodano chorych na astmę, ale z zastrzeżeniem, że w przypadku dzieci i młodzieży zalecenie podawania PPSV-23 dotyczy astmy leczonej doustnymi GKS w dużej dawce (u dorosłych zalecenie obejmuje natomiast wszystkich chorych).3 IChP u dzieci z grup ryzyka wymienionych w tabeli 1. mogą wywoływać pneumokoki należące do szerszego wachlarza typów serologicznych w porównaniu ze zdrowymi dziećmi,55 dlatego od 2000 roku ACIP zaleca, aby dzieciom po 24. miesiącu życia podawać także PPSV-23 po zakończeniu schematu szczepienia szczepionką skoniugowaną (PCV).56 Dzieciom, które ze względu na wiek kwalifikują się do szczepienia PCV (w Polsce, zgodnie z rejestracją PCV-7 i PCV-13, dotyczy to dzieci do ukończenia 5. rż. – przyp. red.) nie należy natomiast podawać samej PPSV-23, bez wcześniejszego szczepienia PCV, gdyż szczepionki skoniugowane przeciwko pneumokokom charakteryzuje wiele korzystnych cech, w porównaniu z PPSV-23, takich jak: 1) skuteczna inicjacja immunologiczna i stymulacja pamięci immunologicznej; 2) ograniczenie nosicielstwa pneumokoków (dotyczy typów serologicznych uwzględnionych w PCV); 3) prawdopodobnie większa skuteczność kliniczna wobec pneumokoków najczęściej wywołujących IChP; 4) efektywność programu szczepień PCV-7 w zapobieganiu zakażeniom nieinwazyjnym (zapaleniu płuc bez bakteriemii, zapaleniu ucha środkowego).57,58
Nie przeprowadzono badań dotyczących oceny bezpieczeństwa podawania PPSV-23 po szczepieniu PCV-13. Jednak obserwacje dotyczące stosowania PPSV-23 w praktyce (od 1983 r.) nie budzą wątpliwości co do jej bezpieczeństwa, które jest podobne jak u dorosłych. Nie dysponujemy również wynikami badań, w których oceniano immunogenność sekwencyjnego schematu szczepienia najpierw PCV-13, a następnie PPSV-23. Niemniej, wcześniejsze badanie potwierdziło, że PPSV-23 podana po szczepieniu PCV-7 wzbudziła silną odpowiedź anamnestyczną (tzw. efekt dawki przypominającej) wobec antygenów 7 typów serologicznych pneumokoka znajdujących się w obu szczepionkach.59 Dane dotyczące skuteczności i efektywności PPSV-23 u dzieci przewlekle chorych z grup ryzyka (tab. 1) są ograniczone i niejednoznaczne, a skuteczności klinicznej PPSV-23 u dzieci zaszczepionych wcześniej PCV-7 lub PCV-13 nie oceniono w badaniach. Nie mamy również danych dotyczących bezpieczeństwa i skuteczności immunologicznej (immunogenności) schematu obejmującego podanie najpierw PPSV-23, a następnie PCV-13 (bardzo ograniczone obserwacje dotyczą podawania PCV-7 po PPSV-23 u dzieci i młodzieży zakażonych HIV).60
|
Ramka 2. Aktualne zalecenia ACIP dotyczące szczepienia dzieci z grup ryzyka przeciwko pneumokokom 23-walentną szczepionką
polisacharydową (PPSV-23)
Szczepienie PPSV-23 (1 dawka) zaleca się: Jedną dawkę przypominającą (>=5 lat po pierwszej) zaleca się tylko: Nie zaleca się podawania więcej niż 2 dawek PPSV-23. |
W niewielu badaniach przeprowadzonych u dzieci systematycznie oceniono immunogenność i bezpieczeństwo więcej niż 1 dawki przypominającej PPSV-23.59,61 Wyniki opublikowanych niedawno badań u dorosłych wzbudziły obawy, że podanie PPSV-23 może osłabiać odpowiedź serologiczną (mniejsze stężenie swoistych przeciwciał) po ponownym kontakcie z antygenami pneumokoka, w tym odpowiedź na wykonane później szczepienie PCV-7.62,63 Znaczenie kliniczne tej obserwacji nie jest znane.59 Nie wiadomo także, czy u dzieci podanie PPSV-23 przed lub po PCV-13 może wywoływać podobną reakcję na kolejne dawki PCV-13. Zalecenia ACIP dotyczące podawania PPSV-23 dzieciom z grup ryzyka (tab. 1) podsumowano w ramce 2. Dzieci te (w Polsce do ukończenia 5. rż., wg ulotki rejestracyjnej PCV-7 i PCV-13 – przyp. red.) należy najpierw zaszczepić szczepionką skoniugowaną PCV zgodnie z zaleceniami dla wieku, a następnie co najmniej 8 tygodni po ostatniej dawce PCV podać im PPSV-23. Tym, które otrzymały PPSV-23 zanim zarejestrowano PCV-13, ACIP zaleca podanie także PCV-13 (w Polsce do ukończenia 5. rż. – przyp. red.). Zalecenia dotyczące podawania dawki przypominającej są takie same jak dla dorosłych pacjentów. Szczepienie przeciwko pneumokokom (PCV i/lub PPSV-23) należy zakończyć co najmniej 2 tygodnie przed planowanym wycięciem śledziony, wszczepieniem protezy ślimaka lub rozpoczęciem leczenia immunosupresyjnego.
_______________________________________________
* Chory na astmę spełniający >=1 z następujących kryteriów: 1) hospitalizacja lub leczenie na szpitalnym oddziale ratunkowym z powodu astmy; 2) wystawiona recepta na cykl leczenia glikokortykosteroidami (GKS) systemowymi w ramach terapii ratującej lub przewlekłe (przez >=120 dni) leczenie GKS doustnymi; 3) >=3 recepty na szybko działający β2-mimetyk w ciągu roku poprzedzającego kwalifikację do badania.
** Od Redakcji: W aktualnym polskim Programie Szczepień Ochronnych szczepienie przeciwko pneumokokom wszystkich osób po 65. rż. oraz chorych na niektóre choroby przewlekłe (wymienione także w zaleceniach ACIP – p. tab. 1) 23-walentną szczepionką polisacharydową (PPSV-23) ma status szczepienia zalecanego, niefinansowanego z budżetu Ministerstwa Zdrowia. Lekarz opiekujący się takim pacjentem jest ustawowo zobowiązany do przekazania mu tej informacji, wraz z rzetelną informacją o korzyściach ze szczepienia i ryzyku niepożądanych odczynów poszczepiennych. Zakup samej szczepionki finansuje pacjent, ale w instytucjach sprawujących opiekę w ramach kontraktu z NFZ kwalifikacja lekarska i zabieg szczepienia są bezpłatne. Dzieci przewlekle chore (z grupy ryzyka – p. tab. 1) do ukończenia 5. rż. należy najpierw zaszczepić skoniugowaną szczepionką przeciwko pneumokokom (PCV) zgodnie z zaleceniami, a dopiero w drugim etapie podać im PPSV-23.
Piśmiennictwo
1. CDC: Active Bacterial Core Surveillance (ABCs) Report: Emerging Infections Program Network. Streptococcus pneumoniae, provisional – 2009. Atlanta, GA, US Department of Health and Human Services, CDC; 2010. http://www.cdc.gov/abcs/reportsfindings/ survreports/spneu09.pdf
2. CDC: Prevention of pneumococcal disease: recommendations of the Advisory Committee on Immunization Practices (ACIP). MMWR, 1997; 46 (No. RR8)
3. Centers for Disease Control and Prevention. Prevention of pneumococcal disease among infants and children – use of 13-valent pneumococcal conjugate vaccine and 23-valent pneumococcal polysaccharide vaccine. Recommendations of the Advisory Committee on Immunization Practices (ACIP). MMWR, 2010; 59 (RR-11): 11–15
4. CDC. Pneumococcal polysaccharide vaccine usage, United States. MMWR, 1984; 33: 273–276, 281
5. Williams W.W., Hickson M.A., Kane M.A., Kendal A.P., Spika J.S., Hinman A.R.: Immunization policies and vaccine coverage among adults: the risk for missed opportunities. Ann. Intern. Med., 1988; 108: 616–625
6. Stool S.E., Field M.J.: The impact of otitis media. Pediatr. Infect. Dis. J., 1989; 8 (supl.): S11–S14
7. Jernigan D.B., Cetron M.S., Breiman R.F.: Minimizing the impact of drug-resistant Streptococcus pneumoniae (DRSP): a strategy from the DRSP working group. JAMA, 1996; 275: 206–209
8. Istre G.R., Tarpay M., Anderson M., Pryor A., Welch D., Pneumococcus Study Group. Invasive disease due to Streptococcus pneumoniae in an area with a high rate of relative penicillin resistance. J. Infect. Dis., 1987; 156: 732–735
9. Breiman R.F., Spika J.S., Navarro V.J., Darden P.M., Darby C.P.: Pneumococcal bacteremia in Charleston County, South Carolina: a decade later. Arch. Intern. Med., 1990; 150: 1401–1405
10. Bennett N.M., Buffington J., LaForce F.M.: Pneumococcal bacteremia in Monroe County, New York. Am. J. Public Health, 1992; 82: 1513–1516
11. Hofmann J., Cetron M.S., Farley M.M., et al.: The prevalence of drug-resistant Streptococcus pneumonia in Atlanta. N. Engl. J. Med., 1995; 333: 481–486
12. Plouffe J.F., Breiman R.F., Facklam R.R.: Franklin County Pneumonia Study Group. Bacteremia with Streptococcus pneumoniae in adults-implications for therapy and prevention. JAMA, 1996; 275: 194–198
13. Burman L.A., Norrby R., Trollfors B.: Invasive pneumococcal infections: incidence, predisposing factors, and prognosis. Rev. Infect. Dis., 1985; 7: 133–142
14. Kuikka A., Syrjänen J., Renkonen O.-V., Valtonen V.: Pneumococcal bacteremia during a recent decade. J. Infect., 1992; 24: 157–168
15. Afessa B., Greaves W.L., Frederick W.R.: Pneumococcal bacteremia in adults: a 14-year experience in an inner-city university hospital. Clin. Infect. Dis., 1995; 21: 345–351
16. Wenger J.D., Hightower A.W., Facklam R.R., Gaventa S., Broome C.V., Bacterial Meningitis Study Group. Bacterial meningitis in the United States, 1986: report of a multistate surveillance study. J. Infect. Dis., 1990; 162: 1316–1323
17. Marrie T.J., Durant H., Yates L.: Community-acquired pneumonia requiring hospitalization: 5-year prospective study. Rev. Infect. Dis., 1989; 11: 586–599
18. Research Committee of the British Thoracic Society. Community-acquired pneumonia in adults in British hospitals in 1982–1983: a survey of aetiology, mortality, prognostic factors and outcome. Q. J. Med., 1987; 62: 195–220
19. Fang G.D., Fine M., Orloff J., et al.: New and emerging etiologies for community-acquired pneumonia with implications for therapy: a prosepective multicenter study of 359 cases. Medicine, 1990; 69: 307–316
20. Torres A., Serra-Batlles J., Ferrer A., et al.: Severe community-acquired pneumonia: epidemiology and prognostic factors. Am. Rev. Respir. Dis., 1991; 144: 312–318
21. CDC. Recommendations of the Immunization Practices Advisory Committee: pneumococcal polysaccharide vaccine. MMWR, 1989; 38: 64–8,73–6
22. Fedson D.S., Musher D.M.: Pneumococcal vaccine. In: Plotkin S.A., Mortimer E.A. Jr, eds. Vaccines. 2nd ed. Philadelphia, PA, WB Saunders, 1994: 517–563
23. Gardner P., Schaffner W.: Immunization of adults. N. Engl. J. Med., 1993; 328: 1252–1258
24. Hook E.W., Horton C.A., Schaberg D.R.: Failure of intensive care unit support to influence mortality from pneumococcal bacteremia. JAMA, 1983; 249: 1055–1057
25. Mufson M.A., Oley G., Hughey D.: Pneumococcal disease in a medium-sized community in the United States. JAMA, 1982; 248: 1486–1489
26. Campbell J.F., Donohue M.A., Mochizuki R.B., Nevin-Woods C.L., Spika J.S.: Pneumococcal bacteremia in Hawaii: initial findings of a pneumococcal disease prevention project. Hawaii Med. J., 1989; 48: 513–518
27. Pilishvili T., Lexau C., Farley M.M., et al.: Sustained reductions in invasive pneumococcal disease in the era of conjugate vaccine. J. Infect. Dis., 2010; 201: 32–41
28. Singleton R.J., Butler J.C., Bulkow L.R., et al.: Invasive pneumococcal disease epidemiology and effectiveness of 23valent pneumococcal polysaccharide vaccine in Alaska Native adults. Vaccine, 2007; 25: 2288–2295
29. Talbot T.R., Hartert T.V., Mitchel E., et al.: Asthma as a risk factor for invasive pneumococcal disease. N. Engl. J. Med., 2005; 352: 2082–2090
30. Lee T.A., Weaver F.M., Weiss K.B.: Impact of pneumococcal vaccination on pneumonia rates in patients with COPD and asthma. J. Gen. Intern. Med., 2007; 22: 62–67
31. Plouffe J.F., Breiman R.F., Facklam R.R.: Bacteremia with Streptococcus pneumoniae: implications for therapy and prevention. Franklin County Pneumonia Study Group. JAMA, 1996; 275: 194–198
32. Nuorti J.P., Butler J.C., Farley M.M., et al.: Cigarette smoking and invasive pneumococcal disease. Active Bacterial Core Surveillance Team. N. Engl. J. Med., 2000; 342: 681–689
33. Breiman R.F., Keller D.W., Phelan M.A., et al.: Evaluation of effectiveness of the 23valent pneumococcal capsular polysaccharide vaccine for HIVinfected patients. Arch. Intern. Med., 2000; 160: 2633–2638
34. Klugman K.P.: Pneumococcal resistance to antibiotics. Clin. Microbiol. Rev., 1990; 3: 171–196
35. Butler J.C., Hofmann J., Cetron M.S., Elliott J.A., Facklam R.R., Breiman R.F.: The continued emergence of drug-resistant Streptococcus pneumoniae in the United States: an update from the Centers for Disease Control and Prevention's Pneumococcal Sentinel Surveillance System. J. Infect. Dis., 1996; 174: 986–993
36. Arnold K.E., Leggiadro R.J., Breiman R.F., et al.: Risk factors for carriage of drug-resistant Streptococcus pneumoniae among children in Memphis, Tennessee. J. Pediatr., 1996; 128: 757–764
37. Duchin J.S., Breiman R.F., Diamond A., et al.: High prevalence of multidrug-resistant Streptococcus pneumoniae among children in a rural Kentucky community. Pediatr. Infect. Dis. J., 1995; 14: 745–750
38. American Academy of Pediatrics, Committee on Infectious Diseases. Therapy for children with invasive pneumococcal infections. Pediatrics, 1997; 99: 289–299
39. Musher D.M., Luchi M., Watson D.A., Hamilton R., Baughn R.E.: Pneumococcal polysaccharide vaccine in young adults and older bronchitics: determination of IgG responses by ELISA and the effect of adsorption of serum with non-type–specific cell wall polysaccharide. J. Infect. Dis., 1990; 161: 728–735
40. Ammann A.J., Addiego K., Wara D.W., Lubin D., Smith W.B., Mentzer W.C.: Polyvalent pneumococcal-polysaccharide immunization of patients with sickle cell anemia and patients with splenectomy. N. Engl. J. Med., 1977; 297: 897–900
41. Siber G.R., Gorham C., Martin P., Corkey J.C., Schiffman G.: Antibody response to pretreatment immunization and post-treatment boosting with bacterial polysaccharide vaccines in patients with Hodgkins disease. Ann Intern. Med., 1986; 104: 467–475
42. Ammann A.J., Schiffman G., Abrams D., Volberding P., Ziegler J., Conant M.: B-cell immunodeficiency in acquired immune deficiency syndrome. JAMA, 1984; 251: 1447–1449
43. Ballet J.-J., Sulcebe G., Couderc L.-J., et al.: Impaired anti-pneumococcal antibody response in patients with AIDS-related persistent generalized lymphadenopathy. Clin. Exp. Immunol., 1987; 68: 479–487
44. Huang K.-L., Ruben F.L., Rinaldo C.R. Jr, Kingsley L., Lyter D.W., Ho M.: Antibody responses after influenza and pneumococcal immunization in HIV infected homosexual men. JAMA, 1987; 257: 2047–2050
45. Rodriguez-Barradas M.C., Musher D.M., Lahart C., et al.: Antibody to capsular polysaccharides of Streptococcus pneumoniae after vaccination of human immunodeficiency virus-infected subjects with 23-valent pneumococcal vaccine. J. Infect. Dis., 1992; 165: 553–556
46. Fine M.J., Smith M.A., Carson C.A., et al.: Efficacy of pneumococcal vaccination in adults: a metaanalysis of randomized controlled trials. Arch. Intern. Med., 1994; 154: 2666–2677
47. Brichacek B., Swindells S., Janoff E.N., Pirruccello S., Stevenson M.: Increased plasma HIV-1 burden following antigenic challenge with pneumococcal vaccine. J. Infect. Dis., 1996; 174: 1191–1199
48. Katzenstein T.L., Gerstoft J., Nielsen H.: Assessments of plasma HIV RNA and CD4 cell counts after combined Pneumovax and tetanus toxoid vaccination: no detectable increase in HIV replication 6 weeks after immunization. Scand. J. Infect. Dis., 1996; 28: 239–241
49. World Health Organization: 23valent pneumococcal polysaccharide vaccine. WHO position paper. Wkly Epidemiol. Rec., 2008; 83: 373–384
50. Moberley S.A., Holden J., Tatham D.P., Andrews R.M.: Vaccines for preventing pneumococcal infection in adults. Cochrane Database Syst. Rev., 2008; 1: CD000 422
51. Huss A., Scott P., Stuck A.E., Trotter C., Egger M.: Efficacy of pneumococcal vaccination in adults: a metaanalysis. CMAJ, 2009; 180: 48–58
52. Hilleman M.R., Carlson A.J., McLean A.A., Vella P.P., Weibel R.E., Woodhour A.F.: Streptococcus pneumonia polysaccharide vaccine: age and dose responses, safety, persistence of antibody, revaccination, and simultaneous administration of pneumococcal and influenza vaccines. Rev. Infect. Dis., 1981; 3 (supl): S31–S42
53. DeStefano F., Goodman R.A., Noble G.R., McClary G.D., Smith S.J., Broome C.V.: Simultaneous administration of influenza and pneumococcal vaccines. JAMA, 1982; 247: 2551–2554
54. Mandell L.A., Wunderink R.G., Anzueto A., et al.: Infectious Diseases Society of America/ American Thoracic Society consensus guidelines on the management of communityacquired pneumonia in adults. Clin. Infect. Dis., 2 007; 44 (suppl. 2): S27–S72
55. Hausdorff W.P., Feikin D.R., Klugman K.P.: Epidemiological differences among pneumococcal serotypes. Lancet Infect. Dis. 2005; 5: 83–93
56. Centers for Diseases Control and Prevention: Preventing pneumococcal disease among infants and young children: recommendations of the Advisory Committee on Immunization Practices (ACIP). MMWR 2000; 49 (No. RR-9)
57. Black S., Eskola J., Whitney C., Shinefield H.: Pneumococcal conjugate vaccine and pneumococcal common protein vaccines. W: Plotkin S.A., Orenstein W.A., Offit P.A. (red.): Vaccines. 5th ed. Philadelphia, PA, WB Saunders Company, 2008: 531–568
58. O'Brien K.L., Santosham M.: Potential impact of conjugate pneumococcal vaccines on pediatric pneumococcal diseases. Am. J. Epidemiol., 2004; 159: 634–644
59. O'Brien K.L., Hochman M., Goldblatt D.: Combined schedules of pneumococcal conjugate and polysaccharide vaccines: is hyporesponsiveness an issue? Lancet Infect. Dis., 2007; 7: 597–606
60. Abzug M.J., Pelton S.I., Song L.Y. i wsp.: Immunogenicity, safety, and predictors of response after a pneumococcal conjugate and pneumococcal polysaccharide vaccine series in human immunodeficiency virus-infected children receiving highly active antiretroviral therapy. Pediatr. Infect. Dis. J., 2006; 25: 920–929
61. Jackson L.A., Neuzil K.M.: Pneumococcal polysaccharide vaccines. W: Plotkin S.A., Orenstein W.A., Offit P.A. (red.): Vaccines. 5th ed. Philadelphia, PA, WB Saunders Company, 2008: 569–604
62. de Roux A., Schmole-Thoma B., Siber G.R. i wsp.: Comparison of pneumococcal conjugate polysaccharide and free polysaccharide vaccines in elderly adults: conjugate vaccine elicits improved antibacterial immune responses and immunological memory. Clin. Infect. Dis., 2008; 46: 1015–1023
63. Torling J., Hedlund J., Konradsen H.B., Ortqvist A.: Revaccination with the 23-valent pneumococcal polysaccharide vaccine in middle-aged and elderly persons previously treated for pneumonia. Vaccine, 2003; 22: 96–103
Komentarz
prof. dr hab. med. Waleria HryniewiczZakład Epidemiologii i Mikrobiologii Klinicznej Narodowego Instytutu Leków w Warszawie
Zakażenia pneumokokowe (Streptococcus pneumoniae) stanowią jeden z najpoważniejszych problemów medycyny zakażeń, odpowiadając za znaczną zachorowalność oraz śmiertelność, i to nie tylko w krajach rozwijających się.1,2 Dotyczy to przede wszystkich pacjentów w skrajnych grupach wiekowych lub z dodatkowymi medycznymi czynnikami ryzyka. Pneumokoki charakteryzują się znaczną zjadliwością i coraz szerszą opornością na najważniejsze grupy antybiotyków. W związku z tym obecnie najskuteczniejszą metodą zmniejszenia liczby zakażeń pneumokokowych i ich konsekwencji jest wprowadzanie programów szczepień. Aktualne zalecenia różnych towarzystw naukowych i instytucji krajowych dotyczące stosowania szczepionek przeciwko pneumokokom skupiają się właśnie na tych dwóch wymienionych powyżej grupach wiekowych (najmłodszych dzieciach oraz osobach w podeszłym wieku), a także na osobach z grup ryzyka ze względu na stan zdrowia (chorych przewlekle, bez względu na wiek).
Ponieważ odporność związana jest z obecnością przeciwciał przeciwko wielocukrom otoczkowym pneumokoka, to one są składnikami szczepionek. Opisano już 93 typy serologiczne S. pneumoniae wyodrębnione na podstawie różnic antygenowych polisacharydów otoczkowych. Wiele lat temu udało się wprowadzić do praktyki szczepionkę zawierającą 23 z nich (23-walentna szczepionka polisacharydowa – PPS V-23), tych które najczęściej wywołują inwazyjne zakażenia. Praktycznie jej szerokie stosowanie miało miejsce jedynie w Stanach Zjednoczonych i zalecano ją przede wszystkim osobom >=65. roku życia, a także chorym po 2. roku życia szczególnie narażonym na ciężkie zakażenia pneumokokowe ze względu na stan zdrowia. Na podkreślenie zasługuje dodanie przez ACIP do grup ryzyka ciężkich zakażeń pneumokokowych u dorosłych także wszystkich chorych na astmę oraz palących papierosy – dość licznej populacji, której nie uwzględniono we wcześniejszych wersjach zaleceń.
Od lat toczy się dyskusja na temat właściwego miejsca PPS V-23 w profilaktyce zakażeń pneumokokowych. Ograniczeniem tej szczepionki jest brak skuteczności u dzieci <2. roku życia, a także obawa przed podaniem dawki przypominającej ze względu na ryzyko osłabienia odpowiedzi immunologicznej po kolejnych dawkach, co zaobserwowano w przypadku powtórnej immunizacji także innymi antygenami polisacharydowymi. Po wprowadzeniu do użycia szczepionek skoniugowanych przeciwko pneumokokom (PC V) – najpierw 7-walentnej, a następnie 10- i 13-walentnych, skutecznych u najmłodszych dzieci – zainteresowanie PPS V-23 się zwiększyło i ukazało się kilka nowych badań klinicznych i metaanaliz dotyczących jej skuteczności, a także potencjalnego stosowania jako dawki uzupełniającej po szczepionce skoniugowanej.
Opublikowane w 2010 roku badanie z randomizacją Maruyamy i wsp. (omówienie – p. Med. Prakt. 9/2010, s. 72), pomimo pewnych zastrzeżeń w kwestii dokładnej analizy sytuacji epidemiologicznej, wskazuje na ważną rolę PPS V-23 w zmniejszeniu zachorowalności i umieralności z powodu pneumokokowego zapalenia płuc w populacji ludzi starszych i pensjonariuszy domów przewlekłej opieki.3 Korzyści ze szczepienia obejmują także mniejszą śmiertelność oraz łagodniejszy przebieg w razie zachorowania.3
Wprowadzenie PC V-7 dla niemowląt i małych dzieci do kalendarza szczepień powszechnych w Stanach Zjednoczonych w 2000 roku (rejestracja <5. rż.) okazało się ogromnym sukcesem także dla dorosłych. Powszechne szczepienia dzieci spowodowały zmniejszenie liczby zachorowań wywoływanych przez pneumokoki u dzieci, zwłaszcza inwazyjnych, a dzięki wytworzeniu odporności zbiorowiskowej zaobserwowano także zmniejszenie o 55% zapadalności na inwazyjną chorobę pneumokokową (IC hP) w populacji >=50. roku życia, wywoływaną przez typy serologiczne zawarte w tej szczepionce.4
Obecnie są już dostępne PC V-10 (rejestracja do 24. mż.) i PC V-13 (rejestracja w Europie do 5. rż.), które z pewnością dalej ograniczą zapadalność na IC hP. Wydaje się jednak, że ze względu na trudności w opracowaniu nie należy się już spodziewać kolejnych PC V zawierających jeszcze więcej typów serologicznych pneumokoka. Z tego między innymi powodu ponownie zaczęto analizować przydatność i rolę PPS V-23 w procesie immunizacji przeciwko pneumokokom.
Zaletą PPS V-23 jest niewątpliwie najszersze pokrycie serotypów pneumokoka (p. także ryc. 1). Wady i zastrzeżenia wymieniono powyżej. Trwające aktualnie badania dotyczące skuteczności PC V-13 u dorosłych skłaniają także do zadania kilku pytań odnośnie do możliwości zastosowania PPS V-23 po skoniugowanej szczepionce, a odpowiedź na nie powinna wykluczyć efekt obniżonej odpowiedzi po drugiej dawce i dać możliwość zastosowania PPS V-23 w celu przedłużenia okresu ochrony przed zakażeniem.5,6
Wyniki pierwszego ze wspomnianych powyżej badań dotyczących sekwencyjnych schematów szczepienia PC V i PPS V-23, w którym analizowano podawanie jako pierwszej dawki PC V-7, a następnie PPS V-23 u osób w wieku 50–80 lat, były dość zaskakujące. Wykazano bowiem, że odpowiedź immunologiczna (stężenie swoistych przeciwciał) po pierwszej dawce PC V-7 zależała od typu serologicznego pneumokoka. Porównano ją z odpowiedzią wytworzoną po pierwszej dawce PPS V-23. Okazało się, że PC V-7 dawała lepszą odpowiedź dla typów serologicznych 4, 9V i 23F, ale gorszą dla 19F. Natomiast gdy pacjentom podawano drugą dawkę szczepionki PC V-7, to wyniki nie zawsze były lepsze, niż po podaniu jako drugiej dawki PPS V-23. Ostateczny wniosek z tego badania brzmi, że podanie dwóch dawek w najstarszej badanej grupie nie zwiększyło stężenia swoistych przeciwciał. Nie obserwowano jednak obniżenia odpowiedzi po drugiej dawce szczepionki skoniugowanej.5 Wadą badania było zastosowanie jedynie testu pomiaru stężenia przeciwciał bez oceny ich właściwości funkcjonalnych, co wydaje się być pożądane u osób w podeszłym wieku.
Podobne wnioski przynosi najnowsza publikacja dotycząca podawania PPS V-23 po PC V-7 u dorosłych (choć wydaje się, że wnioski można odnieść generalnie do szczepionek PC V).6 Zaobserwowano zróżnicowaną odpowiedź serologiczną na wspólne w obu szczepionkach typy serologiczne pneumokoka. Okazało się, że podanie dwóch dawek PC V-7, a następnie PPS V-23 jedynie nieznacznie poprawia odpowiedź, w porównaniu z podaniem tylko jednej dawki PPS V-23. Podobnie jak w wyżej omawianym badaniu zastosowano jedynie oznaczanie stężenia przeciwciał bez oceny ich wartości funkcjonalnej. Wyniki te są zaskakujące, a brak wzmocnienia odpowiedzi po podaniu drugiej dawki nie do końca jest wytłumaczalne. Wskazuje się na rolę nosicielstwa, które mogło pobudzać odpowiedź immunologiczną w przeszłości na tyle, że nie dochodziło już do jej dalszego zwiększenia, a także możliwość neutralizacji drugiej dawki przez wzbudzone pierwszą dawką przeciwciała. Aktualnie brak przekonujących danych i silnych zaleceń dotyczących sekwencyjnego stosowania PC V i PPS V-23 u dorosłych, a w naszych warunkach zgodnie z rejestracją do wykorzystania pozostaje na razie PPS V-23. Niezbędne są jednak dalsze badania dotyczące optymalnego sposobu uodpornienia dorosłych w podeszłym wieku i pacjentów z grup ryzyka przeciwko pneumokokom (m.in. z zastosowaniem PC V-13).
W Polsce sytuacja epidemiologiczna IC hP jest coraz lepiej rozpoznawana dzięki dynamicznej aktywności Krajowego Ośrodka Referencyjnego (www.koroun.edu.pl). Ostatnie dane (2010 r., nieopublikowane) wskazują, że zapadalność na IC hP u dzieci <2. roku życia wynosi średnio ponad 5/100 000, a u dorosłych >60. roku życia 1,6/100 000. Wydaje się, że wskaźniki te są znacznie zaniżone (aczkolwiek są dużo większe niż dotychczas), bowiem w niektórych województwach analiza opiera się na niewielkiej liczbie przypadków. Są one jednak coraz bardziej wiarygodne i stopniowo zbliżają się do wartości obserwowanych w innych krajach Europy i Ameryki Północnej. Opublikowane ostatnio wyniki monitorowania IC hP w Polsce w latach 2006–2009 (n = 725 przypadków IC hP) wskazywały na zapadalność 2,7/100 000 w grupie <2. roku życia i 0,5/100 000 u osób >60. roku życia.7 Szczególnie niepokojąca jest w Polsce znaczna oporność inwazyjnych pneumokoków na antybiotyki, co utrudnia wybór właściwego leczenia empirycznego. Wiąże się to także z bardzo dużą śmiertelnością, która dla całej grupy badanej wyniosła 15%, natomiast dla pacjentów ze znanym przebiegiem choroby aż 38,4% (>65. rż.– 59%!). Jeśli spojrzymy na pokrycie typów serologicznych u dzieci do 2. roku życia na podstawie izolatów uzyskanych w 2010 roku, to wynosiło ono dla szczepionki PC V-10 – 78%, a dla PC V-13 – 94% (dane KOROUN).
Omówiona powyżej sytuacja epidemiologiczna ciężkich zakażeń pneumokokowych w P olsce wskazuje na pilną potrzebę:
Piśmiennictwo do komentarza
1. www.who.int/vaccine_research/diseases/ari/en/index3.html
2. CDC. Active Core Surveillance (ABCs) Report: Emerging Infections Program Network. Streptococcus pneumonia, 2010 (www.Cdc.gov/abcs/reports-findings/survreports/spneu09.pdf
3. Maruyama T., Taguchi O., Niederman M.S. i wsp.: Efficacy of 23-valent pneumococcal vaccine in preventing pneumonia and improving survival In nursing home residents: double blind, randomized and placebo controlled trial. BMJ, 2010; 340: c1004
4. Lexau C.A., Lynfield R., Danila R. i wsp.: Changing epidemiology of invasive pneumococcal disease among older adults In the era of pediatric pneumococcal conjugate vaccine. JAMA, 2005; 294: 2043–2051
5. Goldblatt D., Southern J., Andrews N. i wsp.: The immunogenicity of 7-valent pneumococcal conjugate versus 23-valent polysaccharide vaccine in adults aged 50–80 years. Clin. Infect. Dis., 2009; 49: 1318–1325
6. Lazarus R., Clutterbuck E., Yu L.-M. i wsp.: A randomized study comparing combined pneumococcal conjugate and polysaccharide vaccination schedules in adults. Clin. Infect. Dis., 2011; 52: 736–742
7. Skoczynska A., Sadowy E., Bojarska K. i wsp.: The current status of invasive pneumococcal disease in Poland. Vaccine, 2011; 29: 2199–2205

























