Komentarz
U pacjentów z podejrzeniem bądź rozpoznaniem
zakażenia SARS-CoV-2 RTG klatki piersiowej
może być badaniem obrazowym pierwszego wyboru,
wykonywanym zarówno przy przyjęciu
do szpitala, jak i później, w celu monitorowania
przebiegu choroby. Użycie przenośnych aparatów
rentgenowskich i wykonywanie badań przyłóżkowych
eliminuje konieczność przewożenia chorego
do pracowni radiologicznej i zmniejsza ryzyko rozprzestrzeniania
się wirusa.2,3 W retrospektywnym
badaniu przeprowadzonym we Włoszech w marcu
2020 roku oceniono RTG klatki piersiowej 234 pacjentów z dodatnim wynikiem testu RT-PCR w kierunku zakażenia SARS-CoV-2. Najczęściej
występującymi nieprawidłowościami były zacienienia
siateczkowo-guzkowe (u 66,6% chorych),
przymglenia (62,8%) oraz zagęszczenia (konsolidacje)
miąższowe (57,7%). Zmiany te zwykle były
umiejscowione przypodstawnie i obwodowo, w obu
płucach. Jedynie u 13 chorych (5,6%) nie stwierdzono
nieprawidłowości w płucach na RTG.2,3
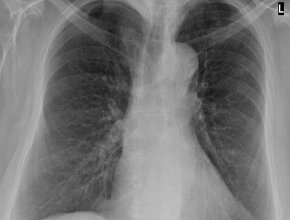
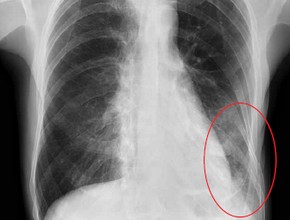
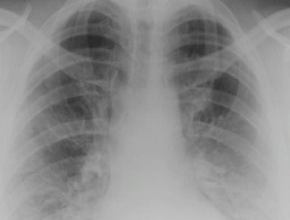
U opisanego chorego RTG klatki piersiowej wykonany w dniu przyjęcia uwidocznił obustronne
plamiste zacienienia wskazujące na zmiany zapalne.
Kolejny RTG, wykonany po 2 dniach, wykazał
wyraźną progresję zagęszczeń miąższowych w całych
płucach, z największym nasileniem obwodowo, z czym korespondował gorszy stan ogólny chorego.
Stwierdzane zmiany w płucach były typowe dla
COVID-19. Regresję zmian stwierdzono dopiero
na RTG wykonanym w 9. dobie hospitalizacji.
Tomografia komputerowa (TK) klatki piersiowej
charakteryzuje się dużą czułością (92%) w wykrywaniu zmian śródmiąższowych i pozwala
na wczesne stwierdzenie zajęcia płuc w przebiegu
zakażenia SARS-CoV-2.3 Wykonanie TK należy
rozważyć w przypadku niezgodności obrazu
klinicznego z wynikami badań diagnostycznych
(zwłaszcza, gdy stężenie dimeru D jest znacznie
zwiększone i rośnie w czasie leczenia) oraz u chorych z podejrzeniem współistnienia innych
chorób lub powikłań (ropień płuca, guz płuca).3,4 U opisanego pacjenta nie wykonywano TK klatki
piersiowej, gdyż obraz kliniczny i zmiany stwierdzane
na RTG klatki piersiowej były spójne; wynik
TK klatki piersiowej nie zmieniłby postępowania.
U chorego zastosowano glikokortykosteroid
(deksametazon) ogólnoustrojowo, opierając się
na wynikach brytyjskiego wieloośrodkowego badania o akronimie RECOVERY. W badaniu tym
wykazano znamienne zmniejszenie 28-dniowej
śmiertelności u chorych na COVID-19 wymagających
wspomagania wentylacji i otrzymujących
deksametazon dożylnie w dawce dobowej 6 mg
przez 10 dni: w grupie chorych wymagających
samej tlenoterapii – o 18%, a w grupie chorych
wentylowanej mechanicznie – o 36%. Przypuszcza
się, że korzystne działanie deksametazonu polega
na zmniejszaniu uszkodzeń narządowych powodowanych
przez nadmierną reakcję zapalną.5 Na podstawie wyników badania RECOVERY Europejska
Agencja Leków zatwierdziła stosowanie
deksametazonu u chorych na COVID-19 wymagających
tlenoterapii biernej lub wentylacji mechanicznej.5,6
Z powodu dużych i narastających wartości parametrów
stanu zapalnego (CRP) oraz leukocytozy z przewagą neutrofilów, mogących świadczyć o nadkażeniu bakteryjnym dróg oddechowych, u chorego stosowano antybiotykoterapię empiryczną
ceftriaksonem w dawce 2 g 2 × dz. dożylnie
przez 10 dni. Pomimo małego stężenia prokalcytoniny
nie można było wykluczyć współistnienia
zakażenia bakteryjnego powodującego pozaszpitalne
zapalenie płuc. Ponadto zakażenie wirusowe
sprzyja wtórnemu zakażeniu bakteryjnemu,
co wynika z uszkadzającego działania wirusów
na nabłonek pęcherzyków płucnych oraz zaburzeń
funkcjonowania układu immunologicznego.7 Oczywiście
przy podejmowaniu decyzji o zastosowaniu
antybiotyku należy mieć na uwadze cały obraz
kliniczny, a w razie konieczności wykonać posiewy
krwi, moczu lub plwociny bądź wykluczyć infekcyjne
zapalenie wsierdzia.8
W ramach profilaktyki przeciwzakrzepowej
chory otrzymywał enoksaparynę przez 10 dni.
Istnieją doniesienia z różnych ośrodków, że u chorych na COVID-19 podawanie pośredniej
dawki heparyny drobnocząsteczkowej (HDCz, 1 mg/kg mc. 1 × dz.) poprawiało rokowanie. Efekt
ten wiąże się prawdopodobnie z zapobieganiem
mikrozatorowości płucnej oraz rozsianemu krzepnięciu
wewnątrznaczyniowemu (DIC), które mogą
być następstwem nasilonej reakcji zapalnej towarzyszącej
COVID-19.9 Aktualnie nie ma danych,
które pozwalałyby określić optymalne dawkowanie
HDCz w COVID-19. Polskie Towarzystwo Epidemiologów i Lekarzy Chorób Zakaźnych zaleca
stosowanie HDCzu wszystkich chorych hospitalizowanych,
ale nie wskazuje konkretnego dawkowania
(dawka profilaktyczna czy lecznicza).10
Ze względu na brak poprawy klinicznej oraz
zwiększanie się stężenia CRP w surowicy, progresję
zmian w płucach na RTG oraz konieczność
stosowania tlenoterapii uzasadnione było
zastosowanie remdesiwiru. Lek ten, opracowany
do leczenia gorączki krwotocznej ebola, jest analogiem
adenozyny i jako prolek ulega w komórkach przekształceniu w czynny metabolit konkurujący z naturalnym substratem (ATP) o włączenie
do powstających łańcuchów RNA, przez co hamuje
wirusową polimerazę RNA.11 Był stosowany w wybranych ośrodkach zajmujących się chorymi
na COVID-19 i budził nadzieje na łagodzenie
przebiegu choroby.12 Na początku października
2020 roku opublikowano końcowy raport z badania
ACTT-1 (Adaptive COVID-19 Treatment
Trial), w którym oceniono skuteczność remdesiwiru u 1062 chorych na COVID-19 wymagających
leczenia szpitalnego. Lek ten skracał czas do uzyskania
poprawy (rozumianej jako wypis ze szpitala
lub hospitalizację wyłącznie w celu kontroli
szerzenia się zakażenia) o 5 dni w porównaniu z placebo (p <0,001). Nie uzyskano jednak istotnego
zmniejszenia śmiertelności w grupie leczonej
remdesiwirem (11,4% vs 15,2%).12 W październiku
2020 roku opublikowano również wyniki badania
Solidarity, koordynowanego przez Światową
Organizację Zdrowia (WHO), w którym także
nie stwierdzono istotnego wpływu remdesiwiru
na śmiertelność chorych na COVID-19 i konieczność
rozpoczęcia wentylacji mechanicznej; w przeciwieństwie
do badania ACTT-1 nie obserwowano
natomiast skrócenia czasu hospitalizacji.13,14
Remdesiwir od lipca 2020 roku jest lekiem zarejestrowanym w Unii Europejskiej do leczenia
chorych na COVID-19 wymagających tlenoterapii.
Decyzja o jego ewentualnym zastosowaniu powinna
zostać podjęta na wczesnym etapie choroby, w ciągu kilku pierwszych dni, aby lek mógł wpłynąć
na jej przebieg. Niewątpliwie należy rozważyć
taką terapię u chorych, których stan nie poprawia
się pomimo leczenia objawowego, podawania
tlenu, deksametazonu, a także antybiotyku (przy
podejrzeniu nadkażenia bakteryjnego). Pojedyncza
dawka nasycająca remdesiwiru, jak wspomniano
wcześniej, w 1. dniu terapii wynosi 200 mg, w kolejnych
podaje się 100 mg 1 × dz. Lek ten powinno się
stosować nie krócej niż 5 i nie dłużej niż 10 dni.11,12
Podczas terapii należy monitorować parametry
czynności wątroby. Nie podaje się remdesiwiru
chorym, u których aktywność aminotransferazy
alaninowej (ALT) w surowicy przekracza >5-krotnie
górną granicę normy w danym laboratorium.
Takie zwiększenie aktywności ALT jest wskazaniem
do odstawienia remdesiwiru, nawet jeśli był podawany krócej niż przez 5 dni. Konieczne jest
także monitorowanie stężenia kreatyniny w surowicy,
gdyż eGFR <30 ml/min/1,73 m2 stanowi
przeciwwskazanie do stosowania tego leku z powodu
jego nieznanej farmakokinetyki u takich chorych.15 Z uwagi na niejednoznaczne wyniki
dotyczące skuteczności remdesiwiru w leczeniu
zakażenia SARS-CoV-2 konieczne są dalsze badania
kliniczne.
Piśmiennictwo:
1. Rozporządzenie Ministra Zdrowia z dnia 1 września 2020 r. zmieniające rozporządzenie w sprawie chorób zakaźnych powodujących powstanie obowiązku hospitalizacji, izolacji lub izolacji w warunkach domowych oraz obowiązku kwarantanny lub nadzoru epidemiologicznego. http://isap.sejm.gov.pl/isap.nsf/download.xsp/WDU20 200 001 506/O/ D20 201 506.pdf (dostęp: 1.12.2020)2. Cozzi D., Albanesi M., Cavigli E. i wsp.: Chest X-ray in new Coronavirus Disease 2019 (COVID-19) infection: findings and correlation with clinical outcome.Radiol. Med., 2020; 125: 730–737
3. Xu B., Xing Y., Peng J. i wsp.: Chest CT for detecting COVID-19: a systematic review and meta-analysis of diagnostic accuracy. Eur. Radiol., 2020; 30: 5720–5727
4. Cieszanowski A., Czekajska E., Giżycka B. i wsp.: Wskazania do wykonywania badań obrazowych w zakażeniach SARS-CoV-2 – zalecenia Polskiego Lekarskiego Towarzystwa Radiologicznego. https://pltr.pl/wp-content/uploads/2020/04/2020.04.06-PLTR-COVID-19-Wskazania-do-obrazowania-2.pdf (dostęp: 1.12.2020)
5. Horby P., Lim W.S., Emberson J.R. i wsp.; RECOVERY Collaborative Group: Dexamethasone in hospitalized patients with Covid-19 – preliminary report. N. Engl. J. Med., 2020; 17. doi: 10.1056/NEJMoa2 021 436
6. European Medicine Agency: EMA endorses use of dexamethasone in COVID-19 patients on oxygen or mechanical ventilation. www.ema.europa.eu/en/documents/press-release/ ema-endorses-use-dexamethasone-covid-19-patients-oxygen-mechanical-ventilation_ en.pdf (dostęp: 1.12.2020)
7. Hendaus M.A., Jomha F.A.: Covid-19 induced superimposed bacterial infection. J. Biomol. Struct. Dyn., 2020; 9: 1–7
8. Mantero M., Tarsia P., Gramegna A. i wsp.: Antibiotic therapy, supportive treatment and management of immunomodulation-inflammation response in community acquired pneumonia: review of recommendations. Multidiscip. Respir. Med., 2017; 12: 26
9. Paolisso P., Bergamaschi L., D’Angelo E.C. i wsp.: Preliminary experience with low molecular weight heparin strategy in COVID-19 patients. Front Pharmacol., 2020; 11: 1124
10. Flisiak R., Parczewski M., Horban A. i wsp.: Management of SARS-CoV-2 infection: recommendations of the Polish Association of Epidemiologists and Infectiologists. Annex no. 2 as of October 13, 2020. Pol. Arch. Intern. Med., 2020; 130: 915–918
11. Goldman J.D., LyeD.C.B., Hui D.S. i wsp.: Remdesivir for 5 or 10 days in patients with severe Covid-19. N. Engl. J. Med., 2020; 383: 1827–1837
12. Beigel J.H., Tomashek K.M., Dodd L.E. i wsp.: ACTT-1 Study Group Members. Remdesivir for the treatment of Covid-19 – final report. N. Engl. J. Med., 2020; 383: 1827–1837
13. World Health Organization: “Solidarity” clinical trial for COVID-19 treatments. https:// www.who.int/emergencies/diseases/novel-coronavirus-2019/global-research-on-novel-coronavirus-2019-ncov/ solidarity-clinical-trial-for-covid-19-treatments (dostęp: 1.12.2020)
14. Pan H., Peto R., Karim Q.A. i wsp.: Repurposed antiviral drugs for COVID-19 – interim WHO SOLIDARITY trial results. www.medrxiv.org/content/10.1101/2020.10.15.202098 17v1 (dostęp: 1.12.2020)
15. Charakterystyka produktu leczniczego zawierającego remdesiwir. www.ema.europa. eu/en/documents/product-information/veklury-epar-product-information_pl.pdf (dostęp: 1.12.2020)