Tłumaczyła lek. Iwona Rywczak
Skróty: ACIP – Advisory Committee on Immunization Practices, PCV-7 – skoniugowana 7-walentna szczepionka przeciwko pneumokokom, PCV-13 – skoniugowana 13-walentna szczepionka przeciwko pneumokokom, PPSV-23 – 23-walentna polisacharydowa szczepionka przeciwko pneumokokom
Jakie zalecenia obowiązywały do tej pory?
Aktualnie ACIP zaleca, aby wszystkim dorosłym w wieku ≥65 lat, bez niedoboru odporności, podać obie szczepionki przeciwko pneumokokom – PCV-13 i PPSV-23. ACIP zalecał, aby w pierwszej kolejności podać PCV-13, a po upływie 6–12 miesięcy – PPSV-23, a także, aby dorosłym >65. roku życia, którzy już zostali zaszczepieni PPSV-23, po upływie co najmniej roku podać 1 dawkę PCV-13. W przypadku osób w wieku ≥2 lat, u których istnieją wskazania do szczepienia PCV-13 i PPSV-23 (m.in. dorosłych w wieku ≥65 lat z niedoborem odporności, osób z czynnościową lub anatomiczną asplenią, wszczepionym implantem ślimakowym lub wyciekiem płynu mózgowo-rdzeniowego), PPSV-23 należy podać ≥8 tygodni po PCV-13.
Dlaczego zmieniono obecne zalecenia?
Aby uprościć zalecenia dotyczące stosowania PCV-13 i PPSV-23 u immunokompetentnych dorosłych w wieku ≥65 lat, ACIP zalecił ujednolicenie zalecanych odstępów pomiędzy PCV-13 a PPSV-23 niezależnie od tego, którą szczepionkę podano jako pierwszą.
Jakie są nowe zalecenia?
ACIP zaleca, aby dorosłych w wieku ≥65 lat bez niedoboru odporności zaszczepić przeciwko pneumokokom w schemacie obejmującym podanie 2 szczepionek (PCV-13 i PPSV-23). PCV-13 należy podać jako pierwszą, a po upływie co najmniej roku – PPSV-23. Obu wymienionych szczepionek nie należy podawać podczas jednej wizyty. W przypadku niezamierzonego podania PPSV-23 we wcześniejszym terminie nie należy powtarzać szczepienia PPSV-23.
W Stanach Zjednoczonych aktualnie zarejestrowane są 2 szczepionki przeciwko pneumokokom: skoniugowana 13-walentna (PCV-13 […]) i polisacharydowa 23-walentna (PPSV-23 [w Polsce dostępna jest jeszcze skoniugowana szczepionka 10-walentna przeznaczona dla dzieci do ukończenia 5. rż. – przyp. red.]). Zgodnie z aktualnymi zaleceniami Advisory Committee on Immunization Practices (ACIP), wszystkim dorosłym w wieku ≥65 lat nieszczepionym wcześniej przeciwko pneumokokom oraz osobom, które ukończyły 2. rok życia i należą do grupy ryzyka choroby pneumokokowej, należy podać 1 dawkę PCV-13, a następnie 1 dawkę PPSV-23 (p. tab.).1-4 Zalecane odstępy pomiędzy PCV-13 a PPSV-23 w schemacie szczepienia przeciwko pneumokokom różnią się w zależności od wieku i grupy ryzyka oraz kolejności podania tych 2 szczepionek.1-4
25 czerwca 2015 roku ACIP zmienił zalecany czas podania PPSV-23 jako kolejnej szczepionki po szczepieniu PCV-13 w schemacie stosowanym u immunokompetentnych dorosłych w wieku ≥65 lat (schemat PCV-13–PPSV-23) z 6–12 miesięcy na co najmniej rok. Zalecany odstęp w przypadku pozostałych grup wiekowych i grup ryzyka nie zmienił się. W artykule uzasadniono wprowadzenie tej zmiany i podsumowano dane uwzględnione przez ACIP w procesie tworzenia tego zalecenia.
W sierpniu 2014 roku ACIP zalecił rutynowe szczepienie dorosłych >65. roku życia bez niedoborów odporności 1 dawką PCV-13, a następnie – po upływie 6–12 miesięcy – 1 dawką PPSV-23 (p. Zastosowanie szczepionek przeciwko pneumokokom u dorosłych w wieku ≥65 lat. Wytyczne (2014) ACIP – przyp. red.).1 Osobom w wieku ≥65 lat z niedoborami odporności, bez śledziony (asplenia czynnościowa lub anatomiczna), z wyciekiem płynu mózgowo-rdzeniowego lub wszczepionym implantem ślimakowym zaleca się podać w pierwszej kolejności szczepionkę PCV-13, a następnie – po upływie ≥8 tygodni – PPSV-23.2 ACIP zaleca również, aby wszystkich dorosłych w wieku ≥65 lat, którzy otrzymali w przeszłości PPSV-23, zaszczepić PCV-13 co najmniej rok po szczepieniu PPSV-23 (schemat PPSV-23–PCV-13). Różnica w zalecanych schematach w zależności od kolejności podania poszczególnych preparatów skomplikowała zalecenia i ich realizację. W celu uproszczenia zaleceń ACIP dokonał przeglądu dostępnych danych, szukając podstaw do ujednolicenia zalecanych odstępów pomiędzy podaniem tych szczepionek. Oceniono, czy zgodnie z tymi danymi można zmienić zalecany odstęp w schemacie PCV-13–PPSV-23 przewidziany dla immunokompetentnych dorosłych w wieku ≥65 lat z 6–12 miesięcy na co najmniej rok, tj. odstęp taki sam jak w zalecanym schemacie PPSV-23–PCV-13 dla tej grupy wiekowej.
| Tabela. Zalecane odstępy pomiędzy szczepionkami w zależności od wieku i grupy ryzyka u osób z aktualnymi wskazaniami do szczepienia PCV-13 i PPSV-23 (ACIP, Stany Zjednoczone, wrzesień 2015 r.) | ||||||||
|---|---|---|---|---|---|---|---|---|
| Grupa ryzyka/choroba przewlekła | Odstępy pomiędzy dawkami w schemacie PCV-13–PPSV-23 w zależności od grupy wiekowej | Odstępy pomiędzy dawkami w schemacie PPSV-23–PCV-13 w zależności od grupy wiekowej | ||||||
| 24–71 mies. | 6–18 lat | 19–64 lat | ≥65 lat | 24–71 mies. | 6–18 lat | 19–64 lat | ≥65 lat | |
| brak choroby przewlekłej | ND | ND | ND | ≥1 rok | ND | ND | ND | ≥1 rok |
osoby bez niedoboru odporności:
|
≥8 tyg. | ND | ND | ≥1 rok | ≥8 tyg. | ND | ND | ≥1 rok |
osoby bez niedoboru odporności:
|
≥8 tyg. | ≥8 tyg. | ≥8 tyg. | ≥8 tyg. | ≥8 tyg. | ≥8 tyg. | ≥1 rok | ≥1 rok |
brak śledziony (anatomiczny lub czynnościowy):
|
≥8 tyg. | ≥8 tyg. | ≥8 tyg. | ≥8 tyg. | ≥8 tyg. | ≥8 tyg. | ≥1 rok | ≥1 rok |
osoby z niedoborem odporności:
|
≥8 tyg. | ≥8 tyg. | ≥8 tyg. | ≥8 tyg. | ≥8 tyg. | ≥8 tyg. | ≥1 rok | ≥1 rok |
| 1 Choroby przewlekłe nieuwzględnione w zaleceniach dotyczących dzieci <6. rż. ND – nie dotyczy (schemat szczepienia obejmujący podanie PCV-13 i PPSV-23 nie jest zalecany w tym wieku i w tej grupie ryzyka) | ||||||||
Nie ma badań klinicznych oceniających skuteczność obu szczepionek podanych w ramach jednego schematu, dlatego obecne zalecenia opierają się na najlepszych dostępnych danych pochodzących z badań nad immunogennością. Do opracowania obowiązujących zaleceń szczepień dzieci z niedoborem odporności (www.cdc.gov/vaccines/acip/recs/ grade/pneumo-immuno-child.html [p. Szczepienie przeciwko pneumokokom u dzieci w wieku 6-18 lat z niedoborami odporności – przyp. red.]), dorosłych z niedoborem odporności (www.cdc.gov/vaccines/acip/recs/grade/pneumo-immuno-adults.html [p. Szczepionki przeciwko pneumokokom u dorosłych z niedoborami odporności – przyp. red.]) oraz dorosłych w wieku ≥65 lat (www.cdc.gov/vaccines/acip/recs/grade/pneumo-vac-adult.html) ACIP wykorzystał system Grading of Recommendations, Assessment, Development, and Evaluation (GRADE).1-3 Nie ma nowych danych na temat ujednolicenia odstępów między dawkami, dlatego nie powtarzano procedury przewidzianej w systemie GRADE. Poza tym w badaniach nad immunogennością nie planowano oceniać, jakie powinny być optymalne odstępy między podaniem poszczególnych szczepionek. Jeżeli istnieją wskazania zarówno do podania PCV-13, jak i PPSV-23, w pierwszej kolejności należy podać PCV-13, a następnie PPSV-23 – w badaniach wykazano bowiem lepszą odpowiedź na antygeny typów serologicznych pneumokoka obecnych w obu szczepionkach, gdy jako pierwszą podano szczepionkę skoniugowaną.5-7
Badania oceniające odpowiedź immunologiczną na szczepionkę skoniugowaną (PCV) – 7-walentną (PCV-7) lub PCV-13 oraz szczepionkę polisacharydową (schemat PCV–PPSV-23) podaną po 2, 6 lub 12 miesiącach albo 3–4 latach wykazały, że po szczepieniu PPSV-23 stężenie przeciwciał przeciwko serotypom wspólnym dla obu szczepionek było większe niż przed podaniem szczepionki skoniugowanej.5,6,8-13 W 8 badaniach porównano odpowiedź immunologiczną u dorosłych w wieku ≥50 lat bez niedoboru odporności zaszczepionych w schemacie PCV–PPSV-23 z odpowiedzią na szczepienie wyłącznie PCV lub PPSV-23.5,6,8-13 W 4 badaniach stwierdzono, że dla większości ocenianych typów serologicznych pneumokoka odpowiedź na szczepienie (mierzona za pomocą testu opsonofagocytozy [OPA], stężenia immunoglobulin G [IgG] lub obu tych testów) w schemacie PCV-7–PPSV-23 z zachowaniem 6-miesięcznego odstępu pomiędzy dawkami była lepsza lub taka sama jak odpowiedź na szczepienie samą PCV-7 lub PPSV-23.6,8,11,12 W innym badaniu wykazano, że lepszą odpowiedź immunologiczną uzyskano także w przypadku zachowania rocznego odstępu między szczepionką skoniugowaną a szczepionką polisacharydową (schemat PCV-7–PPSV-23) niż po podaniu pojedynczej dawki PPSV-23.13 W 2 badaniach porównano odpowiedź na szczepienie w schemacie PCV-13–PPSV-23 z odpowiedzią na szczepionkę PCV-13 lub PPSV-23 podaną po roku lub 3–4 latach, wykazując lepszą odpowiedź na większą liczbę serotypów po podaniu drugiej szczepionki 3–4 lata po pierwszej niż w przypadku szczepienia po roku.5,9 W badaniu obejmującym nieszczepionych wcześniej przeciwko pneumokokom rdzennych mieszkańców Alaski w wieku 55–70 lat porównano bezpośrednio odstępy 2- i 6-miesięczne między szczepionkami PCV-7 i PPSV-23. Nie stwierdzono różnic w zakresie odpowiedzi immunologicznej, jednak w grupie zaszczepionej w odstępie 2-miesięcznym częściej obserwowano obrzęk w miejscu wkłucia.10
Podsumowując, w badaniach dotyczących oceny schematu PCV–PPSV-23 u dorosłych bez niedoborów odporności wykazano, że: (1) krótsze odstępy (np. 8 tyg.) między szczepionkami, w porównaniu z dłuższymi odstępami, mogą zwiększać częstość występowania miejscowych niepożądanych odczynów poszczepiennych; (2) dłuższe odstępy (np. co najmniej rok) między szczepionkami mogą się przyczyniać do uzyskania lepszej odpowiedzi immunologicznej na antygeny typów serologicznych wspólnych dla obu szczepionek niż w przypadku szczepienia pojedynczą dawką PCV-13 lub PPSV-23. Poza tym zmiana zalecanego odstępu w schemacie PCV-13–PPSV-23 na co najmniej rok pozwoliłaby ujednolicić zalecane odstępy między szczepieniami u immunokompetentnych dorosłych w wieku ≥65 lat, niezależnie od tego, którą szczepionkę podano jako pierwszą (p. ryc.).
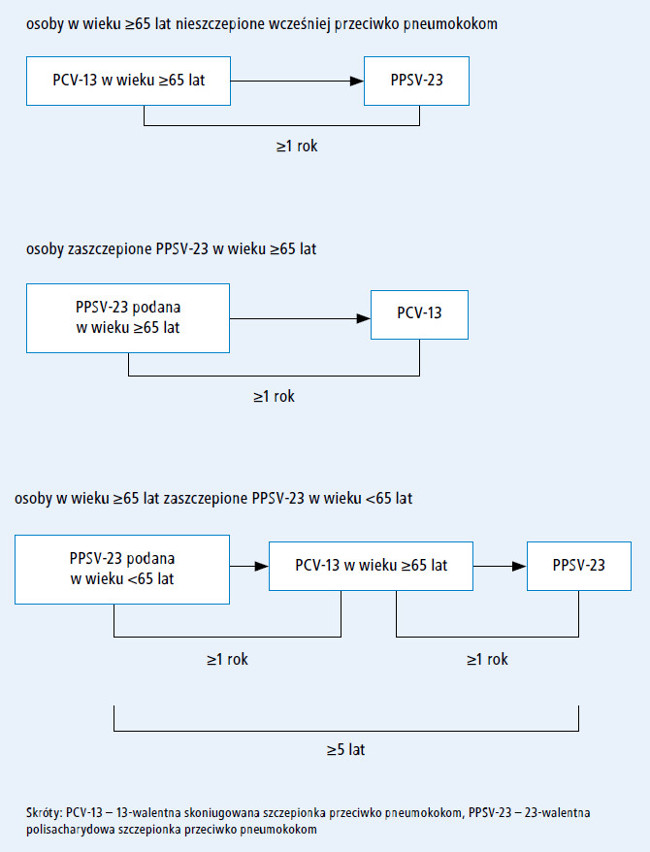
Ryc. Zalecane odstępy
między szczepionkami w schemacie obejmującym
podanie PCV-13 i PPSV-23 u dorosłych w wieku ≥65 lat
bez niedoboru odporności
(ACIP, Stany Zjednoczone)
ACIP rozważał inne czynniki, które mogłyby uzasadnić zmianę schematu szczepienia, takie jak okres ryzyka związany z brakiem ochrony przed typami serologicznymi uwzględnionymi wyłącznie w PPSV-23, czas kolejnej wizyty w placówce wykonującej szczepienia oraz aktualne przepisy Centers for Medicare and Medicaid Services (CMS) umożliwiające refundację 2 szczepionek przeciwko pneumokokom podawanych w ramach jednego schematu w rocznym odstępie. U dorosłych w wieku ≥65 lat 40% zachorowań na inwazyjną chorobę pneumokokową (IChP) wywołują typy serologiczne swoiste dla PPSV-23. Ewentualna zmiana odstępu w schemacie PCV-13–PPSV-23 może dotknąć najmłodsze osoby z tej grupy wiekowej, które prawdopodobnie wcześniej nie były szczepione przeciwko pneumokokom. U tych osób zapadalność na chorobę pneumokokową wywołaną przez typy uwzględnione tylko w PPSV-23 jest najmniejsza.14 (…)
Zalecane odstępy między podaniem PCV-13 i PPSV-23 u osób w wieku ≥2 lat, u których istnieją wskazania medyczne do szczepienia oboma rodzajami szczepionek, pozostają bez zmian (p. tab.). Dzieciom i dorosłym w wieku ≥19 lat z niektórymi chorobami przewlekłymi (w tym również dorosłym >65. rż. z niedoborem odporności, czynnościową lub anatomiczną asplenią, wyciekiem płynu mózgowo-rdzeniowego, wszczepionym implantem ślimakowym) należy podać PPSV-23 ≥8 tygodni po szczepieniu PCV-13. Badania oceniające odpowiedź immunologiczną na PPSV-23 podaną dorosłym zakażonym HIV 4 lub 8 tygodni po szczepieniu PCV-7 wykazały statystycznie istotnie większe stężenie przeciwciał niż po wyłącznym szczepieniu PPSV-23.17,18 Aktualnie zalecany 8-tygodniowy odstęp skraca do minimum okres ryzyka, w którym ta bardzo wrażliwa populacja jest narażona na IChP wywołaną przez typy serologiczne swoiste dla PPSV-23.
Zalecenia ACIP dotyczące odstępów w schemacie szczepienia PCV-13–PPSV-23 u osób >65. roku życia bez niedoboru odporności
W przypadku osób nieszczepionych wcześniej przeciwko pneumokokom zalecenia są następujące: 1 dawkę PPSV-23 należy podać co najmniej rok po podaniu PCV-13. Nie należy podawać tych 2 szczepionek jednocześnie, podczas tej samej wizyty. W przypadku niezamierzonego podania PPSV-23 we wcześniejszym terminie nie należy powtarzać szczepienia PPSV-23.
Zdarzenia niepożądane po podaniu którejkolwiek z tych szczepionek należy zgłaszać do Vaccine Adverse Events Reporting System (VAERS [w polskich warunkach do powiatowych stacji sanitarno-epidemiologicznych – przyp. red.]). (…)
Piśmiennictwo:
1. Tomczyk S., Bennett N.M., Stoecker C., et al.: Use of 13-valent pneumococcal conjugate vaccine and 23-valent pneumococcal polysaccharide vaccine among adults aged ≥65 years: recommendations of the Advisory Committee on Immunization Practices (ACIP). MMWR Morb. Mortal. Wkly Rep., 2014; 63: 822–8252. CDC. Use of 13-valent pneumococcal conjugate vaccine and 23-valent pneumococcal polysaccharide vaccine for adults with immunocompromising conditions: recommendations of the Advisory Committee on Immunization Practices (ACIP). MMWR Morb. Mortal. Wkly Rep., 2012; 61: 816–819
3. CDC. Use of 13-valent pneumococcal conjugate vaccine and 23-valent pneumococcal polysaccharide vaccine among children aged 6–18 years with immunocompromising conditions: recommendations of the Advisory Committee on Immunization Practices (ACIP). MMWR Morb. Mortal. Wkly Rep., 2013; 62: 521–524
4. Nuorti J.P., Whitney C.G.: Prevention of pneumococcal disease among infants and children – use of 13-valent pneumococcal conjugate vaccine and 23-valent pneumococcal polysaccharide vaccine – recommendations of the Advisory Committee on Immunization Practices (ACIP). MMWR Recomm. Rep., 2010; 59 (No. RR-11): 1–18
5. Greenberg R.N., Gurtman A., Frenck R.W., et al.: Sequential administration of 13-valent pneumococcal conjugate vaccine and 23-valent pneumococcal polysaccharide vaccine in pneumococcal vaccine-naive adults 60–64 years of age. Vaccine, 2014; 32: 2364–2374
6. Musher D.M., Rueda A.M., Nahm M.H., Graviss E.A., Rodriguez-Barradas M.C.: Initial and subsequent response to pneumococcal polysaccharide and protein-conjugate vaccines administered sequentially to adults who have recovered from pneumococcal pneumonia. J. Infect. Dis., 2008; 198: 1019–1027
7. Blum M.D., Dagan R., Mendelman P.M., et al.: A comparison of multiple regimens of pneumococcal polysaccharide-meningococcal outer membrane protein complex conjugate vaccine and pneumococcal polysaccharide vaccine in toddlers. Vaccine, 2000; 18: 2359–2367
8. Goldblatt D., Southern J., Andrews N., et al.: The immunogenicity of 7-valent pneumococcal conjugate vaccine versus 23-valent polysaccharide vaccine in adults aged 50–80 years. Clin. Infect. Dis., 2009; 49: 1318–1325
9. Jackson L.A., Gurtman A., van Cleeff M., et al.: Influence of initial vaccination with 13-valent pneumococcal conjugate vaccine or 23-valent pneumococcal polysaccharide vaccine on anti-pneumococcal responses following subsequent pneumococcal vaccination in adults 50 years and older. Vaccine, 2013; 31: 3594–3602
10. Miernyk K.M., Butler J.C., Bulkow L.R., et al.: Immunogenicity and reactogenicity of pneumococcal polysaccharide and conjugate vaccines in Alaska native adults 55–70 years of age. Clin. Infect. Dis., 2009; 49: 241–248
11. Lazarus R., Clutterbuck E., Yu L.M., et al.: A randomized study comparing combined pneumococcal conjugate and polysaccharide vaccination schedules in adults. Clin. Infect. Dis., 2011; 52: 736–742
12. Macintyre C.R., Ridda I., Gao Z., et al.: A randomized clinical trial of the immunogenicity of 7-valent pneumococcal conjugate vaccine compared to 23-valent polysaccharide vaccine in frail, hospitalized elderly. PLoS One, 2014; 9: e94 578.
13. de Roux A., Schmöle-Thoma B., Siber G.R., et al.: Comparison of pneumococcal conjugate polysaccharide and free polysaccharide vaccines in elderly adults: conjugate vaccine elicits improved antibacterial immune responses and immunological memory. Clin. Infect. Dis., 2008; 46: 1015–1023
14. CDC. Active bacterial core surveilance (ABCs). Atlanta, GA: US Department of Health and Human Services, CDC; 2013. Available from: http://www.cdc.gov/abcs/reports-findings/ survreports/spneu13.html.
15. Blackwell D.L., Lucas J.W., Clarke T.C.: Summary health statistics for US adults: national health interview survey, 2012. Vital Health Stat 10, 2014; 10: 1–161
16. Centers for Medicare and Medicaid Services. Modifications to Medicare part B coverage of pneumococcal vaccinations. Washington, DC: Department of Health and Human Services, Centers for Medicare and Medicaid Services; 2014. Available at https://www. cms.gov/Outreach-and-Education/Medicare-Learning-Network-MLN/MLNMattersArticles/ Downloads/MM9051.pdf Adobe PDF fileExternal Web Site Icon.
17. Feikin D.R., Elie C.M., Goetz M.B., et al.: Randomized trial of the quantitative and functional antibody responses to a 7-valent pneumococcal conjugate vaccine and/or 23-valent polysaccharide vaccine among HIV-infected adults. Vaccine, 2001; 20: 545–553
18. Lesprit P., Pédrono G., Molina J.M., et al.: Immunological efficacy of a prime-boost pneumococcal vaccination in HIV-infected adults. AIDS, 2007; 21: 2425–2434















