Skróty: CYD-TDV (chimeric yellow fever-dengue tetravalent dengue vaccine) – chimeryczna, 4-walentna szczepionka przeciwko dendze z rdzeniem wirusa żółtej gorączki, DENV (dengue virus) – wirus dengi, IHR (International Health Regulations) – Międzynarodowe Przepisy Zdrowotne, JE – japońskie zapalenie mózgu, YEL-AND (yellow fever vaccine-associated neurotropic disease) – choroba neurotropowa związana ze szczepieniem, YEL-AVD (yellow fever vaccine-associated viscerotropic disease) – choroba trzewna związana ze szczepieniem, YFV (yellow fever virus) – wirus żółtej gorączki
Wprowadzenie
Komary są wektorami wielu chorób zakaźnych o różnorodnej etiologii. Gatunki, które są zdolne do przenoszenia chorób zakaźnych, należą do trzech głównych rodzajów: Anopheles, Aedes i Culex. Wśród chorób wirusowych, dla których wektorem jest komar, należy wymienić: chikungunyę, żółtą gorączkę, dengę, japońskie zapalenie mózgu, zapalenie mózgu La Crosse, wschodnie końskie zapalenie mózgu, gorączkę Zachodniego Nilu oraz zikę. Chorobą pierwotniakową przenoszoną przez komary jest malaria. Komary potrafią nawet przenosić choroby wywoływane przez pasożyty wielokomórkowe – dotyczy to dirofilarioz i filarioz (np. wuchereriozy).
Historia badań nad szczepionkami przeciwko chorobom przenoszonym przez komary jest bardzo długa. Próby opracowania szczepionki przeciwko żółtej gorączce rozpoczęto w 1912 roku, a do użycia wprowadzono ją 26 lat później. Pracę nad jej wynalezieniem zwieńczono przyznaniem Nagrody Nobla, którą w 1951 roku otrzymał Max Theiler.1 Natomiast pierwsze próby uodpornienia przeciwko japońskiemu zapaleniu mózgu sięgają czasów II wojny światowej.2 Przeciwko wielu chorobom niestety do tej pory nie udało się opracować skutecznej szczepionki i aktualnie w medycynie podróży rutynowo stosuje się tylko 2 szczepionki zapobiegające chorobom przenoszonym przez komary – przeciwko żółtej gorączce i japońskiemu zapaleniu mózgu. Pozostałe dostępne preparaty (np. przeciwko malarii i dendze), choć są dostępne w regionach endemicznych, właściwie nie mają zastosowania u osób podróżujących z krajów europejskich do tropików.
Żółta gorączka
Żółta gorączka należy do grupy wirusowych gorączek krwotocznych, wywoływanych przez wirusa żółtej gorączki (yellow fever virus – YFV), należącego do RNA wirusów z rodzaju Flavivirus. Infekcje YFV występują w tropikalnej części Afryki oraz Ameryki Południowej i Środkowej, a rezerwuar wirusa stanowią ssaki naczelne – ludzie i małpy. Do zakażenia dochodzi przez ukłucia komarów, głównie z rodzaju Aedes lub Haemagogus (rzadko).
Wyróżnia się 3 cykle transmisji YFV:
- leśny, w którym wirus jest przenoszony między małpami a komarami bytującymi w dżungli tropikalnej (bez udziału człowieka). Brak doniesień o zachorowaniach wśród ludzi na takich terenach nie jest równoznaczny z brakiem zagrożenia żółtą gorączką. Człowiek może ulec zakażeniu podczas podróży do lasów tropikalnych, w których zachodzi transmisja YFV.
- miejski, w którym wirus jest przenoszony między ludźmi, głównie z udziałem komarów z gatunku Aedes aegypti
- pośredni (sawannowy), zachodzący w Afryce na pograniczu lasów tropikalnych, w którym wirus jest przenoszony z małp na ludzi oraz między ludźmi przez komary z rodzaju Aedes spp.3
Istnieje teoretyczne ryzyko przeniesienia zakażenia między ludźmi drogą krwiopochodną, jednak dotychczas nie opisano takiego przypadku.
Szacuje się, że ryzyko zachorowania osoby nieuodpornionej wynosi 50/100 000 w ciągu 2-tygodniowego pobytu w Afryce oraz 5/100 000 w ciągu 2-tygodniowego pobytu w Ameryce Południowej.4 Są to wartości orientacyjne, oparte na danych dotyczących ryzyka zachorowania w populacjach zamieszkujących regiony endemiczne w porze zwiększonej transmisji YFV. Trudno ocenić dokładnie, jakie jest ryzyko zarażenia żółtą gorączką u podróżnych, ponieważ zależy ono od wielu czynników, takich jak intensywność transmisji w regionie docelowym, charakter podróży i związana z tym eskpozycja na ukłucia komarów, a także stosowanie przez podróżnych środków ochrony przed owadami. Największe ryzyko zakażenia obserwuje się w porze deszczowej, zwłaszcza pod koniec tego okresu oraz na przełomie pory deszczowej i suchej. W Ameryce Południowej okres ten przypada od stycznia do maja, a w Afryce Zachodniej – od sierpnia do października. Epidemie żółtej gorączki, zwłaszcza związane z transmisją w cyklu miejskim, mogą jednak występować niezależnie od pory roku.
Okres wylęgania choroby trwa około 3–6 dni od ukłucia komara. Chory w okresie wiremii (pierwsze 3–4 dni po wystąpieniu objawów) może stanowić źródło zakażenia komara.
U większości osób zakażenie YFV przebiega bezobjawowo. U pozostałych osób w pierwszej fazie choroby dominują nietypowe objawy o nagłym początku, w tym gorączka, dreszcze i ból głowy. Część chorych zgłasza ból okolicy krzyżowej, ból mięśni, osłabienie, nudności, wymioty i zawroty głowy. Najczęściej w ciągu kilku dni stan zdrowia zakażonych poprawia się. U około 15% chorych w ciągu 48 h po ustąpieniu objawów dochodzi do nawrotu i progresji choroby. W tej fazie zakażenia zwykle obserwuje się gorączkę, nudności i wymioty, ból nadbrzusza, żółtaczkę oraz objawy niewydolności nerek. W zakażeniach o ciężkim przebiegu występują krwawienia z błon śluzowych oraz miejsc wkłuć, niewydolność wielonarządowa i wstrząs, ze śmiertelnością 30–60%, a u nieodpornych podróżnych nawet do 80%.5
Szczepienie przeciwko żółtej gorączce
Szczepionka przeciwko żółtej gorączce jest stosowana od wielu lat i stanowi bezpieczną oraz skuteczną formę profilaktyki tej choroby. Jest to preparat „żywy”, atenuowany, zawierający szczep 17 D-204 YFV namnożony na zarodkach kurzych.6 Szczepienie przeciwko żółtej gorączce jest zalecane dorosłym i dzieciom w wieku ≥9 miesięcy przed podróżą do regionów w Ameryce Południowej i Środkowej oraz Afryce, w których występuje transmisja wirusa (p. tab. 1.). Ponadto, wiele krajów wymaga tego szczepienia od podróżnych na podstawie Międzynarodowych Przepisów Zdrowotnych (International Health Regulations – IHR) Światowej Organizacji Zdrowia (WHO).
| Tabela 1. Kraje, w których istnieje ryzyko zakażenia wirusem żółtej gorączkia,b | |
|---|---|
| Afryka | Angola, Burundi, Benin, Burkina Faso, Kamerun, Republika Środkowoafrykańska, Czad, Kongo, Republika Wybrzeża Kości Słoniowej, Demokratyczna Republika Kongo, Gwinea Równikowa, Etiopia, Gabon, Gambia, Ghana, Gwinea, Gwinea–Bissau, Kenia, Liberia, Mali, Mauretania, Niger, Nigeria, Senegal, Sierra Leone, Południowy Sudan, Sudan, Togo, Uganda |
| Ameryka Południowa | Argentyna, Boliwia, Brazylia, Kolumbia, Ekwador, Gujana Francuska, Gujana, Panama, Paragwaj, Peru, Surinam, Trynidad i Tobago, Wenezuela |
| a Opracowano na podstawie 7. pozycji piśmiennictwa. b Boldem zaznaczono kraje, w których szczepienie jest obowiązkowe dla wszystkich przybywających osób, o ile nie występują przeciwwskazania do podania szczepionki. W pozostałych krajach szczepienie może być obowiązkowe dla osób przybywających bezpośrednio z innych państw zagrożonych żółtą gorączką, a szczegółowe wymogi zależą od dokładnej trasy podróży. Kraje, w których występuje małe ryzyko ekzpozycji na zakażenie YFV i szczepienie nie jest zwykle zalecane, to: Erytrea, Ruanda, Somalia, Tanzania i Zambia. | |
W zależności od trasy wyjazdu szczepienie przeciwko żółtej gorączce może być:
- obowiązkowe
- u wszystkich podróżujących do kilkunastu krajów Afryki i Ameryki Południowej, jeśli nie występują przeciwwskazania do podania szczepionki
- u osób opuszczających rejony występowania żółtej gorączki i przybywających do niektórych krajów potencjalnie zagrożonych transmisją YFV; takie wymagania dotyczą podróżnych przekraczających granice państwowe w Afryce i Ameryce Południowej lub Środkowej, a także udających się z tych regionów do krajów położonych w tropikalnej części Azji oraz do Australii
- zalecane osobom udającym się do regionów zagrożonych żółtą gorączką w Afryce i Ameryce Południowej niezależnie od tego, czy są one objęte obowiązkiem szczepień.
Od 2011 roku WHO oraz CDC regularnie publikują zalecenia dotyczące szczepienia przeciwko żółtej gorączce przed wyjazdem do poszczególnych krajów uwzględniające trzy kategorie: szczepienie może być zalecane, generalnie niezalecane lub niezalecane przed podróżą do danego kraju lub regionu (p. tab. 2.).7 Kategorie te uwzględniają ryzyko zakażenia YFV w danym regionie świata, a w niektórych sytuacjach także charakter podróży i związaną z tym ekspozycję na ukłucia komarów przenoszących żółtą gorączkę.
| Tabela 2. Kategorie zaleceń dotyczące szczepienia przeciwko żółtej gorączce przed podróżą według WHO oraz CDCa | |
|---|---|
| Kategoria | Wyjaśnienie |
| zalecane | – regiony endemicznego występowania żółtej gorączki lub regiony o pośrednim ryzyku (na tych terenach stwierdza się stałą lub okresową
transmisję YFV) – szczepienie zalecane wszystkim podróżnym, u których nie stwierdza się przeciwwskazań |
| generalnie niezalecane | – rejony o małym ryzyku ekspozycji na zakażenie YFV, w których obecnie nie
występują zachorowania, a w przeszłości obserwowano jedynie małe
nasilenie transmisji wirusa – zwykle szczepienie nie jest zalecane – szczepienie można jednak rozważyć u niewielkiej grupy podróżnych szczególnie narażonych na zakażenie w związku z długotrwałą podróżą w tym regionie, bardzo dużą ekspozycję na ukłucia komarów lub brak możliwości ochrony przed nimi w trakcie podróży |
| niezalecane | – szczepienie nie jest potrzebne (rejony wolne od ryzyka żółtej gorączki, w których nie stwierdzano transmisji wirusa żółtej gorączki w przeszłości oraz obecnie lub warunki środowiskowe nie pozwalają na transmisję) |
| a Opracowano na podstawie 7. pozycji piśmiennictwa. CDC – Centers for Disease Control and Prevention, YFV – wirus żółtej gorączki, WHO – Światowa Organizacja Zdrowia | |
Dostępny preparat i dawkowanie
Obecnie szczepienia przeciwko żółtej gorączce są jako jedyne objęte regulacjami IHR opracowanymi w 2005 roku przez WHO, zgodnie z którymi szczepienie należy przeprowadzać wyłącznie przy użyciu preparatów posiadających akceptację WHO.8 Dostępna w Polsce szczepionka przeciwko żółtej gorączce („żywa”, atenuowana, zawierająca szczep 17 D-204 [preparat Stamaril]) taką akceptację posiada.
Szczepienie podstawowe obejmuje podanie 1 dawki podskórnie (s.c.) lub domięśniowo (i.m.). U większości osób zapewnia ono odporność na wiele
lat. W indywidualnych przypadkach, w razie
niewystarczającej odpowiedzi immunologicznej
po szczepieniu podstawowym, po 10 latach należy
podać dawkę przypominającą. Zalecenie to
dotyczy:
– kobiet przed kolejną podróżą do regionów zagrożonych
żółtą gorączką, które otrzymały szczepionkę w czasie ciąży
– osób przed kolejną podróżą po przeszczepieniu
krwiotwórczych komórek macierzystych, o ile
nie stwierdza się u nich zaburzeń odporności
stanowiących przeciwwskazanie do szczepienia
– osób zakażonych ludzkim wirusem niedoboru
odporności (HIV) w razie utrzymywania się narażenia
na zakażenie wirusem żółtej gorączki
(szczepienie co 10 lat).
Zgodnie z zaleceniami Advisory Committee on Immunization Practices (ACIP) szczepienie przypominające można także rozważyć u podróżnych, u których minęło ≥10 lat od podania ostatniej dawki szczepionki, planujących wyjazd obarczony szczególnie dużym ryzykiem zakażenia wirusem żółtej gorączki ze względu na trasę, porę roku, planowane aktywności oraz długość pobytu w regionie zagrożonym (np. długi pobyt na terenach wiejskich Afryki Zachodniej w porze deszczowej lub podróż do regionu, w którym występuje ognisko epidemii żółtej gorączki).9 Według WHO szczepienie przypominające nie powinno stanowić warunku przekroczenia granic państwowych.
Kwalifikacja do szczepienia
Kwalifikacja do szczepienia przeciwko żółtej gorączce przed wyjazdem zagranicznym powinna uwzględniać:
- ryzyko zakażenia w danym regionie świata
- przewidywaną ekspozycję na ukłucia komarów
- konsekwencje kliniczne w razie zachorowania
- wymogi wynikające z przepisów
- ryzyko rzadkich, ciężkich niepożądanych odczynów poszczepiennych (NOP).
W celu zminimalizowania ryzyka NOP szczepienie przeciwko żółtej gorączce przed podróżą należy przeprowadzać wyłącznie u osób, które planują podróż na tereny zagrożone tą chorobą lub objęte są obowiązkiem szczepień ze względu na trasę podróży. Należy również ocenić, czy u danego pacjenta występują przeciwwskazania do szczepienia przeciwko żółtej gorączce lub okoliczności wymagające szczególnej ostrożności przy kwalifikacji do podania szczepionki, w tym związane z wiekiem pacjenta (p. tab. 3.).4, 10
| Tabela 3. Przeciwwskazania do szczepienia przeciwko żółtej gorączce oraz sytuacje wymagające szczególnej ostrożnościa | |
|---|---|
| Przeciwwskazania | Sytuacje wymagające szczególnej ostrożności |
| nadwrażliwość na składniki szczepionki wiek <6. mż. zakażenie wirusem HIV: objawowe lub z CD4 <200/mm3 (lub <15% u dzieci <6. rż.) choroby grasicy lub stan po tymektomii pierwotne niedobory odporności nowotwory złośliwe stan po przeszczepieniu narządów leczenie immunosupresyjne lub immunomodulujące | wiek 6.–8. mż. wiek ≥60. rż. bezobjawowe zakażenie HIV z CD4 200–499/mm3 (lub 15–24% u dzieci <6. rż.) ciąża karmienie piersią |
| a Opracowano na podstawie 4. i 10. pozycji piśmiennictwa. HIV – ludzki wirus niedoboru odporności, mż. – miesiąc życia, rż. – rok życia | |
Wskazania i przeciwwskazania
Szczepienie przeciwko żółtej gorączce przed podróżą stosuje się u dzieci od 9. miesiąca życia. W przypadku szczególnie dużego ryzyka zakażenia YFV podczas nieuniknionej podróży dopuszczalne jest szczepienie niemowląt w wieku 6–8 miesięcy. Nie należy szczepić dzieci w wieku <6. miesiąca życia ze względu na zwiększone ryzyko ciężkich, neurologicznych NOP. Wiek od 60. roku życia nie stanowi przeciwwskazania do szczepienia przeciwko żółtej gorączce, ale jest czynnikiem zwiększonego ryzyka ciężkich NOP, takich jak związana ze szczepieniem choroba trzewna (yellow fever vaccine-associated viscerotropic disease – YEL-AVD) oraz związana ze szczepieniem choroba neurotropowa (yellow fever vaccine-associated neurotropic disease – YEL-AND). Z tego powodu pacjentów ≥60. roku życia należy kwalifikować do szczepienia przeciwko żółtej gorączce bardzo ostrożnie, po starannej analizie przepisów obowiązujących w kraju docelowym oraz ryzyka ekspozycji na YFV w trakcie podróży. Szczepienie przeciwko żółtej gorączce jest bezwzględnie przeciwwskazane u osób po tymektomii oraz z chorobami grasicy. Zaburzenia czynności grasicy lub stan po tymektomii są czynnikiem ryzyka rozwoju YEL-AVD. Na świecie bardzo dobrze udokumentowano ciężkie NOP, w tym zgony u pacjentów z chorobami grasicy zaszczepionych przeciwko żółtej gorączce.11,12
Ciąża nie jest bezwzględnym przeciwwskazaniem do szczepienia przeciwko żółtej gorączce, ale jak dotąd nie przeprowadzono dużych, prospektywnych badań oceniających bezpieczeństwo takiego postępowania u ciężarnych. Dostępne wyniki obserwacji retrospektywnych wskazują, że szczepienie matki podczas ciąży nie zwiększa ryzyka dużych wad płodu, natomiast dane dotyczące ryzyka poronień u kobiet zaszczepionych podczas ciąży są niespójne i nie pozwalają wyciągnąć jednoznacznych wniosków. Wykazano, że odpowiedź serologiczna na szczepionkę przeciwko żółtej gorączce jest zmniejszona u ciężarnych, zwłaszcza w przypadku szczepienia w III trymestrze. Szczepienie przeciwko żółtej gorączce u kobiet ciężarnych przed podróżą można rozważyć wyłącznie w razie nieuniknionego wyjazdu na tereny szczególnie zagrożone tą chorobą. U kobiet planujących ciążę ACIP zaleca 4-tygodniowy odstęp między przyjęciem szczepionki przeciwko żółtej gorączce a poczęciem. U kobiet karmiących piersią szczepienie przeciwko żółtej gorączce może być zalecane tylko w wyjątkowych sytuacjach z uwagi na opisane w piśmiennictwie 3 przypadki YEL-AND u noworodków karmionych piersią, których matki zaszczepiono przeciwko żółtej gorączce.13 Niektórzy eksperci zalecają, aby kobiety karmiące piersią, które zaszczepiono w związku z nieuniknioną podróżą do regionów zagrożonych tą chorobą, przerwały karmienie na ≥2 tygodnie, utrzymując laktację.
Szczególnym przeciwwskazaniem do szczepienia przeciwko żółtej gorączce jest alergia na białko jaja kurzego. Zawartość owoalbuminy w dostępnych preparatach waha się w granicach 2,43–4,42 µg/ml.14 Z tego powodu generalnie szczepionka ta jest przeciwwskazana u osób z alergią na białka jaja kurzego. Jednak istnieją ograniczone dowody na bezpieczeństwo stosowania tej szczepionki z zachowaniem szczególnych środków ostrożności, takich jak podanie preparatu w kilku krokach, zaczynając od wstrzyknięcia minimalnej dawki śródskórnie (p. także Czy szczepienie przeciwko żółtej gorączce było bezpieczne u osób z alergią na białko jaja kurzego? – przyp. red.).15 Jeśli ryzyko zachorowania na żółtą gorączkę jest bardzo duże (np. planowany jest pobyt stały w rejonie endemicznym), a pacjenta potwierdzono alergię na białko jaja kurzego, można rozważać podanie szczepionki w warunkach szpitalnych, zachowując ekstremalną ostrożność, w asyście anestezjologa, oraz zapewniając możliwość obserwacji pacjenta co najmniej przez kilkanaście godzin po szczepieniu.
Dokumentacja szczepienia
Sposób dokumentacji szczepienia przeciwko żółtej gorączce regulują zapisy w IHR opracowanych przez WHO, a w Polsce także Rozporządzenie Ministra Zdrowia w sprawie wykazu zalecanych szczepień ochronnych oraz sposobu finansowania i dokumentowania zalecanych szczepień ochronnych wymaganych międzynarodowymi przepisami zdrowotnymi.16 Wykonanie szczepienia przeciwko żółtej gorączce należy potwierdzić wpisem do Międzynarodowej Książeczki Szczepień (International Certificate of Vaccination or Prophylaxis). Wzór Międzynarodowej Książeczki Szczepień stanowi załącznik nr 2 do wymienionego powyżej Rozporządzenia. Zgodnie z aktualizacją IHR przygotowaną w 2016 roku przez WHO, wpis uzyskuje ważność 10 dni po podaniu szczepionki i zachowuje ją na całe życie osoby zaszczepionej (p. ryc. 1.).17 Dotyczy to także szczepień wykonanych w przeszłości, przed zmianą przepisów w 2016 roku.
W razie przeciwwskazań do podania szczepionki u osoby udającej się do kraju objętego obowiązkiem uodpornienia przeciwko żółtej gorączce, IHR dopuszcza możliwość wystawienia przez lekarza zaświadczenia zwalniającego podróżnego z tego obowiązku. Zaświadczenie, wystawione w języku angielskim lub francuskim, jest ważne w odniesieniu do danej podróży i w określonym przedziale czasu. IHR nie przedstawia wzorca takiego dokumentu, nie istnieją również spójne, międzynarodowe wytyczne określające formę listu. W niektórych krajach (m.in. w Kanadzie i Wielkiej Brytanii) narodowe instytucje zdrowia publicznego opracowały obowiązujący wzór dokumentu zwalniającego ze szczepienia. Służby sanitarne państw docelowych powinny respektować zwolnienie ze szczepienia przeciwko żółtej gorączce. Podróżnego zwolnionego ze szczepienia przeciwko żółtej gorączce ze względu na przeciwwskazania do jej podania należy poinformować o ryzyku i konsekwencjach zachorowania, jak również konieczności rygorystycznego stosowania środków ochrony przed ukłuciami komarów przenoszących tę chorobę podczas podróży (repelenty, odzież ochronna, insektycydy, moskitiera nadłóżkowa lub korzystanie z klimatyzowanych pomieszczeń).
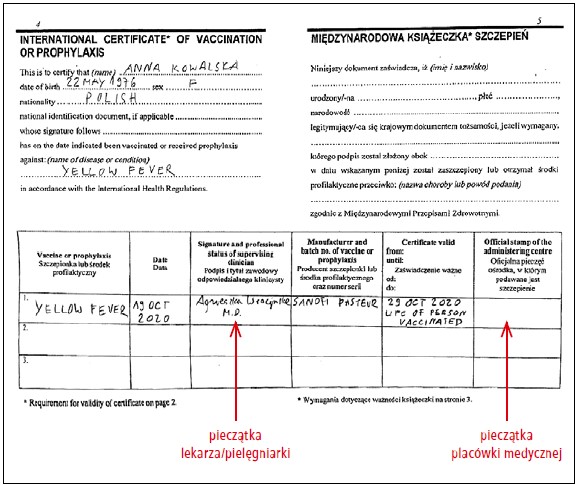
Ryc. 1. Przykładowy wpis do Międzynarodowej Książeczki Szczepień potwierdzający szczepienie przeciwko żółtej gorączce przed podróżą.
Skuteczność szczepienia i ryzyko NOP
Szczepienie przeciwko żółtej gorączce zapewnia ochronę przed zachorowaniem u 80–100% osób w ciągu 10 dni po podaniu szczepionki i u >99% 30 dni po szczepieniu. Większość osób dobrze toleruje szczepienie, na ogół obserwuje się łagodne miejscowe i uogólnione NOP. U 10–30% pacjentów w ciągu 10 dni po szczepieniu występują łagodne odczyny ogólnoustrojowe, takie jak gorączka, ból głowy i mięśni, które mogą się utrzymywać przez kilka dni. Ryzyko anafilaksji ocenia się na 1,3/100 000 podanych dawek i jest największe u osób w wieku ≤18 lat. Do bardzo rzadkich, ciężkich NOP swoistych dla szczepionki przeciwko żółtej gorączce należy YEL-AVD oraz YEL-AND.
Objawy YEL-AVD najczęściej pojawiają się w ciągu 10 dni po szczepieniu i przypominają zakażenie dzikim wirusem żółtej gorączki o ciężkim przebiegu. U niektórych osób rozwija się niewydolność wielonarządowa. Śmiertelność w przebiegu YEL-AVD wynosi około 60%. Dotychczas na całym świecie zgłoszono >100 przypadków YEL-AVD. Ryzyko wystąpienia tego odczynu szacuje się na 0,3/100 000 podanych dawek szczepionki. Czynnikiem zwiększonego ryzyka YEL-AVD jest wiek ≥60 lat (1,2/100 000 podanych dawek) oraz zaburzenia czynności grasicy. W przebiegu YEL-AND w ciągu 30 dni po szczepieniu przeciwko żółtej gorączce rozwijają się powikłania neurologiczne, w tym m.in. zapalenie opon mózgowo-rdzeniowych i mózgu, zespół Guillaina i Barrégo oraz porażenie nerwów czaszkowych. Szacuje się, że ogółem ryzyko YEL-AND wynosi 0,8/100 000 podanych dawek i jest większe u osób w wieku ≥60 lat (2,2/100 000 podanych dawek) oraz u niemowląt <9. miesiąca życia.18
Japońskie zapalenie mózgu
Wirus japońskiego zapalenia mózgu (japanese encephalitis – JE), podobnie jak wirus dengi, żółtej gorączki i gorączki Zachodniego Nilu, należy do rodziny Flaviviridae. Wektorem wirusa JE są komary należące do rodzaju Culex. Rezerwuarem są kręgowce – przede wszystkim świnie i ptaki brodzące. Człowiek jest zasadniczo gospodarzem przypadkowym i zazwyczaj nie ma znaczenia w cyklu rozwojowym wirusa.19
Okres wylęgania JE wynosi około 5–15 dni. Znamienne jest to, że objawy choroby rozwijają się u nielicznych osób (1%). Początkowo pojawia się gorączka, ból głowy i wymioty, a w kolejnych dniach występują typowe objawy zapalenia mózgu, czyli zaburzenia neurologiczne, jakościowe zaburzenia świadomości, zaburzenia ruchu i drgawki. Rokowanie w przypadkach objawowych jest niepomyślne – u 30% osób z zapaleniem mózgu dochodzi do zgonu, a u 30–50% stwierdza się trwałe powikłania neurologiczne.
Zachorowania występują sezonowo – zazwyczaj w trakcie pory deszczowej lub tuż po jej zakończeniu. W niektórych regionach Azji obserwuje się całoroczną transmisję wirusa JE. Najczęściej chorują osoby przebywające na terenach pozamiejskich w pobliżu obszarów wilgotnych (np. pól ryżowych).20
Wirus JE jest najczęstszą przyczyną wirusowego zapalenia mózgu w państwach azjatyckich. Do krajów endemicznych JE należą 24 kraje Azji Południowo-Wschodniej i regionu Zachodniego Pacyfiku (p. ryc. 2.). Rocznie na świecie notuje się około 68 000 zachorowań na JE, przy czym najwięcej przypadków występuje w Chinach, Birmie, Tajlandii, Wietnamie, Kambodży, Laosie, Nepalu, Indiach, Filipinach, Sri Lance, Malezji i Indonezji. Mimo nazwy JE obecnie rzadko występuje w Japonii dzięki programom masowych szczepień ochronnych.21 W krajach endemicznych na JE chorują przede wszystkim dzieci (większość dorosłych nabywa odporność w dzieciństwie). Natomiast w przypadku osób podróżujących z krajów, w których JE nie występuje, choroba ta dotyczy wszystkich grup wiekowych, jednak objawowe zakażenie JE obserwuje się bardzo rzadko. Szacuje się, że ryzyko zachorowania wynosi <1/1 000 000 podróżujących, ale zwiększa się w przypadku dłuższych pobytów – oceniono, że jest ono podobne do ryzyka w populacji pediatrycznej zamieszkującej tereny endemiczne i wynosi 6–11/100 000/rok.19
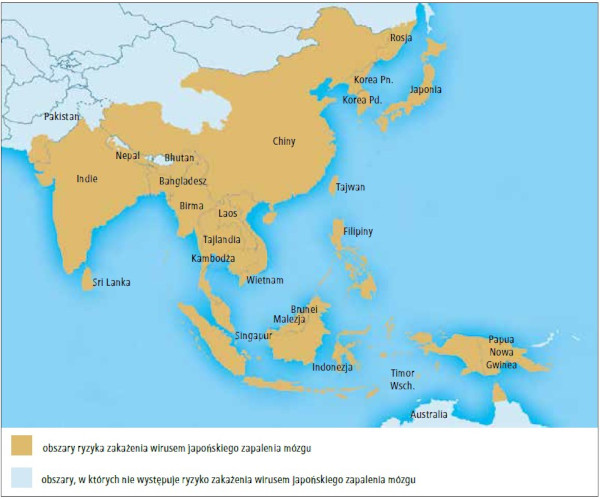
Ryc. 2. Regiony endemicznego występowania japońskiego zapalenia mózgu.
Szczepienie przeciwko japońskiemu zapaleniu mózgu
Na świecie dostępnych jest kilka szczepionek przeciwko JE przeznaczonych do stosowania zarówno w regionach endemicznych JE, jak i u osób podróżujących do krajów występowania JE. Są wśród nich preparaty inaktywowane, namnażane na komórkach mózgów myszy lub hodowlach komórkowych, „żywe” szczepionki atenuowane oraz szczepionka chimeric wytwarzana na żywym, atenuowanym wirusie żółtej gorączki (szczep 17D). Wszystkie dostępne szczepionki oparte są na genotypie III wirusa JE, ale są skuteczne również wobec innych genotypów i szczepów wirusa.22
Niektóre kraje azjatyckie wprowadziły szczepienie przeciwko JE do powszechnych programów szczepień obowiązkowych u dzieci (np. Chiny, Indie, Korea, Sri Lanka, Tajlandia).23 W ramach tych programów stosuje się szczepionkę „żywą”, atenuowaną, opartą na szczepach wirusa SA 14-14-2. Jest to inny preparat niż stosowany w medycynie podróży (p. niżej). Istnieją dowody na to, że już 1 dawka tej szczepionki generuje długotrwałą odporność na zakażenie wirusem, choć w niektórych krajach stosuje się więcej dawek – na przykład w Chinach pierwszą dawkę szczepienia podaje się podskórnie w wieku 8 miesięcy, a dawkę przypominającą w wieku 2 lat (w niektórych regionach stosuje się jeszcze jedną dawkę w wieku 6–7 lat).24,25 W Japonii w ramach szczepień powszechnych stosuje się inaktywowaną (zabitą) szczepionkę przeciwko JE namnażaną na mózgach mysich.25
W medycynie podróży stosuje się szczepionkę inaktywowaną opartą na szczepie SA 14-14-2, namnożonym na komórkach Vero, adsorbowanym na wodorotlenku glinu (preparat Ixiaro). Szczepionka jest dostępna w Stanach Zjednoczonych, Europie, Kanadzie, Singapurze, Hong Kongu, Izraelu, Australii i Nowej Zelandii.26
Dawkowanie, wskazania i przeciwwskazania
Schemat podstawowy szczepienia obejmuje podanie 2 dawek w odstępie 28 dni (dla dorosłych w wieku 18–65 lat zarejestrowano również schemat przyspieszony 0, 7 dni). Szczepionka jest zarejestrowana do stosowania we wszystkich grupach wiekowych, począwszy od ukończenia 2. miesiąca życia (bez górnego limitu wieku). Dzieciom w wieku od 2 miesięcy do 3 lat należy podać połowę dawki dla dorosłych (czyli 0,25 ml zamiast 0,5 ml). Zaleca się, aby schemat podstawowy szczepienia zakończyć tydzień przed rozpoczęciem pobytu w regionie zagrożenia JE.
U dorosłych (>18. rż.), u których nadal występuje ryzyko zakażenia JE, zaleca się podanie trzeciej dawki (przypominającej) po upływie roku od zakończenia schematu podstawowego.27 Nie ma danych dotyczących celowości i bezpieczeństwa stosowania tej dawki u dzieci.
Szczepienie przeciwko JE jest zalecane (nieobowiązkowe) u podróżnych planujących pobyt w regionie endemicznym przez ≥1 miesiąc. Dotyczy to osób podróżujących długoterminowo oraz planujących krótkie, ale częste pobyty w rejonach endemicznych. Szczepienie należy także rozważyć u podróżnych planujących krótkie wyjazdy związane ze zwiększonym ryzykiem zakażenia (trasa podróży, planowane aktywności, warunki noclegowe) oraz nieznających dokładnie charakteru swojej podróży. Nie zaleca się szczepienia osób planujących krótką podróż (<1 mies.), ograniczoną do terenów miejskich lub poza sezonem transmisji JE.
Nie ma badań dotyczących skuteczności klinicznej szczepionki inaktywowanej Ixiaro (preparat zarejestrowano na podstawie badań imunogenności). W piśmiennictwie dostępne są jedynie dane na temat skuteczności klinicznej preparatów stosowanych w krajach endemicznych JE, jednak nie można ich odnieść do preparatu stosowanego w medycynie podróży u turystów z Europy (i np. z Ameryki Północnej). Szczepionka jest bardzo dobrze tolerowana, nie obserwuje się żadnych NOP swoistych dla tego preparatu. Przeciwwskazania do stosowania preparatu Ixiaro są takie jak dla innych preparatów inaktywowanych (reakcja anafilaktyczna na wcześniejszą dawkę lub składnik szczepionki). Ogółem ryzyko wystąpienia NOP oceniano na 13/100 000 podanych dawek (oczekiwane wartości dla NOP powinny się mieścić w przedziale 2–30/100 000 podanych dawek).26
Szczepienie przeciwko dendze
Denga jest chorobą wywoływaną przez wirusa dengi (DENV). Wyróżnia się cztery typy serologiczne wirusa (DENV 1–4) należącego do rodzaju Flavivirus. Choroba ta występuje endemicznie w tropikalnej części Azji, na Karaibach, w Ameryce Południowej i Środkowej oraz na wyspach Pacyfiku i w niektórych krajach Afryki. Przebycie dengi wiąże się z odpornością przeciwko zakażeniom wywołanym danym serotypem DENV, natomiast nie chroni przed zakażeniami pozostałymi serotypami. Rezerwuarem wirusa są ludzie i małpy, a przenosicielami – komary z rodzaju Aedes.
Większość infekcji DENV przebiega bezobjawowo. W zakażeniach objawowych początkowo dominuje wysoka gorączka, silny ból głowy i typowy ból zagałkowy, nudności, ból stawów oraz osłabienie. U niektórych chorych obserwuje się osutkę, najczęściej plamisto-grudkową, a w późniejszym okresie infekcji pojawiają się zmiany rumieniowe. Może dojść do uszkodzenia wątroby i rozwoju żółtaczki. Po kilku dniach gorączka ustępuje i stan większości chorych się poprawia. W rzadkich przypadkach dengi o ciężkim przebiegu wraz z obniżeniem temperatury ciała do 37,5–38°C następuje szybkie pogorszenie stanu chorego, występują krwawienia oraz objawy zwiększonej przepuszczalności ścian naczyń włosowatych z przeciekiem osocza do jam ciała, a niekiedy ze spadkiem ciśnienia tętniczego, utratą przytomności i wstrząsem. Może też wystąpić rozsiane krzepnięcie wewnątrznaczyniowe (DIC) i hipoalbuminemia.
Od wielu lat denga stanowi najczęstsze rozpoznanie u podróżnych z gorączką powracających ze wszystkich regionów tropikalnych, z wyjątkiem Afryki Subsaharyjskiej.
„Żywa”, atenuowana, 4-walentna szczepionka CYD-TDV przeciwko dendze została zarejestrowana w 2016 roku i obecnie jest dostępna m.in. w Brazylii, Meksyku, Salwadorze, Paragwaju, Kostaryce, Indonezji i na Filipinach oraz w Stanach Zjednoczonych (u mieszkańców obszarów Stanów Zjednoczonych, na których denga występuje endemicznie). WHO zaleca stosowanie tej szczepionki wyłącznie u osób w wieku 9–45 lat z potwierdzoną w badaniu serologicznym wcześniejszą infekcją dowolnym serotypem wirusa dengi, w celu ochrony przed zakażeniem pozostałymi serotypami DENV. Szczepionki nie należy podawać osobom, które w przeszłości nie przebyły zakażenia wirusem dengi, oraz osobom o nieznanym statusie zakażenia. W długotrwałej obserwacji prowadzonej w ramach badań klinicznych stwierdzono bowiem, że osoby takie są narażone na zwiększone ryzyko dengi o ciężkim przebiegu w razie zakażenia dzikim DENV po szczepieniu. W przypadku braku dokumentacji potwierdzającej wcześniejsze zakażenie wirusem gorączki denga, w celu jego potwierdzenia, przed szczepieniem należy wykonać testy serologiczne.28
U większości podróżujących do tropiku nie można więc zastosować szczepionki przeciwko dendze, ponieważ zwykle są to osoby seronegatywne, które nie były eksponowane na wirusa dengi i w przeszłości nie przebyły zakażenia DENV. Producent nie zaleca stosowania szczepionki CYD-TDV u podróżnych ze względu na brak danych dotyczących jej bezpieczeństwa, immunogenności i skuteczności u osób mieszkających poza regionami endemicznymi dengi. Zgodnie z zaleceniami WHO podanie szczepionki CYD-TDV można rozważyć w razie udokumentowanego przebycia dengi w przeszłości lub dodatniego wyniku badania serologicznego u osób planujących wyjazd na tereny o dużym ryzyku dengi. Zastosowanie szczepionki przeciwko dendze w medycynie podróży utrudnia jednak schemat szczepienia podstawowego obejmujący podanie 3 dawek w odstępie 6 miesięcy oraz niedostępność szczepionki CYD-TDV w Europie.
Szczepienia przeciwko innym chorobom przenoszonym przez komary
Na świecie zarejestrowano jedną szczepionkę przeciwko malarii – jest to szczepionka RTS,S (Mosquirix) dla niemowląt (p. Szczepienia przeciwko zarodźcom malarii – przyp. red.). Wymaga ona podania aż 4 dawek (schemat 3+1, odstęp między trzecią a czwartą dawką wynosi 18 mies.) i generalnie jest mało skuteczna. WHO nie zaleca rutynowego szczepienia niemowląt tym preparatem. Obecnie stosuje się go jedynie w ramach pilotażowych programów szczepień w trzech krajach afrykańskich. W związku z tym szczepionka ta nie znajduje zastosowania w medycynie podróży.Jak dotąd na świecie nie zarejestrowano innych szczepionek przeciwko chorobom przenoszonym przez komary, choć trwają prace nad wieloma z nich (np. przeciwko wirusowi zika).
Podsumowanie
Szczepienia przeciwko żółtej gorączce i japońskiemu zapaleniu mózgu są stosowane w medycynie podróży od 10-leci. Można je wykonywać zarówno w przychodniach medycyny podróży, jak i punktach szczepień działających przy przychodniach podstawowej opieki zdrowotnej (POZ), o ile zapewniają one dostęp do tzw. żółtych książeczek, a personel potrafi je prawidłowo wypełnić. Staranna kwalifikacja do szczepienia przeciwko żółtej gorączce z wnikliwą oceną wskazań do uodpornienia, ryzyka żółtej gorączki na trasie planowanego wyjazdu, regulacji prawnych oraz występowania przeciwwskazań lub sytuacji wymagających zachowania większej ostrożności związanej ze stanem zdrowia podróżnego pozwalają zminimalizować ryzyko NOP i jednocześnie zapewnić bezpieczeństwo podróżującym do regionów zagrożonych tą chorobą.
Piśmiennictwo:
1. Frierson J.G.: The yellow fever vaccine: a history. Yale J. Biol. Med., 2010; 83 (2): 77–852. Military Infectious Diseases Research Programme. https://midrp.amedd.army.mil/info/je.jsp
3. Wroczyńska A., Kuna A., Rymer W.: Zapobieganie chorobom zakaźnym w podróży. (W:) Gajewski P. (red.): Interna Szczeklika. Kraków, Medycyna Praktyczna, 2020: 2623–2630
4. Centers for Disease Control and Prevention: CDC Health Information for International Travel 2020. New York, Oxford University Press, 2019
5. Keystone J., Kozarsky P., Connor B. i wsp.: Travel Medicine. Philadelphia, Mosby Elsevier, 2018
6. Charakterystyka Produktu Leczniczego Stamaril
7. World Health Organization: International Travel and Health 2012. Geneva, WHO Press, 2012 (Vaccine-preventable diseases and vaccines – 2019 update)
8. World Health Organization: International Health Regulations (2005). Wyd. 2., Geneva, WHO Press, 2009
9. Staples E., Bocchini J., Rubin L. i wsp.: Yellow fever vaccine booster doses: recommendations of the Advisory Committee on Immunization Practices, 2015. MMWR, 2015; 64: 647–650
10. Wilder-Smith A.: Yellow fever in travelers. Curr. Infect. Dis. Rep., 2019; 21 (11): 42
11. DeSilva M., Sharma A., Staples E. i wsp.: Fatal yellow fever vaccine – associated viscerotropic disease – Oregon, September 2014. MMWR, 2015; 64 (10): 279–281
12. Barwick Eidex R., Yellow Fever Vaccine Safety Working Group: History of thymoma and yellow fever vaccination. Lancet, 2004; 364 (9438): 936
13. Staples J., Gershman M., Fischer M. i wsp.: Yellow fever vaccine. Recommendations of the Advisory Commitee on Immunization Practices (ACIP). MMWR, 2010; 59: 1–27
14. Smith D., Wong P., Gomez R., White K.: Ovalbumin content in the yellow fever vaccine. J. Allergy Clin. Immunol. Pract., 2015; 3: 794–795
15. Rutkowski K., Ewan P.W., Nasser S.: Administration of yellow fever vaccine in patients with egg allergy. Int. Arch. Allergy Immunol., 2013; 161 (3): 274–278
16. Rozporządzenie Ministra Zdrowia w sprawie wykazu zalecanych szczepień ochronnych oraz sposobu finansowania i dokumentowania zalecanych szczepień ochronnych wymaganych międzynarodowymi przepisami zdrowotnymi z dnia 16 września 2010 r. (Dz.U.2010, nr 180 poz. 1215)
17. World Health Organization. Amendment to International Health Regulations (2005), Annex 7 (yellow fever): Term of protection provided by vaccination against yellow fever infection, and validity of related IHR certificate of vaccination, extended to life of the person vaccinated. 2016. www.who.int/ith/annex7-ihr.pdf?ua=1
18. Lindsey P., Rabe I., Miller R. i wsp.: Adverse event reports following yellow fever vaccination, 2007–13. J. Travel Med., 2016; 23 (5). doi: 10.1093/jtm/taw045
19. wwwnc.cdc.gov/travel/yellowbook/2020/travel-related-infectious-diseases/japanese-encephalitis
20. Japan Selective Vaccinations. www.iamat.org/country/japan/risk/japanese-encephalitis
21. NHS: Japanese encephalitis. www.nhs.uk/conditions/japanese-encephalitis/causes/
22. Hegde N.R., Gore M.M.: Japanese encephalitis vaccines: immunogenicity, protective efficacy, effectiveness, and impact on the burden of disease. Hum. Vaccin. Immunother., 2017; 13 (6): 1–18
23. WHO – Japanese encephalitis. www.who.int/ith/vaccines/japanese_encephalitis/en/
24. The Pediatric Immunization Schedule in China as of 2012. www.researchgate.net/figure/The-Pediatric-Immunization-Schedule-in-China-as-of-2012_tbl1_303916318
25. Vaccination Schedule Recommended by the Japan Pediatric Society, August 1, 2018 Japan Pediatric Society. www.jpeds.or.jp/uploads/files/20180801_JPS%20Schedule%20English.pdf
26. Firbas C., Jilma B.: Product review on the JE vaccine IXIARO. Hum. Vaccin. Immunother., 2015; 11 (2): 411–420
27. Eder S., Dubischar-Kastner K., Firbas C.: Long term immunity following a booster dose of the inactivated Japanese Encephalitis vaccine IXIARO®, IC51. Vaccine, 2011; 29 (14): 2607–2612
28. WHO: Questions and Answers on Dengue Vaccines. www.who.int/immunization/research/development/dengue_q_and_a/en/




























