Opracowała lek. Iwona Rywczak
Jak cytować: Rywczak I.: Szczepienie dorosłych chorych na autoimmunologiczne zapalne choroby reumatyczne. Podsumowanie zaleceń European League Against Rheumatism 2019. Med. Prakt., 2020; 1: 75–84
Skróty: ANCA (anti-neutrophil cyloplasmic antibodies) – przeciwciała przeciwko cytoplazmie neutrofilów, AZChR – autoimmunologiczne zapalne choroby reumatyczne, CAPS (cryopyrin-associated periodic syndromes) – zespoły gorączek nawrotowych zależnych od kriopiryny, CDC – Centers for Disease Control and Prevention, EULAR – European League Against Rheumatism, GKS – glikokortykosteroid (y), LMPCh – leki modyfikujące przebieg choroby, MIZS – młodzieńcze idiopatyczne zapalenie stawów, MMR (measles–mumps–rubella) – trójskładnikowa szczepionka przeciwko odrze, śwince i różyczce, NOP – niepożądany odczyn poszczepienny, PCV-13 – 13-walentna skoniugowana szczepionka przeciwko pneumokokom, PPSV-23 – 23-walentna polisacharydowa szczepionka przeciwko pneumokokom, RZS – reumatoidalne zapalenie stawów, TRU – toczeń rumieniowaty układowy, WZW – wirusowe zapalenie wątroby
Wprowadzenie
Chorzy na zapalne choroby reumatyczne o podłożu immunologicznym (AZChR) należą do grupy zwiększonego ryzyka zakażeń, co wynika z samej choroby podstawowej, leczenia immunosupresyjnego oraz chorób współistniejących. Intensywne leczenie immunosupresyjne często stosuje się na początku rozwoju AZChR. Mimo szczególnego znaczenia profilaktyki chorób zakaźnych u chorych na AZChR szczepienia nie są u nich realizowane optymalnie. Wynika to m.in. ze zbyt małej świadomości reumatologów i innych lekarzy zajmujących się tą grupą chorych na temat znaczenia takiego postępowania oraz obaw o skuteczność, immunogenność i bezpieczeństwo szczepionek podawanych chorym na AZChR.
Cel i metodyka
Niniejszy dokument jest aktualizacją wytycznych
European League Against Rheumatism (EULAR) opublikowanych w 2011 roku, w której
uwzględniono nowe dane. Wytyczne są adresowane
do wszystkich pracowników placówek opieki
zdrowotnej zaangażowanych w opiekę nad chorymi
na AZChR, a ich celem jest poprawa realizacji
szczepień w tej grupie pacjentów.
Aktualizacji wytycznych dokonała grupa robocza, w której skład weszli specjaliści z 7 krajów
europejskich i z Izraela (w dziedzinie reumatologii,
immunologii klinicznej, chorób zakaźnych i pediatrii), a także 2 pacjentów. Przeprowadzono 4 przeglądy
systematyczne piśmiennictwa, opierając się
na sformułowanym wcześniej pytaniu klinicznym.
Przeszukano bazę MEDLINE (przez PubMed),
EMBASE i Cochrane Library, uwzględniając
artykuły opublikowane w języku angielskim od 1 października 2009 roku do 1 sierpnia 2018 roku.
Eksperci mogli proponować także uwzględnienie
innych artykułów, które uważali za istotne.
Zorganizowano 2 spotkania grupy roboczej.
Na pierwszym spotkaniu przedstawiono wstępne
wyniki 4 przeglądów systematycznych. Wtedy też grupa robocza podzieliła się na 2 zespoły w celu
sformułowania osobnych zaleceń dla dzieci i dorosłych.
Na kolejnym spotkaniu każde zalecenie
omówiono osobno aż do uzyskania porozumienia,
po czym poddano je głosowaniu, w którym uczestniczyli
wszyscy członkowie grupy roboczej.
Sformułowano 6 nadrzędnych (uniwersalnych)
zasad postępowania i 9 zaleceń, określając jakość
danych oraz siłę zaleceń według klasyfikacji
Oxford Centre for Evidence Based Medicine
(zgodnie z którą jakość danych oceniono w skali
od 1 [najwyższa] do 5 [najniższa], a siłę zaleceń w skali od A [zalecenie silne] do D [zalecenie słabe]
– przyp. red.). W głosowaniu nad ostateczną
wersją każde zalecenie oceniano w oddzielnym
głosowaniu w skali od 0 (całkowity brak zgody) do
10 (całkowite poparcie). Po każdym zaleceniu podano
średnią liczbę przyznanych punktów, zakres
ocen oraz odsetek głosujących, którzy przyznali
≥8 punktów. Ostateczną wersję artykułu przed publikacją
zatwierdził Komitet Wykonawczy EULAR.
Zasady uniwersalne
1. U chorych na AZChR należy raz w roku
ocenić stan uodpornienia oraz wskazania
do przeprowadzenia kolejnych szczepień.
Ocena jest jednym z zadań zespołu specjalistycznej
placówki reumatologicznej opiekującego
się pacjentem (zgodność 100%).
W aktualnej wersji wytycznych podkreślono, że
taka ocena powinna być rutynowym elementem
opieki nad chorym na AZChR. Należy również
uwzględnić ewentualne niepożądane zdarzenia i zaostrzenia choroby podstawowej, które wystąpiły
po wcześniejszych szczepieniach.
2. Zespół specjalistycznej placówki reumatologicznej
powinien omówić z chorym
indywidualny program szczepień, umożliwiając
mu udział w podejmowaniu decyzji,
natomiast realizacja szczepień musi być
wynikiem współpracy lekarza podstawowej
opieki zdrowotnej, reumatologa oraz pacjenta
(zgodność 94%).
Pacjent powinien otrzymać informację o ryzyku
związanym z chorobami zakaźnymi, wskazaniach
do wykonania szczepienia, wynikających z niego
korzyściach i związanym z nim ryzyku niepożądanych odczynów poszczepiennych (NOP), co pozwoli
mu podjąć świadomą decyzję o profilaktyce. Wykazano,
że szersza wiedza na temat szczepień wśród
chorych na AZChR i ich zalecenie przez reumatologa
wiązały się z większymi wskaźnikami wyszczepialności w tej grupie pacjentów. Realizację
szczepień u chorych na AZChR usprawnia także
współpraca placówki reumatologicznej z placówką
podstawowej opieki zdrowotnej.
3. Szczepienia u chorych na AZChR powinno
się wykonywać w stabilnej fazie choroby, w okresie remisji (zgodność 94%).
W większości badań dotyczących szczepień chorych
na AZChR uczestniczyły osoby w stabilnej
fazie choroby (remisji). Danych na temat szczepień w aktywnej fazie choroby jest zbyt mało, aby można
było rozstrzygnąć, czy szczepienia w ostrej fazie
choroby są bezpieczne i skuteczne. Szczepienie w aktywnej fazie choroby nie jest natomiast przeciwwskazane,
ale należy je rozważyć indywidualnie
(np. szczepienie przeciwko grypie jest wystarczająco
immunogenne
mimo dużego stopnia aktywności
reumatoidalnego zapalenia stawów [RZS]). Optymalną
strategią pozostaje jednak wykonywanie
szczepień w okresie remisji choroby (stabilnym).
4. Należy dążyć do wykonywania szczepień
przed rozpoczęciem planowanego leczenia
immunosupresyjnego, w szczególności
dotyczy to leków zmniejszających liczbę
limfocytów B (zgodność 100%).
Takie postępowanie ma na celu uzyskanie optymalnej
odpowiedzi na szczepienie. Szczególne znaczenie
ma to w przypadku rytuksymabu, którego
hamujące działanie na odpowiedź immunologiczną
na szczepienie przeciwko grypie i pneumokokom
potwierdzono u chorych na RZS, toczeń rumieniowaty
układowy (TRU) i spondyloartropatie.
Wpływ innych leków biologicznych modyfikujących
przebieg choroby (LMPCh) na immunogenność
szczepionek jest zmienny, ale u większości
pacjentów można uzyskać zadowalające stężenie
swoistych przeciwciał. Nie należy jednak opóźniać
rozpoczęcia leczenia immunosupresyjnego w celu
wykonania szczepień, jeżeli istnieje wskazanie
do niezwłocznej terapii.
Jeśli pacjent otrzymuje lek zmniejszający liczbę
limfocytów B, szczepienia zaleca się rozpoczynać
≥6 miesięcy po ostatniej dawce leku w cyklu i ≥4 tygodnie przed kolejnym cyklem leczenia. Jeżeli
zachowanie takich odstępów nie jest możliwe,
można rozważyć szczepienie (szczepionkami „nieżywymi”
– przyp. red.), jednak odpowiedź immunologiczna
może być niewystarczająca.
5. W razie potrzeby chorym na AZChR
można podawać szczepionki „nieżywe” w trakcie leczenia glikokortykosteroidami
(GKS) lub LMPCh (zgodność 100%).
Zalecenie to uzasadniają dostępne dane o skuteczności,
immunogenności i bezpieczeństwie
szczepionek „nieżywych” podawanych w trakcie
stosowania takich leków w ramach terapii różnych
AZChR. Nie dotyczy to leków zmniejszających liczbę
limfocytów B i prawdopodobnie również abataceptu.
6. W razie potrzeby u chorych na AZChR
można rozważyć zastosowanie szczepionek
„żywych”, z zachowaniem szczególnej ostrożności
(zgodność 53%).
Ogólnie zaleca się, aby w trakcie leczenia immunosupresyjnego
nie podawać szczepionek „żywych”.
Optymalnie takie szczepienie należy wykonać
≥4 tygodnie przed rozpoczęciem leczenia immunosupresyjnego.
Wyjątkiem może być szczepionka
przeciwko odrze, śwince i różyczce (MMR) oraz
atenuowana szczepionka przeciwko półpaścowi.
Badania dotyczące MMR przeprowadzono
głównie u dzieci, którym podawano drugą dawką
szczepionki. W badaniach tych stwierdzono
dobry profil bezpieczeństwa tej dawki. U dzieci
chorych na młodzieńcze idiopatyczne zapalenie
stawów (MIZS) leczonych metotreksatem w małej
dawce (p. ramka) i/lub etanerceptem nie obserwowano
zwiększonego ryzyka zaostrzeń choroby
podstawowej ani ciężkich zakażeń. W badaniach obejmujących dzieci chore na MIZS, TRU, leczone
m.in. GKS, metotreksatem i etanerceptem,
zaobserwowano dobrą immunogenność MMR
ocenianą na podstawie stężenia swoistych przeciwciał i wskaźników seroprotekcji. Opierając
się na tych danych, można rozważyć szczepienie
uzupełniające MMR (druga dawka) u chorych
na AZChR narażonych na kontakt z odrą, leczonych
lekami immunosupresyjnymi w małych
dawkach, które nie powodują istotnej immunosupresji
(p. ramka). Szczepienie przeciwko półpaścowi u chorych na AZChR – patrz zalecenie 5.
Ramka. Dawki leków powodujące istotną immunosupresjęa
- GKS stosowane przez ≥2 tyg. w dawceb 20 mg/24 h lub 2 mg/kg mc./24 h
- metotreksat w dawce ≥0,4 mg/kg mc./tydz.
- azatiopryna w dawce ≥3,0 mg/kg mc./24 h
- 6-merkaptopuryna w dawce ≥1,5 mg/kg mc./24 h
_____________________________________
a według Centers for Disease Control and Prevention
b w przeliczeniu na prednizon
Zalecenia
1. U większości chorych na AZChR należy
silnie rozważyć szczepienie przeciwko grypie
(siła zalecenia B, zgodność 93%).
Ryzyko zachorowania na grypę u chorych na
AZChR jest większe niż w populacji ogólnej. Większość
takich pacjentów odniesie więc korzyści
ze szczepienia, szczególnie osoby otrzymujące leki
immunosupresyjne. Nie ma jednak jednoznacznych
danych epidemiologicznych uzasadniających zalecenie
szczepienia wszystkim chorym na AZChR.
Szczepionka „nieżywa” przeciwko grypie sezonowej
lub pandemicznej ma podobny profil bezpieczeństwa u chorych na AZChR i w populacji
ogólnej. Nie wykazano, aby szczepienie przeciwko
grypie wiązało się z ryzykiem zaostrzenia choroby
podstawowej.
W badaniach z zastosowaniem 3-walentnej
szczepionki przeciwko grypie u chorych na AZChR
zmniejszyło się ryzyko zachorowania na grypę
lub zapalenie płuc, ryzyko powikłań, hospitalizacji
oraz zmalała umieralność z powodu grypy
lub zapalenia płuc. Szczepionki przeciwko grypie
sezonowej były immunogenne u chorych na RZS,
TRU, zapalenie naczyń związane z przeciwciałami
przeciwko cytoplazmie neutrofilów (ANCA), twardzinę
układową i łuszczycowe zapalenie stawów,
których leczono różnymi rodzajami LMPCh (lecz
nie rytuksymabem). W badaniach obejmujących
głównie chorych na RZS i TRU, w tym leczonych
immunosupresyjnie, immunogenność szczepionki
przeciwko grypie pandemicznej była zmniejszona,
jednak ochronne stężenie przeciwciał stwierdzono u większości pacjentów, poza osobami leczonymi
rytuksymabem lub abataceptem.
2. U większości chorych na AZChR należy
silnie rozważyć szczepienie przeciwko pneumokokom
(siła zalecenia C, zgodność 93%).
U chorych na AZChR narażonych na zwiększone
ryzyko choroby pneumokokowej zaleca się szczepienie
przeciwko pneumokokom zgodnie z wytycznymi
Centers for Disease Control and Prevention
(CDC) oraz European Society of Clinical Microbiology
and Infectious Diseases, tj. w schemacie
mieszanym uwzględniającym szczepionkę skoniugowaną
13-walentną (PCV-13) i polisacharydową
23-walentną (PPSV-23 [obecnie niedostępna w Polsce – przyp. red.]). Optymalną strategią jest
podanie w pierwszej kolejności PCV-13, a po upływie
≥8 tygodni PPSV-23. U chorych na AZChR
zaleca się podanie dawki przypominającej szczepionki
polisacharydowej 5 lat po pierwszym szczepieniu
PPSV-23 (p. tab. 1).
| Tabela 1. Zalecany schemat szczepienia przeciwko pneumokokom u chorych na AZChRa,b | |
|---|---|
| Aktualny stan uodpornienia | Zalecany schemat szczepienia |
| brak szczepień lub brak danych | 1 dawka PCV-13, a po 8 tyg. 1 dawka PPSV-23
podaj drugą dawkę PPSV-23 ≥5 lat po pierwszym szczepieniu PPSV-23 |
| 1 dawka PPSV-23, nieszczepiony PCV-13 (lub brak danych) | 1 dawka PCV-13 ?1 rok po PPSV-23
podaj drugą dawkę PPSV-23 ≥5 lat po pierwszym szczepieniu PPSV-23 i ≥8 tyg. po PCV-13 |
| nieszczepiony PPSV-23 (lub brak danych), 1 dawka PCV-13 | 1 dawka PPSV-23 ≥8 tyg. po PCV-13 podaj drugą dawkę PPSV-23 ≥5 lat po pierwszym szczepieniu PPSV-23 |
| 1 dawka PPSV-23, 1 dawka PCV-13 | podaj drugą dawkę PPSV-23 ≥5 lat po pierwszym szczepieniu PPSV-23 i ≥8 tyg. po szczepieniu PCV-13 |
| 2 dawki PPSV-23, nieszczepiony PCV-13 (lub brak danych) | 1 dawka PCV-13 po ≥1 roku od drugiej dawki PPSV-23 |
| a Immunization Action Coalition na podstawie zaleceń Centers for Disease Control and Prevention, www.immunize.org/catg.d/p3075.pdf
b PPSV-23 aktualnie nie jest dostępna w Polsce – przyp. red. AZChR – autoimmunologiczne zapalne choroby reumatyczne, PCV-13 – 13-walentna skoniugowana szczepionka przeciwko pneumokokom, PPSV-23 – 23-walentna polisacharydowa szczepionka przeciwko pneumokokom | |
Ryzyko zakażeń układu oddechowego u chorych
na AZChR jest szczególnie duże. W badaniu przeprowadzonym w Holandii u osób z TRU stwierdzono
13-krotnie większe ryzyko inwazyjnych
zakażeń pneumokokowych niż w populacji ogólnej. W badaniach obejmujących chorych na AZChR
obie szczepionki przeciwko pneumokokom – PCV-13
oraz PPSV-23 – były bezpieczne. Jedynie u osób z zespołami gorączek nawrotowych zależnych
od kriopiryny (CAPS) obserwowano ciężkie reakcje
miejscowe i systemowe (w cytowanej publikacji
opisano 7 pacjentów z CAPS, wszyscy rozwinęli
odczyny miejscowe określone jako ciężkie, wśród
objawów ogólnych opisano m.in. gorączkę i objawy
„podrażnienia” opon mózgowo-rdzeniowych – przyp.
red.). Danych na temat skuteczności szczepionek
przeciwko pneumokokom u chorych na AZChR jest
mało i są one niejednorodne. W badaniu z randomizacją u chorych na RZS nie stwierdzono przewagi
PPSV-23 nad placebo w zapobieganiu zapaleniu
płuc (niezależnie od etiologii lub w przebiegu zakażenia
pneumokokowego – przyp. red.). W innym
badaniu obserwacyjnym, z retrospektywnym zbieraniem
danych, ryzyko zachorowania na zapalenie
płuc (w 10-letnim okresie obserwacji – przyp.
red.) u osób nieszczepionych PPSV-23 było prawie
10-krotnie większe od ryzyka u osób zaszczepionych.
Więcej danych zebrano na temat immunogenności szczepionek. Zadowalające stężenie swoistych
przeciwciał w surowicy po szczepieniu PPSV-23 i PCV-13 obserwowano u chorych na RZS i TRU
(choć u chorych na RZS leczenie metotreksatem
wiązało się ze słabszą odpowiedzią na PCV-13). Dobrą
odpowiedź na PCV-13 obserwowano również w małym badaniu obejmującym pacjentów z zapaleniem
naczyń. Natomiast w badaniu z randomizacją
obejmującym chorych na RZS podanie PCV-13, a następnie PPSV-23 po okresie 16–24 tygodni,
prowadziło do uzyskania zadowalającego stężenia
swoistych przeciwciał w surowicy u 87% pacjentów
leczonych biologicznymi LMPCh i u 94% pacjentów
leczonych celowanymi, syntetycznymi LMPCh. Należy
jednak zaznaczyć, że w grupie leczonej rytuksymabem
odsetek ten wyniósł jedynie 25%.
3. Chorych na AZChR należy szczepić
przeciwko tężcowi zgodnie z zaleceniami
dla ogólnej populacji (siła zalecenia B, zgodność
100%). Profilaktykę bierną tężca należy
natomiast rozważyć u osób leczonych lekami
zmniejszającymi liczbę limfocytów B (siła zalecenia
D, zgodność 100%).
U chorych na RZS (w tym leczonych lekami immunosupresyjnymi)
lub TRU stwierdzano zadowalającą immunogenność szczepionek przeciwko
tężcowi. Podobne obserwacje dotyczą pacjentów,
którzy 24 tygodnie przed szczepieniem zakończyli
leczenie rytuksymabem. Ponadto u chorych
na TRU leczonych belimumabem nie wykazano
szybszego zanikania swoistych przeciwciał wytworzonych
po wcześniejszych szczepieniach.
4. Chorych na AZChR należy zaszczepić
przeciwko wirusowemu zapaleniu wątroby
(WZW) typu A lub B, jeśli należą do grupy ryzyka
zachorowania (siła zalecenia B, zgodność
100%). W szczególnych sytuacjach wskazane
jest przeprowadzenie szczepienia przypominającego
lub profilaktyki biernej (siła zalecenia
C, zgodność 100%).
Brakuje danych na temat zapadalności i ryzyka
WZW typu A u chorych na AZChR, natomiast
dane dotyczące epidemiologii zakażenia wirusem
zapalenia wątroby typu B (HBV) pochodzące z różnych regionów świata są niejednorodne.
Grupy ryzyka zakażenia wirusami zapalenia wątroby
– patrz tabela 2.
| Tabela 2. Grupy ryzyka zakażenia wirusami zapalenia wątroby | ||
|---|---|---|
| WZW | Grupa ryzyka | |
| typu A | osoby seroujemne podróżujące do krajów endemicznego występowania WZW typu A lub zamieszkujące takie kraje | |
| typu B | osoby narażone na zwiększone ryzyko ekspozycji na HBV (np. pracownicy placówek opieki zdrowotnej, osoby mieszkające lub utrzymujące kontakty seksualne z chorym na przewlekłe WZW typu B, mężczyźni utrzymujący kontakty seksualne z mężczyznami) | |
| osoby seroujemne podróżujące do krajów endemicznego występowania WZW typu B lub zamieszkujące takie kraje | ||
| HBV – wirus zapalenia wątroby typu B, WZW – wirusowe zapalenie wątroby | ||
| Tabela I. Schemat opracowania indywidualnego kalendarza szczepień u pacjenta leczonego z powodu choroby reumatycznej o podłożu immunologicznym | |
|---|---|
| Krok | Opis działania |
| 1. | określenie ryzyka zakażeń, w profilaktyce których można zastosować szczepienia:
– dla wszystkich chorych: grypa, zakażenie pneumokokowe i meningokokowe, tężec, ospa wietrzna, HPV – w związku z aktualną sytuacją epidemiologiczną na danym terenie pobytu stałego/ czasowego pacjenta: WZW typu B i A, odra, krztusiec, błonica, zakażenie meningokokowe, grypa – w związku ze stylem życia/hobby/narażeniem zawodowym: odkleszczowe zapalenie opon mózgowo-rdzeniowych i mózgu, wścieklizna, szczepienia stosowane w medycynie podróży (żółta gorączka, dur brzuszny, cholera, japońskie zapalenie mózgu, WZW typu A, meningokoki, poliomyelitis) |
| 2. | weryfikacja historii szczepień pacjenta:
– ocena dotychczasowej realizacji szczepień obowiązkowych i zalecanych – identyfikacja szczepień profilaktycznych wymagających podania dawki przypominającej |
| 3. | wstępny wybór szczepień na podstawie kroków 1. i 2. |
| 4. | określenie fazy choroby reumatologicznej (choroba aktywna/remisja) i stosowanego leczenia immunosupresyjnego (aktualnego i planowanego; data przyjęcia ostatniej dawki leku biologicznego, jeśli stosowano takie leczenie) |
| 5. | określenie względnych i bezwzględnych przeciwwskazań do wybranych wstępnie szczepień (dotyczy zwłaszcza szczepionek „żywych”) |
| 6. | w przypadku aktywnej fazy choroby reumatycznej ocena potencjalnych korzyści ze szczepienia i ryzyka związanego z zaostrzeniem choroby podstawowej |
| 7. | ustalenie indywidualnego schematu szczepienia z uwzględnieniem schematu dla osób w immunosupresji |
Leczenie immunosupresyjne stosowane u pacjentów z chorobami o podłożu autoimmunizacyjnym może mieć wpływ na skuteczność szczepienia oraz wiązać się z przeciwwskazaniami do szczepień preparatami zawierającymi atenuowane drobnoustroje (szczepionki „żywe”). W codziennej praktyce klinicznej zwykle trudno jest ocenić odpowiedź immunologiczną na szczepienie osoby będącej w stanie immunosupresji. Wyjątkiem jest oznaczenie stężenia przeciwciał anty-HBs, które jest łatwo dostępne i powinno być rutynowo wykonywane po szczepieniu przeciwko WZW typu B u osób z upośledzeniem odporności (także zgodnie z polskim Programem Szczepień Ochronnych). W przypadku niektórych szczepień, dysponując wiedzą z badań klinicznych i obserwacyjnych, w celu poprawy ich skuteczności opracowano odmienne schematy dla takich pacjentów (np. szczepienie przeciwko pneumokokom, szczepienia przypominające przeciwko meningokokom itp.). Jeśli jest to możliwe, szczepienia należy wykonać przed rozpoczęciem leczenia immunosupresyjnego. W przypadku niektórych chorób (grypa, krztusiec, odra) w celu ochrony przed zakażeniem wykorzystuje się także ochronę zbiorowiskową (szczepienie osób z otoczenia chorego). Wskazane jest, aby osoby, z którymi pacjent ma częsty kontakt (domownicy, personel medyczny), były zaszczepione przeciwko tym chorobom. W przypadku kwalifikacji do szczepienia pacjenta, którego leczono lekami biologicznymi, niekiedy należy odczekać określony czas od zakończenia terapii (p. tab. II), ponieważ zbyt szybkie szczepienie nie gwarantuje uzyskania odpowiedniej ochrony poszczepiennej. Szczególnie długi czas konieczny jest w przypadku rytuksymabu, który upośledza odpowiedź humoralną.
| Tabela II. Zalecany czas wykonania szczepień w zależności od zastosowanego leku biologicznegoa | ||
|---|---|---|
| Lek | Szczepionki „żywe” | Szczepionki „nieżywe” |
| abatacept | ≥4 tyg. przed leczeniem | ≥2 tyg. przed leczeniem
w ciągu 2 tyg. po zakończeniu leczenia odpowiedź na szczepienie jest osłabiona |
| altemtuzumab | nie określono czasu od ostatniej dawki leku, szczepienie przeciwwskazane w czasie leczenia | pełne szczepienie 6 tyg. przed rozpoczęciem leczenia |
| anakinra | ≥3 tyg. przed rozpoczęciem leczenia ≥3 mies. po zakończeniu leczenia | brak ograniczeń |
| ekulizumab | nie określono czasu od ostatniej dawki leku, szczepienia niezalecane |
≥2 tyg. przed rozpoczęciem leczenia w trakcie leczenia – ≥1 tydz. przed podaniem kolejnej dawki leku szczepienie przeciwko meningokokom – dawka przypominająca co 3–5 lat |
| anty-TNFα | etanercept – ≥1 mies. po zakończeniu leczenia przeciwciała anty-TNF – ≥3 mies. po zakończeniu leczenia | brak ograniczeń |
| rytuksymab | ≥1 mies. przed rozpoczęciem leczenia ≥12 mies. po ostatniej dawce leku | ≥6 mies. w przypadku dawki przypominającej ≥12 mies. w przypadku szczepienia podstawowego |
| tocylizumab | ≥3 mies. po ostatniej dawce leku | brak ograniczeń |
| inhibitory immunologicznych punktów kontroli limfocytów T | ≥6 mies. po zakończeniu leczenia | nie określono czasu od ostatniej dawki leku, zalecana indywidualizacja szczepienia |
| a na podstawie: Hall V., Johnson D., Torresi J.: Travel and biologic therapy: travel-related infection risk, vaccine response and recommendations. J. Travel Med., 2018; 25 (1) | ||
Stan istotnej (tzn. znacznej) immunosupresji może się również wiązać z potencjalnym ryzykiem zakażenia szczepem drobnoustroju zawartym w szczepionce „żywej”. Wśród preparatów przeznaczonych dla dorosłych są to szczepionki: MMR, przeciwko żółtej gorączce, durowi brzusznemu (doustna), ospie wietrznej (rzadko stosowana w populacji dorosłych) i półpaścowi (szczepionka zarejestrowana w Unii Europejskiej, ale niedostępna w Polsce). Przeprowadzono niewiele badań dotyczących oceny skuteczności i bezpieczeństwa szczepionek „żywych” u pacjentów leczonych immunosupresyjnie, dlatego przyjęto generalną zasadę, aby takim chorym ich nie podawać, choć są wyjątki od tej reguły. W przypadku wskazań do profilaktyki duru brzusznego można zastosować szczepionkę „nieżywą”, ale w profilaktyce pozostałych z wymienionych powyżej chorób obecnie nie ma preparatów alternatywnych dla szczepionek „żywych” (rekombinowana szczepionka przeciwko półpaścowi jest niedostępna w Polsce). W przypadku chorych, którzy otrzymali w przeszłości jedną dawkę szczepienia przeciwko odrze, eksperci EULAR dopuszczają podanie dawki uzupełniającej, jeśli stopień upośledzenia odporności jest niewielki (tzn. pacjent nie stosuje leczenia powodującego znaczną immunosupresję – p. ramka), a ryzyko zakażenia duże. Szczepienie przeciwko żółtej gorączce stosuje się w medycynie podróży. Chorym na choroby autoimmunizacyjne nie powinno się odmawiać prawa do podróżowania, warto jednak najpierw zwrócić ich uwagę na potencjalne niebezpieczeństwa zakażeń w krajach o odmiennym klimacie. Dopiero jeśli pacjent nie zrezygnuje z wyjazdu w rejony o szczególnie dużym ryzyku zakażenia wirusem żółtej gorączki, można rozważyć chwilowe przerwanie terapii immunosupresyjnej na czas szczepienia (z uwzględnieniem farmakokinetyki stosowanych leków). Jeśli jednak ryzyko zakażenia jest małe lub nie występuje, a szczepienie rozważa się tylko z przyczyn formalnych (niektóre państwa wymagają okazania na granicy międzynarodowego dokumentu z zaświadczeniem o szczepieniu przeciw żółtej gorączce), to należy od niego odstąpić i pacjentowi wystawić stosowny dokument w języku angielskim o przeciwwskazaniu medycznym do szczepienia.
Wielu lekarzy obawia się realizacji szczepień u osób z chorobami o podłożu autoimmunizacyjnym, sądząc,
że mogą one wzbudzić bądź nasilić nieprawidłową
odpowiedź układu odpornościowego i doprowadzić
do zaostrzenia choroby. Obecnie nie ma przeciwwskazań
do podawania szczepionek „nieżywych” pacjentom w okresie remisji, a w przypadku szczepionek „żywych”
należy uwzględnić zastrzeżenia opisane w komentowanych
wytycznych.
Eksperci EULAR odradzają podawanie
szczepionek w okresie zaostrzenia choroby, jednak zwracają uwagę na indywidualne podejście. Jeśli bowiem prawdopodobieństwo kontaktu z dzikim drobnoustrojem
jest duże (np. w okresie epidemii grypy), to dla pacjenta
zdecydowanie bezpieczniejsza jest kontrolowana immunizacja
(szczepienie) niż ryzyko powikłań występujących w przebiegu naturalnego zakażenia, na które i tak jest
potencjalnie narażony. Natomiast w przypadku stosowania
szczepień po ekspozycji na zakażenie (przede wszystkim
dotyczy to poekspozycyjnej profilaktyki WZW typu B,
tężca i wścieklizny) okres aktywności choroby autoimmunizacyjnej
nie jest przeciwwskazaniem do szczepienia
(podobnie jak ciąża i alergia na składniki szczepionki).
Należy też pamiętać, aby u pacjentów w stanie immunosupresji, u których odpowiedź na profilaktykę czynną jest
niepewna, w profilaktyce poekspozycyjnej uwzględnić
podanie swoistych przeciwciał (tzn. profilaktykę bierną). W przypadku istotnej ekspozycji na wirusa odry w profilaktyce
poekspozycyjnej aktualnie stosuje się dożylne
preparaty immunoglobulin.
W aktualizacji wytycznych EULAR eksperci zalecają,
aby stan uodpornienia pacjentów oceniać rutynowo
raz na rok. Zwrócili również uwagę na rolę specjalisty reumatologa w ustalaniu indywidualnego kalendarza
szczepień. Stosowne przepisy określają, kto w Polsce
może przeprowadzać szczepienia. Bez konieczności
ukończenia odrębnego kursu specjalistycznego lub doszkalającego
mogą je prowadzić lekarze ze specjalizacją z pediatrii, chorób zakaźnych, medycyny rodzinnej lub
epidemiologii. Jednak rola reumatologa, nawet jeśli nie
przeszedł on specjalistycznego kursu, jest tu nieodzowna.
To reumatolog określa, czy pacjent jest w aktywnej
fazie choroby, czy w remisji, ustala leczenie immunosupresyjne
oraz czas jego rozpoczęcia i zakończenia, co
ma znaczenie w planowaniu szczepienia szczepionkami
„żywymi”. Poza tym to reumatolog jest w stanie najlepiej
określić, z jakim stopniem upośledzenia odporności
wiąże się zastosowane leczenie. Mając na uwadze te informacje, optymalnym postępowaniem jest coroczne sprawdzanie stanu uodpornienia pacjenta oraz ustalanie
indywidualnego kalendarza szczepień przez reumatologa w ścisłej współpracy z lekarzem rodzinnym, który następnie
przeprowadza szczepienie. Można to robić podczas
corocznej kwalifikacji do profilaktyki grypy.
Dużym utrudnieniem jest brak jednolitej dokumentacji
szczepień u dorosłych pacjentów. Wszystkie
szczepienia prowadzone u dzieci są notowane w książeczce
zdrowia dziecka i karcie uodpornienia w poradni.
Natomiast dokumentacja szczepień u dorosłych często
znajduje się w różnych miejscach i zazwyczaj trudno ocenić,
czy pacjent otrzymał dane szczepienie (np. przeciwko
pneumokokom) i kiedy. Ustalenie daty ostatniego szczepienia
ma szczególne znaczenie, jeśli dawki przypominające
należy podawać cyklicznie (np. w przypadku tężca).
Jeśli szczepienie przeciwko tężcowi wykonano dawno i stężenie przeciwciał neutralizujących toksynę tężcową
jest niewykrywalne, pacjent może zachorować na tężec, a jeśli jest podawane zbyt często – istnieje ryzyko wystąpienia
NOP (np. duży odczyn miejscowy o typie reakcji
Arthusa lub zapalenie splotu ramiennego). U pacjentów,
którzy posiadają międzynarodową książeczkę szczepień,
wpisów można dokonywać w miejscu przeznaczonym
na szczepienia dodatkowe. U pozostałych warto założyć
kartę szczepień lub inny przeznaczony tylko do tego celu
dokument, gdzie będą wpisywane wszystkie wykonywane
szczepienia.
-
 Czy szczepienia mogą wpływać na ryzyko wystąpienia reumatoidalnego zapalenia stawów? To zagadnienie oceniono w przeglądzie systematycznym piśmiennictwa z metaanalizą, w którym uwzględniono 16 badań obserwacyjnych z grupą kontrolną, obejmujących łącznie populację prawie 26 mln osób w wieku 9–80 lat.
Czy szczepienia mogą wpływać na ryzyko wystąpienia reumatoidalnego zapalenia stawów? To zagadnienie oceniono w przeglądzie systematycznym piśmiennictwa z metaanalizą, w którym uwzględniono 16 badań obserwacyjnych z grupą kontrolną, obejmujących łącznie populację prawie 26 mln osób w wieku 9–80 lat. -
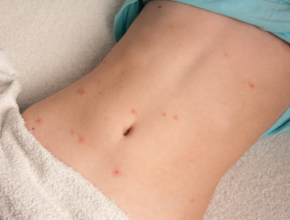
 Gorączka i osutka pęcherzykowa w 2. dobie po podaniu MMR 6-latkowi z MIZS Czy to może być NOP? Jakie dawki metotreksatu stanowią przeciwwskazanie do podawania szczepionek „żywych”? Jeżeli to ospa wietrzna, czy dziecko należy skierować do szpitala?
Gorączka i osutka pęcherzykowa w 2. dobie po podaniu MMR 6-latkowi z MIZS Czy to może być NOP? Jakie dawki metotreksatu stanowią przeciwwskazanie do podawania szczepionek „żywych”? Jeżeli to ospa wietrzna, czy dziecko należy skierować do szpitala? -
 Jak szczepić dzieci chore na autoimmunizacyjne zapalne choroby reumatyczne? Zapoznaj się z zaleceniami European Alliance of Associations for Rheumatology/Pediatric Rheumatology European Society.
Jak szczepić dzieci chore na autoimmunizacyjne zapalne choroby reumatyczne? Zapoznaj się z zaleceniami European Alliance of Associations for Rheumatology/Pediatric Rheumatology European Society. -
 Czy choroba Hashimoto może być przeciwwskazaniem do szczepień? Dziecko jest obecnie w eutyreozie, ale endokrynolog wystawił zaświadczenie o przeciwwskazaniu do realizacji szczepień ochronnych z powodu rozpoznania choroby autoimmunizacyjnej.
Czy choroba Hashimoto może być przeciwwskazaniem do szczepień? Dziecko jest obecnie w eutyreozie, ale endokrynolog wystawił zaświadczenie o przeciwwskazaniu do realizacji szczepień ochronnych z powodu rozpoznania choroby autoimmunizacyjnej.
-

-
 Szczepienia przed wyjazdem na Karaiby (Wyspy Karaibskie) Antigua i Barbuda, Bahamy, Barbados, Dominika, Dominikana, Grenada, Haiti, Jamajka, Kuba, Saint Kitts i Nevis, Saint Lucia, Saint Vincent i Grenadyny, Trynidad i Tobago, Anguilla, Antyle Holenderskie, Aruba, Brytyjskie Wyspy Dziewicze, Gwadelupa, Kajmany, Martynika, Montserrat, Navassa, Portoryko, Saint-Barthélemy, Saint-Martin, Turks i Caicos, Wyspy Dziewicze Stanów Zjednoczonych
Szczepienia przed wyjazdem na Karaiby (Wyspy Karaibskie) Antigua i Barbuda, Bahamy, Barbados, Dominika, Dominikana, Grenada, Haiti, Jamajka, Kuba, Saint Kitts i Nevis, Saint Lucia, Saint Vincent i Grenadyny, Trynidad i Tobago, Anguilla, Antyle Holenderskie, Aruba, Brytyjskie Wyspy Dziewicze, Gwadelupa, Kajmany, Martynika, Montserrat, Navassa, Portoryko, Saint-Barthélemy, Saint-Martin, Turks i Caicos, Wyspy Dziewicze Stanów Zjednoczonych -

-

-

-
 Zapalenie mięśnia sercowego Zapalenie mięśnia sercowego (myocarditis) jest chorobą spowodowaną najczęściej przez zakażenie wirusowe (np. dróg oddechowych). Proces zapalny obejmuje komórki mięśnia sercowego, tkankę śródmiąższową, naczynia, niekiedy też osierdzie, i może doprowadzić do uszkodzenia mięśnia sercowego i niewydolności serca. U większości chorych zapalenie mięśnia sercowego ustępuje samo, bez leczenia. Ważny jest jednak odpoczynek, ograniczenie aktywności fizycznej, picia alkoholu oraz przyjmowania niesteroidowych leków przeciwzapalnych.
Zapalenie mięśnia sercowego Zapalenie mięśnia sercowego (myocarditis) jest chorobą spowodowaną najczęściej przez zakażenie wirusowe (np. dróg oddechowych). Proces zapalny obejmuje komórki mięśnia sercowego, tkankę śródmiąższową, naczynia, niekiedy też osierdzie, i może doprowadzić do uszkodzenia mięśnia sercowego i niewydolności serca. U większości chorych zapalenie mięśnia sercowego ustępuje samo, bez leczenia. Ważny jest jednak odpoczynek, ograniczenie aktywności fizycznej, picia alkoholu oraz przyjmowania niesteroidowych leków przeciwzapalnych. -

-

-

-
 Leptospiroza Leptospiroza jest bakteryjną chorobą zakaźną wywołaną przez krętki z rodzaju Leptospira występujące na całym świecie z wyjątkiem strefy polarnej. Do zakażenia człowieka dochodzi w sposób przypadkowy przez błony śluzowe lub uszkodzoną skórę narażoną na kontakt z płynami ustrojowymi zwierzęcia z ostrą leptospirozą lub poprzez ekspozycję na wodę lub glebę zanieczyszczoną moczem zakażonych przewlekle zwierząt.
Leptospiroza Leptospiroza jest bakteryjną chorobą zakaźną wywołaną przez krętki z rodzaju Leptospira występujące na całym świecie z wyjątkiem strefy polarnej. Do zakażenia człowieka dochodzi w sposób przypadkowy przez błony śluzowe lub uszkodzoną skórę narażoną na kontakt z płynami ustrojowymi zwierzęcia z ostrą leptospirozą lub poprzez ekspozycję na wodę lub glebę zanieczyszczoną moczem zakażonych przewlekle zwierząt.
-
Jesień Pediatryczna 2026
XXV Krajowa Konferencja Szkoleniowa Kraków, 25–26 września
-
Wiosenne Spotkania Pediatryczne 2026
Obejrzyj wykłady
- pediatryczne wyzwania w praktyce
- algorytmy postępowania
- zrób to sam – sesja warsztatowa
- omdlenie – od objawu do rozpoznania
- ostry dyżur – stany nagłe w pediatrii
-
Neonatologia 2026
Obejrzyj wykłady
- antybiotykoterapia w neonatologii
- toksykologia prenatalna – implikacje kliniczne
- wstrząs, hipotensja, PDA – decyzje hemodynamiczne
- wsparcie oddechowe noworodka
- bezdech i sinica
Napisz do nas
Zadaj pytanie ekspertowi, przyślij ciekawy przypadek,
zgłoś absurd, zaproponuj temat dziennikarzom.
Pomóż redagować portal.
Pomóż usprawnić system ochrony zdrowia.