Opracowała: mgr Małgorzata Ściubisz
Komentarz: prof. dr hab. n. med. Jacek Wysocki, Katedra i Zakład Profilaktyki Zdrowotnej Uniwersytetu Medycznego w Poznaniu
Jak cytować: Ściubisz M.: Stosowanie 15- i 20-walentnej skoniugowanej szczepionki przeciwko pneumokokom u dorosłych. Aktualne (2022) wytyczne Advisory Committee on Immunization Practices. Med. Prakt., 2023; 1: 67–76
Aktualizacja wytycznych - p. Jak szczepić dorosłych przeciwko pneumokokom?
Skróty: ACIP – Advisory Committee on Immunization Practices, PCV-13 (13-valent pneumococcal conjugate vaccine) – skoniugowana 13-walentna szczepionka przeciwko pneumokokom, PCV-15 (15-valent pneumococcal conjugate vaccine) – skoniugowana 15-walentna szczepionka przeciwko pneumokokom, PCV-20 (20-valent pneumococcal conjugate vaccine) – skoniugowana 20-walentna szczepionka przeciwko pneumokokom, PPSV-23 (23-valent pneumococcal polysaccharide vaccine) – 23-walentna polisacharydowa szczepionka przeciwko pneumokokom, USA (United States of America) – Stany Zjednoczone Ameryki
Jakie zalecenia obowiązywały do tej pory?
W USA szczepienie przeciwko pneumokokom z użyciem polisacharydowej szczepionki 23-walentnej (PPSV-23) jest zalecane osobom w wieku ≥65 lat oraz dorosłym z czynnikami ryzyka zakażeń pneumokokowych od lat 80. XX wieku. W 2012 roku wprowadzono zalecenie szczepienia dorosłych z niedoborami odporności, implantem ślimakowym lub wyciekiem płynu mózgowo-rdzeniowego preparatami PCV-13 i PPSV-23, a od 2014 roku zalecenie to rozszerzono na wszystkie osoby w wieku ≥65 lat. Opierając się na zgromadzonych danych, w 2019 roku zmieniono zalecenia dotyczące stosowania PCV-13. Wskazano, że u osób w wieku ≥65 lat bez niedoboru odporności, implantu ślimakowego lub wycieku płynu mózgowo-rdzeniowego szczepienie przeciwko pneumokokom należy realizować z użyciem PPSV-23, a decyzję o ewentualnym podaniu PCV-13 podjąć wspólnie z pacjentem (zalecenie to nie było powszechnie stosowane w Polsce z uwagi na odmienną historię szczepień przeciwko pneumokokom i epidemiologię zakażeń pneumokokowych – przyp. red.). Zalecana liczba dawek szczepionek przeciwko pneumokokom i odstępy między dawkami różniły się w zależności od wieku pacjenta i obecności czynników ryzyka, co utrudniało realizację profilaktyki zakażeń pneumokokowych u dorosłych.
Dlaczego zmieniono obecne zalecenia?
Obecne zalecenia zmieniono w związku z rejestracją 2 nowych skoniugowanych szczepionek przeciwko pneumokokom o większej walentności – 15-walentnej (PCV-15), która – w porównaniu z PCV-13 – zawiera antygeny 2 dodatkowych typów serologicznych pneumokoka (Vaxneuvance [nazwa handlowa preparatu zarejestrowanego w Unii Europejskiej] – przyp. red.), i 20-walentnej (PCV-20), która – w porównaniu z PCV-13 – zawiera antygeny 7 dodatkowych typów serologicznych pneumokoka (Apexxnar [nazwa handlowa preparatu dostępnego w Polsce] – przyp. red.). Obie szczepionki zarejestrowano do stosowania u dorosłych w wieku ≥18 lat na podstawie wyników badań z randomizacją (RCT) porównujących ich odpowiedź immunologiczną z dostępnymi dotychczas PCV-13 i PPSV-23. Nowe zalecenia mają również na celu uproszczenie profilaktyki zakażeń pneumokokowych u dorosłych. Schemat szczepienia jest taki sam niezależnie od wieku i czynników ryzyka zakażeń pneumokokowych.
Jaka była metodyka opracowania nowych zaleceń?
Grupa robocza ds. szczepień przeciwko pneumokokom działająca przy Advisory Committee on Immunization Practices (ACIP) oceniła jakość dowodów naukowych dotyczących bezpieczeństwa i immunogenności PCV-15 i PCV-20 zgodnie z procedurą przewidzianą w systemie Grading of Recommendations Assessment, Development, and Evaluation (GRADE). Wykorzystując system Evidence to Recommendation (EtR) Framework, grupa robocza dokonała przeglądu danych naukowych dotyczących korzyści i potencjalnego ryzyka stosowania PCV-15 i PCV-20 u osób w wieku ≥65 lat lub młodszych dorosłych z czynnikami ryzyka zakażeń pneumokokowych. Wzięto także pod uwagę epidemiologię zakażeń pneumokokowych, ich znaczenie, jako problemu zdrowia publicznego, wartości ważne dla populacji docelowych i ich preferencje, kwestie dotyczące wykorzystania dostępnych zasobów, akceptację zaleceń oraz możliwość ich wdrożenia w praktyce.
Jakie są nowe zalecenia?
Zgodnie z nowymi zaleceniami dorosłym w wieku ≥65 lat lub w wieku 19–64 lat z niedoborami odporności lub innymi czynnikami ryzyka zakażeń pneumokokowych (p. ramka) dotychczas nieszczepionym przeciwko pneumokokom lub z nieznaną historią szczepienia należy podać (p. także ryc. 1 i tab. 1):
- 1 dawkę PCV-20 lub
- 1 dawkę PCV-15, a następnie 1 dawkę PPSV-23.
Oczekuje się, że takie schematy szczepienia zmniejszą zapadalność na chorobę pneumokokową w populacji dorosłych w wieku ≥65 lat oraz w wieku 19–64 lat z czynnikami ryzyka zakażeń pneumokokowych. Wyniki RCT sugerują, że bezpieczeństwo i immunogenność szczepienia z użyciem PCV-20 lub PCV-15 i PPSV-23 są podobne do bezpieczeństwa i immunogenności szczepienia z użyciem PCV-13 lub PCV-13 i PPSV-23. Nowe zalecenia upraszczają realizację profilaktyki zakażeń pneumokokowych u dorosłych, co może zwiększyć wyszczepialność i zapobiec większej liczbie zachorowań.
Ramka. Dorośli, którym ACIP zaleca szczepienie przeciwko pneumokokom
- osoby w wieku ≥65 lat
- osoby w wieku 19–64 lat z czynnikami ryzyka zakażenia S. pneumoniae
- choroba alkoholowa
- przewlekła choroba sercaa, wątroby lub płucb
- palenie papierosów
- cukrzyca
- implant ślimakowy
- wyciek płynu mózgowo-rdzeniowego
- przewlekła niewydolność nerekc
- brak śledziony (anatomiczny lub czynnościowy)c
- pierwotny lub wtórny niedobór odpornościc,d
- nowotwory złośliwe w stadium uogólnieniac
- zakażenie HIVc
- chłoniak Hodgkinac
- jatrogenna immunosupresjac,e
- białaczkic
- chłoniakic
- szpiczak mnogic
- zespół nerczycowyc
- niedokrwistość sierpowatokrwinkowa i inne hemoglobinopatiec
- przeszczepienie narządu miąższowegoc
a Dotyczy także chorych z zastoinową niewydolnością serca i kardiomiopatiami.
b Dotyczy także chorych z przewlekłą obturacyjną chorobą płuc, rozedmą płuc i astmą.
c Wskazuje na stan niedoboru odporności.
d Dotyczy także chorych z niedoborami odporności zależnej od limfocytów B (odporności
humoralnej) lub zależnej od limfocytów T (komórkowej), niedoborami składowych układu
dopełniacza (zwłaszcza niedoboru inhibitorów C1, C2, C3 i C4) oraz zaburzeniami układu
fagocytarnego (z wyjątkiem przewlekłej choroby ziarniniakowej).
e Dotyczy chorych przyjmujących leki immunosupresyjne, w tym przewlekle przyjmujących
systemowe glikokortykosteroidy lub poddanych radioterapii.

Ryc. 1. Schemat szczepienia przeciwko pneumokokom dorosłych w wieku ≥65 lat lub 19–64 lat z czynnikami ryzyka dotychczas nieszczepionych lub z nieznaną historią szczepienia
| Tabela 1. Zalecenia ACIP (2022) dotyczące stosowania PCV-15 i PCV-20 u dorosłych w wieku ≥65 lat lub 19–64 lat z czynnikami ryzyka zakażeń pneumokokowych | ||
|---|---|---|
| Czynnik ryzyka/choroba przewlekła | Grupa wiekowa | |
| 19–64 lat | ≥65 lat | |
| brak | nd | 1 dawka PCV-20 lub 1 dawka PCV-15, a następnie po ≥12 mies. 1 dawka PPSV-23 |
| choroba alkoholowa przewlekła choroba sercaa, wątroby lub płucb palenie papierosów cukrzyca implant ślimakowy wyciek PMR przewlekła niewydolność nerekc brak śledziony (anatomiczny lub czynnościowy)c pierwotny lub wtórny niedobór odpornościc,d nowotwory złośliwe w stadium uogólnieniac zakażenie HIVc chłoniak Hodgkinac jatrogenna immunosupresjac,e białaczkic chłoniakic szpiczak mnogic zespół nerczycowyc niedokrwistość sierpowatokrwinkowa i inne hemoglobinopatiec przeszczepienie narządu miąższowegoc |
1 dawka PCV-20 lub 1 dawka PCV-15, a następnie po ≥12 mies. 1 dawka PPSV-23 (minimalny odstęp ≥8 tyg. można rozważyć u dorosłych z niedoborami odporności, implantem ślimakowym lub wyciekiem PMR) |
1 dawka PCV-20 lub 1 dawka PCV-15, a następnie po ≥12 mies. 1 dawka PPSV-23 (minimalny odstęp ≥8 tyg. można rozważyć u dorosłych z niedoborami odporności, implantem ślimakowym lub wyciekiem PMR) uwaga: jeżeli PCV-15 lub PCV-20 podano w wieku <65 lat, nie trzeba podawać dodatkowych dawek |
| a Dotyczy także chorych z zastoinową niewydolnością serca i kardiomiopatiami. b Dotyczy także chorych z przewlekłą obturacyjną chorobą płuc, rozedmą płuc i astmą. c Wskazuje na stan niedoboru odporności. d Dotyczy także chorych z niedoborami odporności zależnej od limfocytów B (odporności humoralnej) lub zależnej od limfocytów T (komórkowej), niedoborami składowych układu dopełniacza (zwłaszcza niedoboru inhibitorów C1, C2, C3 i C4) oraz zaburzeniami układu fagocytarnego (z wyjątkiem przewlekłej choroby ziarniniakowej). e Dotyczy chorych przyjmujących leki immunosupresyjne, w tym przewlekle przyjmujących systemowe glikokortykosteroidy lub poddanych radioterapii. ACIP – Advisory Committee on Immunization Practices, nd – nie dotyczy, PCV-15 – skoniugowana 15-walentna szczepionka przeciwko pneumokokom, PCV-20 – skoniugowana 20-walentna szczepionka przeciwko pneumokokom, PMR – płyn mózgowo-rdzeniowy, PPSV-23 – 23-walentna polisacharydowa szczepionka przeciwko pneumokokom | ||
Wytyczne praktyki klinicznej
Schematy szczepienia
1. Dorośli dotychczas nieszczepieni przeciwko
pneumokokom lub z nieznaną historią
szczepienia
Zaleca się 1 dawkę PCV-20 lub PCV-15. Jeżeli
do realizacji szczepienia przeciwko pneumokokom
wybrano PCV-15, zalecany odstęp między dawką
PCV-15 i PPSV-23 wynosi ≥12 miesięcy (p. ryc. 1 i tab. 1). Minimalny odstęp wynoszący ≥8 tygodni
można rozważyć u dorosłych z niedoborami odporności
(p. ramka), z implantem ślimakowym lub
wyciekiem płynu mózgowo-rdzeniowego.
2. Dorośli, którzy uprzednio otrzymali
dawkę PPSV-23, ale nie otrzymali dawki
PCV.
Dorosłym, którzy uprzednio otrzymali dawkę
PPSV-23, ale nie otrzymali dawki szczepionki
skoniugowanej (PCV-13, PCV-15 lub PCV-20),
po ≥12 miesiącach można podać dawkę PCV-15
lub PCV-20. Jeżeli do kontynuacji szczepienia wybrano
PCV-15, nie trzeba podawać kolejnej dawki
PPSV-23 (p. ryc. 2).

Ryc. 2. Schematy szczepienia przeciwko pneumokokom dorosłych w wieku ≥65 lat lub 19–64 lat z czynnikami ryzyka, którzy uprzednio otrzymali dawkę PPSV-23, ale nie otrzymali dawki szczepionki
skoniugowanej (PCV-13, PCV-15 lub PCV-20)
3. Dorośli, którzy uprzednio otrzymali
dawkę PCV-13, ale nie otrzymali wszystkich
zalecanych dawek PPSV-23.
Nie oceniono, czy podanie PCV-15 lub PCV-20
dorosłym, którzy otrzymali uprzednio dawkę
PCV-13 lub PCV-13 i PPSV-23, przynosi dodatkowe
korzyści dla zdrowia publicznego. Aby dokończyć
schemat szczepienia przeciwko pneumokokom,
dorosłym z tej grupy należy podać brakujące dawki
PPSV-23 (p. ryc. 3 i tab. 2.). Jeżeli PPSV-23
jest niedostępna, można podać 1 dawkę PCV-20
(wówczas schemat szczepienia należy uznać za zakończony
[CDC przygotowały aplikację na urządzenia
mobilne, która pomaga ustalić schematy
szczepienia przeciwko pneumokokom w zależności
od wieku pacjenta, historii dotychczasowych szczepień
oraz obecności czynników ryzyka zakażeń
pneumokokowych zgodne z aktualnymi zaleceniami
amerykańskiego ACIP. Aplikacja „PneumoRecs
VaxAdvisor” dostępna jest bezpłatnie na urządzenia z systemem Android lub iOS; więcej informacji:
https://www.cdc.gov/vaccines/vpd/pneumo/hcp/pneumoapp.htm] – przyp. red.).
| Tabela 2. Zalecenia dotyczące szczepienia dorosłych, którzy uprzednio otrzymali dawkę PCV-13, ale nie otrzymali wszystkich zalecanych dawek PPSV-23 | |||
|---|---|---|---|
| Czynnik ryzyka/choroba przewlekła | Czy podać PPSV-23?a | ||
| 19–64 lat | ≥65 lat | ||
| brak | nd | TAK ≥1 rok po dawce PCV-13 | |
| bez niedoboru odporności | choroba alkoholowa przewlekła choroba sercab, wątroby lub płucc palenie papierosów cukrzyca |
TAK ≥1 rok po dawce PCV-13, jeżeli dawkę PCV-13 podano nieumyślnie lub w okresie dzieciństwa |
TAK ≥1 rok po dawce PCV-13 i ≥5 lat po dawce PPSV-23 podanej w wieku <65 lat |
| bez niedoboru odporności | implant ślimakowy wyciek PMR | TAK ≥8 tyg. po dawce PCV-13 | TAK ≥8 tyg. po dawce PCV-13, a następnie ≥5 lat po ostatniej dawce PPSV-23 podanej w wieku <65 lat |
| niedobór odporności | przewlekła niewydolność nerek brak śledziony (anatomiczny lub czynnościowy) pierwotny lub wtórny niedobór odpornościd nowotwory złośliwe w stadium uogólnienia zakażenie HIV chłoniak Hodgkina jatrogenna immunosupresjae białaczki chłoniaki szpiczak mnogi zespół nerczycowy niedokrwistość sierpowatokrwinkowa i inne hemoglobinopatie przeszczepienie narządu miąższowego |
TAK ≥8 tyg. po dawce PCV-13, a następnie ≥5 lat po pierwszej dawce PPSV-23 | TAK ≥8 tyg. po dawce PCV-13, a następnie ≥5 lat po ostatniej dawce PPSV-23 podanej w wieku <65 lat |
| a Jeżeli PPSV-23 jest niedostępna, można podać 1 dawkę PCV-20 (wówczas schemat szczepienia należy uznać za zakończony). b Dotyczy także chorych z zastoinową niewydolnością serca i kardiomiopatiami. c Dotyczy także chorych z przewlekłą obturacyjną chorobą płuc, rozedmą płuc i astmą. d Dotyczy także chorych z niedoborami odporności zależnej od limfocytów B (odporności humoralnej) lub zależnej od limfocytów T (komórkowej), niedoborami składowych układu dopełniacza (zwłaszcza niedoboru inhibitorów C1, C2, C3 i C4) oraz zaburzeniami układu fagocytarnego (z wyjątkiem przewlekłej choroby ziarniniakowej). e Dotyczy chorych przyjmujących leki immunosupresyjne, w tym przewlekle przyjmujących systemowe glikokortykosteroidy lub poddanych radioterapii. nd – nie dotyczy, PCV-13 – skoniugowana 13-walentna szczepionka przeciwko pneumokokom, PCV-20 – skoniugowana 20-walentna szczepionka przeciwko pneumokokom, PMR – płyn mózgowo-rdzeniowy, PPSV-23 – 23-walentna polisacharydowa szczepionka przeciwko pneumokokom | |||
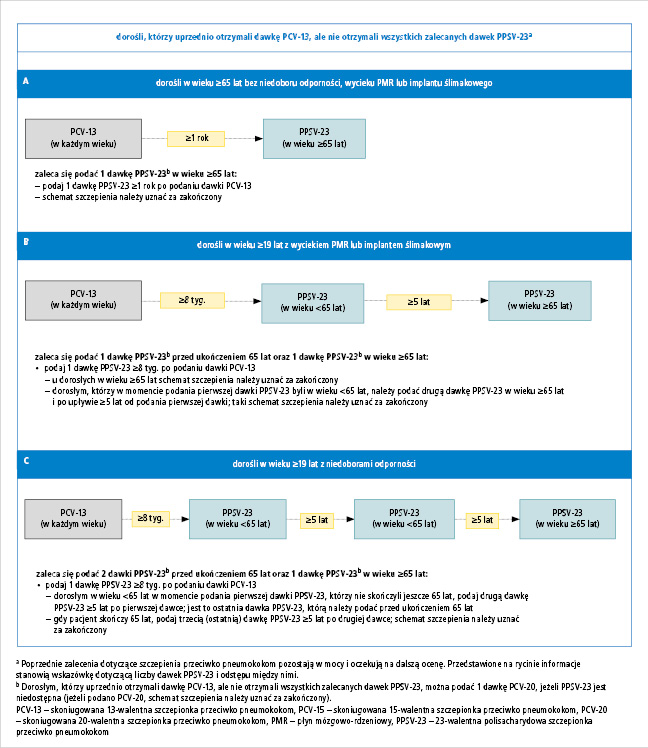
Ryc. 3. Schematy szczepienia przeciwko pneumokokom dorosłych (A–C), którzy uprzednio otrzymali dawkę PCV-13, ale nie otrzymali wszystkich zalecanych dawek PPSV-23
Koadministracja z innymi szczepionkami
PCV-13, PCV-15 i PCV-20 można podawać jednocześnie (w trakcie tej samej wizyty szczepiennej) z 4-walentną inaktywowaną szczepionką przeciwko grypie sezonowej. Wykazano, że takie postępowanie jest bezpieczne i nie ma istotnego wpływu na immunogenność szczepionek. Aktualnie nie ma danych dotyczących koadministracji PCV z innymi rutynowo stosowanymi szczepionkami (np. przeciwko błonicy, tężcowi i krztuścowi [bezkomórkowej], przeciwko wirusowemu zapaleniu wątroby typu B).
(W oryginale 36 pozycji piśmiennictwa.)
Komentarz
prof. dr hab. n. med. Jacek Wysocki
Katedra i Zakład Profilaktyki Zdrowotnej Uniwersytetu Medycznego w Poznaniu
W Polsce przez wiele lat panowało przekonanie, że szczepienia ochronne dotyczą tylko dzieci. Potrzeba szczepienia dorosłych nie była szeroko rozumiana, czego dowodem może być bardzo mały odsetek dorosłych szczepionych przeciwko grypie. Odmienna sytuacja była w USA, gdzie szczepienia przeciwko grypie od wielu lat stosowano na szeroką skalę, stopniowo rozszerzając zalecenia na kolejne grupy osób. Ponadto już w latach 70. XX wieku osobom w wieku ≥65 lat oraz dorosłym z grup ryzyka zalecano podawanie polisacharydowej 23-walentnej szczepionki przeciwko pneumokokom (PPSV-23), chociaż jej skuteczność była dobrze udokumentowana tylko w zapobieganiu inwazyjnej chorobie pneumokokowej (IChP), natomiast dane dotyczące skuteczności w zapobieganiu pneumokokowemu zapaleniu płuc pozostawiały wątpliwości (wyniki metaanalizy Falkenhorst i wsp. z 2017 r. potwierdzają, że PPSV-23 istotnie zmniejsza także ryzyko zachorowania na pneumokokowe zapalenie płuc, a jej skuteczność jest podobna wobec tego punktu końcowego do skuteczności skoniugowanej szczepionki 13-walentnej [p. Co wiadomo o skuteczności polisacharydowej szczepionki przeciwko pneumokokom u osób po 60. roku życia? – przyp. red.).1-3
Szczepienia przeciwko pneumokokom dorosłych również są w Polsce mało popularne. Może to wynikać z nieznajomości danych dotyczących obciążenia tej populacji zakażeniami pneumokokowymi, zwłaszcza osób starszych oraz młodszych dorosłych z grup ryzyka (p. ramka), dlatego poniżej przytoczę wybrane dane Krajowego Ośrodka Referencyjnego ds. Diagnostyki Bakteryjnych Zakażeń Ośrodkowego Układu Nerwowego (KOROUN). Od wielu lat największą zapadalność (wykrywalność) na IChP i śmiertelność z powodu tej choroby notuje się u osób w wieku ≥65 lat – w 2019 roku wskaźniki te wyniosły odpowiednio 6,91/100 000 i aż 44,4% (dla porównania u dzieci w wieku 2–4 lat wynosiły one 1,85/100 000 i 16,7%).4 Warto dodać, że znacznie lepszej jakości dane epidemiologiczne z USA (nadzór czynny) dowodzą, że w latach 2018–2019 zapadalność na IChP w populacji dorosłych była znacznie większa i wyniosła 24/100 000, a w latach 2010–2016 zapadalność na pozaszpitalne zapalenie płuc wymagające hospitalizacji wyniosła aż 847–3365/100 000.5 Zatem profilaktyka zakażeń pneumokokowych u dorosłych może odgrywać istotną rolę w wydłużeniu życia i poprawie jego jakości.
USA i Polska różnią się także historią szczepień przeciwko pneumokokom. Rozpoczęty w USA w 2000 roku program powszechnych szczepień niemowląt skoniugowaną szczepionką 7-walentną w ciągu kilku lat zmniejszył zapadalność na IChP we wszystkich grupach wiekowych, w tym o 37% w populacji osób w wieku ≥65 lat.6 W momencie zarejestrowania dla dorosłych skoniugowanej szczepionki 13-walentnej (PCV-13) w USA pojawiły się wątpliwości, czy preparat ten stosować na masową skalę u dorosłych, czy raczej tylko u małych dzieci, a dorosłych objąć szczepieniami z użyciem PPSV-23. Zmiany w zalecanej profilaktyce zakażeń pneumokokowych u dorosłych w USA przedstawiono krótko we wstępie omawianych wytycznych. Tymczasem pod koniec 2021 roku zarejestrowano 2 nowe skoniugowane szczepionki przeciwko pneumokokom: 15-walentną (PCV-15) i 20-walentną (PCV-20), obie do stosowania u dorosłych w wieku ≥18 lat (p. tab. 3 [w czerwcu 2022 r. w USA rozszerzono wskazania wiekowe do stosowania PCV-15 o niemowlęta i dzieci w wieku od 6 tyg. do 17 lat]), co zmusiło specjalistów zdrowia publicznego do weryfikacji dotychczasowych zaleceń. Obie szczepionki zarejestrowano na podstawie badań z randomizacją, w których wykorzystano zastępczy punkt końcowy w postaci immunogenności. Wykazano w nich, że PCV-15 i PCV-20 są nie mniej immunogenne niż dotychczas stosowana PCV-13 i/lub PPSV-23 wobec wspólnych typów serologicznych pneumokoka, stąd możemy się spodziewać, że będą przynajmniej tak samo skuteczne.7-9 Jednak, aby to potwierdzić, należy przeprowadzić badania oceniające istotne klinicznie punkty końcowe (IChP, pneumokokowe zapalenie płuc).
| Tabela 3. Szczepionki przeciwko pneumokokom zarejestrowane w Polsce do stosowania u dorosłycha | ||||
|---|---|---|---|---|
| PCV-13 | PCV-15 | PCV-20 | PPSV-23 | |
| nazwa handlowa | Prevenar 13 | Vaxneuvanceb | Apexxnar | Pneumovax 23 |
| rodzaj szczepionki | polisacharydowa, skoniugowana z białkiem nośnikowym CRM197 | polisacharydowa, skoniugowana z białkiem nośnikowym CRM197 | polisacharydowa, skoniugowana z białkiem nośnikowym CRM197 | polisacharydowa |
| wskazania do stosowania |
|
|
|
|
| skład jakościowy i ilościowy | 1 dawka (0,5 ml) zawiera:
|
1 dawka (0,5 ml) zawiera:
|
1 dawka (0,5 ml) zawiera:
|
1 dawka (0,5 ml) zawiera: polisacharyd otoczkowy (25 µg) serotypu 1, 2, 3, 4, 5, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19F, 19A, 20, 22F, 23F, 33F |
| a Opracowano na podstawie ChPL Prevenar 13, ChPL Vaxneuvance, ChPL Apexxnar, ChPL Pneumovax 23 b Szczepionka zarejestrowana w Unii Europejskiej, ale jeszcze niedostępna w Polsce IChP – inwazyjna choroba pneumokokowa, OZUŚ – ostre zapalenie ucha środkowego | ||||
Lekarze opiekujący się pacjentami w naszym kraju na pewno zauważą, że zarówno osoby w wieku ≥65 lat, jak i w wieku 19–64 lat z grupy ryzyka zakażeń pneumokokowych (p. ramka) rzadko korzystają z tego szczepienia. Od lat 90. XX wieku w Polsce PPSV-23 stosowano na niewielką skalę, a jej popularyzacji przeszkodziły także przerwy w dostawach do aptek. Na początku pandemii COVID-19 nieco zwiększyło się zainteresowanie PCV-13, zwłaszcza wśród osób starszych, choć dotyczyło to głównie okresu poprzedzającego rozpoczęcie stosowania szczepionek przeciwko COVID-19. W związku z tym w polskich warunkach podstawowym problemem pozostaje budowanie u pacjentów świadomości na temat znaczenia zakażeń pneumokokowych i możliwości ich zapobiegania. Od pewnego czasu mamy w tym obszarze wsparcie pulmonologów, onkologów i reumatologów, którzy sprawują opiekę specjalistyczną nad dorosłymi z grup ryzyka zakażeń pneumokokowych.
Zatem podstawową grupą pacjentów, z którymi zetkniemy się w codziennej praktyce, będą osoby dotychczas nieszczepione przeciwko pneumokokom. Dla tych osób PCV-20 będzie bardzo wygodną opcją, a fakt, że wymaga podania tylko 1 dawki (p. ryc. 1), może bardzo pozytywnie wpłynąć na jej akceptację i zwiększenie wyszczepialności. Mniej wygodną, ale zalecaną alternatywą jest zastosowanie PCV-15, a następnie 1 dawki PPSV-23 (p. ryc. 1). O przyszłości obu tych schematów szczepienia mogą zadecydować wyniki badań porównujących ich skuteczność rzeczywistą.
Od czasu pojawienia się w polskich aptekach PCV-20 otrzymujemy bardzo dużo pytań o to, czy warto nią doszczepiać pacjentów, którzy otrzymali już 1 dawkę PCV-13. Z omawianych wytycznych ACIP wynika, że na razie nie ma przekonujących danych potwierdzających dodatkowe korzyści dla zdrowia publicznego z podania tym osobom 1 dawki PCV-15 lub PCV-20. W związku z tym sugeruje się, aby na razie u tych osób szczepienia kontynuować przy użyciu PPSV-23, tak jak ujęto to w poprzednich zaleceniach ACIP (p. ryc. 3).2 Warto jednak zauważyć, że w przypadku trudności w dostępie do PPSV-23 ACIP dopuszcza podanie 1 dawki PCV-20 po PCV-13 i uznaje taki schemat za zakończony (polski czytelnik spotyka w tym miejscu rzadko stosowaną w naszej praktyce analizę korzyści dla zdrowia publicznego zestawioną z kosztami i nakładem pracy; jej wyniki nie wykluczają użycia PCV-20 po PCV-13, chociaż korzyści z takiego postępowania nie są jeszcze dobrze znane). Niemniej jednak jest to bardzo ważne zalecenie, bo jak nauczyło nas doświadczenie, dostępność PPSV-23 w Polsce jest bardzo zmienna.
| Tabela 4. Zalecenia dotyczące szczepienia przeciwko pneumokokom dorosłych w wybranych krajacha,b | |
|---|---|
| Kraj | Zalecenie |
| Niemcy | dorośli w wieku ≥60 lat: PPSV-23 (1 dawka co ≥6 lat) |
| Holandia | dorośli w wieku ≥60 lat: PPSV-23 (1 dawka co 5 lat aż do wieku 75 lat) dorośli z grup ryzyka: PCV-13 |
| Dania | dorośli w wieku ≥65 lat: PPSV-23 dorośli w wieku ≥18 lat z grup ryzyka: PCV-13 + PPSV-23 w odstępie ≥8 tyg. |
| Norwegia | dorośli w wieku ≥65 lat: PPSV-23 (1 dawka co ≥5 lat) dorośli w wieku ≥18 lat z grup ryzyka: PCV-15/PCV-20 (indywidualna ocena wskazań) + PPSV-23 w dostępie ≥8 tyg.; dawka PPSV-23 podawana co 3–5 lat |
| Włochy | dorośli w wieku ≥65 lat: PCV-13 + PPSV-23c |
| Wielka Brytania | dorośli w wieku ≥65 lat: PPSV-23 dorośli w wieku ≥18 lat z grup ryzyka: PCV-13 + PPSV-23 odstępie ≥8 tyg. |
| Kanada | dorośli w wieku ≥65 lat: PPSV-23 dorośli w wieku ≥18 lat z grup ryzyka: PCV-13 + PPSV-23 odstępie ≥8 tyg. |
| Australia | dorośli w wieku ≥70 lat: PCV-13 dorośli w wieku ≥18 lat z grup ryzyka: PCV-13 + PPSV-23 w odstępie 2–12 mies.; druga dawka PPSV-23 po ≥5 latach |
| a Niniejsza tabela ma charakter orientacyjny, dlatego ujęto w niej ogólne zalecenia (szczegółowe dane dotyczące odstępów między dawkami, ew. podawania dawek
przypominających lub szczepienia grup ryzyka nie zawsze były dostępne). b Opracowano na podstawie: (1) Impfkalender 2022 (dostęp: 6.10.2022); (2) Perniciaro S. i wsp.: Pneumococcal vaccine uptake and vaccine effectiveness in older adults with invasive pneumococcal disease in Germany: a retrospective cohort study. Lancet Reg. Health Eur., 2021; 7: 100–126; (3) Background paper to the updated pneumococcal vaccination recommendation for older adults in Germany (dostęp: 6.10.2022); (4) Information for policy makers (dostęp: 6.10.2022); (5) Pneumococcal vaccination programme for persons aged 65 years or more and for risk groups (dostęp: 6.10.2022); (6) Pneumokokkvaksine – veileder for helsepersonell (dostęp: 6.10.2022); (7) Calendario vaccinale (dostęp: 6.10.2022); (8) Orsi A. i wsp.: A summary of available evidence regarding carriage, clinical burden of lower respiratory tract infections and on-field effectiveness of PCV13 vaccination. Int. J. Mol. Sci., 2016; 17 (7): 1140; (9) Pneumococcal: the Green book, chapter 25 (dostęp: 6.10.2022); (10) Pneumococcal vaccine: Canadian Immunization Guide (dostęp: 6.10.2022); (11) Australian Immunisation Handbook. Pneumococcal disease (dostęp: 6.10.2022) c Zalecenia mogą się różnić między regionami. | |
Spoglądając szerzej na epidemiologię zakażeń pneumokokowych na świecie, wyraźnie widać, że rozszerzaniu składu szczepionek o kolejne serotypy pneumokoka towarzyszy zjawisko częściowego zastępowania serotypów – w miejsce serotypów szczepionkowych odpowiadających za coraz mniej zakażeń pojawiają się serotypy o dotychczas mniejszym znaczeniu (rzadziej odpowiadające za zakażenia) i nie ujęte w stosowanych szczepionkach.10 Ze względu na zróżnicowaną politykę szczepień przeciwko pneumokokom na świecie, również w zakresie rodzaju stosowanego preparatu (p. tab. 4), bardzo ważne jest stałe monitorowanie lokalnej sytuacji epidemiologicznej i dostosowywanie do niej krajowych lub regionalnych zaleceń (o standardach nadzoru nad inwazyjnymi zakażeniami pneumokokowymi pisaliśmy szerzej w Med. Prakt. Szczepienia WS 3/2019 oraz w serwisie Szczepienia: Wykrywanie i monitorowanie inwazyjnych zakażeń pneumokokowych. Aktualny (2018) standard nadzoru WHO i wskazówki dla lekarzy – przyp. red.). Należy o tym informować pacjentów zaniepokojonych zmieniającymi się zaleceniami.
Piśmiennictwo do komentarza:
1. Tomczyk S., Bennett N.M., Stoecker C. i wsp.: Use of 13-valent pneumococcal conjugate vaccine and 23-valent pneumococcal polysaccharide vaccine among adults aged ?65 years: recommendations of the Advisory Committee on Immunization Practices (ACIP). MMWR, 2014; 63: 822–8252. Kobayashi M., Bennett N.M., Gierke R. i wsp.: Intervals between PCV13 and PPSV23 vaccines: recommendations of the Advisory Committee on Immunization Practices (ACIP). MMWR, 2015; 64 (34): 944–947
3. Falkenhorst G., Remschmidt C., Harder T. i wsp.: Effectiveness of the 23-valent pneumococcal polysaccharide vaccine (PPV23) against pneumococcal disease in the elderly: systematic review and meta-analysis. PLoS One, 2017; 12 (1): e0169368
4. Skoczyńska A., Wróbel-Pawelczyk I., Gołębiewska A. i wsp.: Inwazyjna choroba pneumokokowa w Polsce w 2019 roku (dane KOROUN), 2020. http://koroun.nil.gov.pl/wp-content/ uploads/2020/06/Inwazyjna-choroba-pneumokokowa-IChP-w-Polsce-w-2019-roku.pdf (dostęp: 6.10.2022)
5. McLaughlin J.M., Khan F.L., Thoburn E.A. i wsp.: Rates of hospitalization for community-acquired pneumonia among US adults: a systematic review. Vaccine, 2020; 38: 741–751
6. Advisory Committee on Immunization Practices. Updated recommendations for prevention of invasive pneumococcal disease among adults using the 23-valent pneumococcal polysaccharide vaccine (PPSV23). MMWR, 2010; 59: 1102–1106
7. Essink B., Sabharwal C., Cannon K. i wsp.: Pivotal phase 3 randomized clinical trial of the safety, tolerability, and immunogenicity of 20-valent pneumococcal conjugate vaccine in adults 18 years and older. Clin. Infect. Dis., 2021. doi: 10.1093/cid/ciab990
8. Hammitt L.L., Quinn D., Janczewska E. i wsp.: Immunogenicity, safety, and tolerability of V114, a 15-valent pneumococcal conjugate vaccine, in immunocompetent adults aged 18–49 years with or without risk factors for pneumococcal disease: a randomized phase 3 trial (PNEU-DAY). Open Forum Infect. Dis., 2021; 9 (3). doi: 10.1093/ofid/ofab605
9. Platt H.L., Cardona J.F., Haranaka M. i wsp.: A phase 3 trial of safety, tolerability, and immunogenicity of V114, 15-valent pneumococcal conjugate vaccine, compared with 13-valent pneumococcal conjugate vaccine in adults 50 years of age and older (PNEU-AGE). Vaccine, 2022; 40 (1): 162–172
10. Du Q.Q., Shi W., Yu D., Yao K.H.: Epidemiology of nonvaccine serotypes of Streptococcus pneumoniae before and after universal administration of pneumococcal conjugate vaccines. Hum. Vaccin. Immunother., 2021; 17: 5628–5637