Skróty: ANC (absolute neutrophil count) – bezwzględna liczba neutrofili, G-CSF (granulocyte colony-stimulating factor) – czynnik wzrostu kolonii granulocytów, SCN (severe congenital neutropenia) – ciężka wrodzona neutropenia, SCNIR – Severe Congenital Neutropenia International Registry
Wprowadzenie
Granulocyty
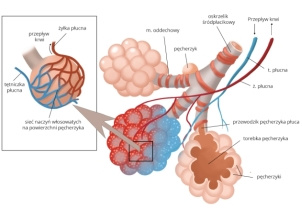
Granulocyty obojętnochłonne (neutrofile, neutrocyty) to komórki zaliczane do leukocytów, wywodzące się z macierzystej komórki krwiotwórczej. Szpik produkuje około 2 × 109 neutrofili/kg mc./24 h. W trakcie infekcji produkcja i uwalnianie komórek może się zwiększyć nawet 10-krotnie. Neutrofile żyją 2–3 dni, w tym przez 6–20 godzin przebywają we krwi, następnie migrują do tkanek, a po 1–2 dobach podlegają apoptozie (zaprogramowana śmierć komórki). Około 50% granulocytów obojętnochłonnych znajduje się we krwi obwodowej, a pozostałe – w tkankach. Spośród wszystkich granulocytów krwi obwodowej tylko około 49% znajduje się w strumieniu krwi płynącej (pula krążąca granulocytów), a pozostałe (51%) stanowią pulę marginalną, uwięzioną przyściennie w sieci drobnych naczyń.1 Wypływają z tego dwa bardzo ważne praktyczne wnioski:
- człowieka ma ogromną rezerwę uwalniania i produkcji granulocytów obojętnochłonnych, co wykorzystuje na przykład w czasie infekcji
- w ramach morfologii krwi obwodowej ocenia się jedynie pulę krążącą, która stanowi około 1 wszystkich granulocytów znajdujących się w organizmie, dlatego nie zawsze skrajnie mała liczba granulocytów wykazana w morfologii krwi obwodowej wskazuje na brak granulocytów w innych kompartmentach organizmu (w puli zapasowej szpikowej i obwodowej oraz w tkankach).
Neutropenia
Jako neutropenię określa się zmniejszenie w odniesieniu do normy wiekowej liczby granulocytów obojętnochłonnych z puli krążącej, ocenianej w morfologii krwi obwodowej. U starszych dzieci i dorosłych neutropenię rozpoznaje się, jeśli bezwzględna liczba neutrofili (absolute neutrophil count – ANC) wynosi <1500/µl krwi obwodowej. Neutropenia zdecydowanie częściej jest objawem różnych zaburzeń niż chorobą. Może być problemem izolowanym albo występować jednocześnie z innymi zaburzeniami.1-5 Podział neutropenii w zależności od zastosowanych kryteriów przedstawiono w tabeli 1.
| Tabela 1. Podział neutropenii z uwzględnieniem wybranych kryteriów klinicznycha | ||
|---|---|---|
| Kryterium | Rodzaj neutropenii | Opis/przykłady |
| czas trwania | ostra | <3 mies. |
| przewlekła | ≥3 mies. | |
| ANC | agranulocytoza | <100/µl |
| ciężka neutropenia | 100–500/µl | |
| umiarkowana neutropenia | 501–1000/µl | |
| łagodna neutropenia | 1001/µl – dolna granica normy wiekowej (dla większości 1500/µl) | |
| etiologia | wrodzona | uwarunkowana genetycznie występująca rodzinnie, mimo braku potwierdzenia w badaniach genetycznych |
| nabyta (wtórna) | efekt zahamowanej produkcji (np. po cytostatykach) efekt wyparcia przez inne, zazwyczaj patologiczne komórki (np. ostre białaczki) efekt skróconego przeżycia we krwi obwodowej (autoimmunizacyjna, hipersplenizm) | |
| a Opracowano na podstawie 2.–5. pozycji piśmiennictwa. ANC – bezwzględna liczba granulocytów | ||
Epidemiologia neutropenii
Neutropenia jest jednym z częstszych zaburzeń układu krwiotwórczego zarówno u dzieci, jak i dorosłych. Ponieważ morfologia krwi obwodowej jest najczęściej wykonywanym badaniem laboratoryjnym, także u osób zdrowych, rozpoznanie neutropenii jest relatywnie łatwe. U pacjentów, u których nie stwierdza się czynników ryzyka neutropenii (np. leczenie onkologiczne lub immunosupresyjne, ostra infekcja wirusowa, układowa choroba tkanki łącznej), jej obecność zwykle jest zaskakująca i wymaga podjęcia decyzji odnośnie do dalszej diagnostyki lub badań kontrolnych. Należy podkreślić, że u zdecydowanej większości osób z przypadkowo wykrytą neutropenią wynik kontrolnej morfologii krwi wykonanej 2–4 tygodni później jest prawidłowy. Najczęstszą przyczyną ostrej i bezobjawowej neutropenii są infekcje wirusowe. Znacznie rzadziej rozpoznaje się neutropenię przewlekłą.3 W tabeli 2 wymieniono objawy wymagające poszerzenia diagnostyki w celu wyjaśnienia przyczyny zmniejszenia liczby granulocytów obojętnochłonnych. Częstość neutropenii, niezależnie od jej przyczyny, oceniono w kilku szeroko zakrojonych badaniach. Andersen i wsp.3 rozpoznali neutropenię u 2,1% z 370 000 przebadanych mieszkańców Danii, w tym u 2% ostrą, a u 0,1% przewlekłą. Z kolei w USA neutropenię rozpoznano u 4,5% populacji Afroamerykanów oraz 0,8% osób rasy białej.4
| Tabela 2. Najczęstsze objawy i nieprawidłowe wyniki badań laboratoryjnych wskazujące na konieczność poszerzenia diagnostykia | ||
|---|---|---|
| objawy towarzyszące nowo rozpoznanej neutropenii | powiększenie wątroby, śledziony, węzłów chłonnych wady rozwojowe, zespoły chorobowe zakażenia, zwłaszcza o poważnym przebiegu występowanie ropni/zakażeń ropnych w przeszłości i/lub aktualnie, zwłaszcza o poważnym, nawrotowym lub przewlekłym przebiegu zakażenia grzybicze, w tym drożdżyce błony śluzowej jamy ustnej o poważnym, przewlekłym lub nawrotowym charakterze nawracająca gorączka z towarzyszącymi innymi objawami lub bez zmniejszenie masy ciała, złe ogólne samopoczucie | |
| nieprawidłowe wyniki badań laboratoryjnych i/lub obrazowych | nieprawidłowości w zakresie innych linii komórkowych w morfologii
krwi (np. niedokrwistość, małopłytkowość) duże wykładniki stanu zapalnego nawet po ustąpieniu infekcji (CRP, OB) nieprawidłowe wyniki innych badań (np. LDH) nieprawidłowy wynik USG jamy brzusznej, węzłów chłonnych nieprawidłowy obraz RTG klatki piersiowej | |
| inne | współwystępowanie chorób przewlekłych przyjmowanie leków z udowodnioną supresją szpiku rodzinne występowanie neutropenii rodzinne występowanie różnych problemów hematologicznych dodatni wywiad rodzinny w kierunku poważnych zakażeń, ropni dodatni wywiad rodzinny w kierunku wczesnych/niewyjaśnionych zgonów dzieci i dorosłych z powodów infekcji, nowotworów, innych chorób hematologicznych | |
| a opracowała autorka CRP – białko C-reaktywne, LDH – dehydrogenaza mleczanowa, OB – odczyn Biernackiego, RTG – badanie rentgenowskie, USG – badanie ultrasonograficzne | ||
Łagodna przewlekła neutropenia
Własne doświadczenie kliniczne wskazuje, że przypadkowo wykryta izolowana neutropenia u dzieci i dorosłych utrzymująca się przez >3 miesiące jest przejawem przewlekłej łagodnej neutropenii autoimmunizacyjnej lub idiopatycznej. Zwykle przebiega bez poważnych powikłań infekcyjnych lub typowo dla wieku chorego oraz z wyrzutem granulocytów do wartości >1000/µl w sytuacji stresowej (np. na początku infekcji). Obserwacje te znajdują potwierdzenie w piśmiennictwie.2,5 W przypadku innych zaburzeń, w tym poważnych infekcji, konieczne jest poszukiwanie innych możliwych przyczyn, w tym neutropenii wrodzonej.
Szczepienia ochronne u osób z przypadkowo wykrytą neutropenią
Granulocyty obojętnochłonne uczestniczą w indukcji humoralnej odpowiedzi poszczepiennej. W szczepionkach inaktywowanych znajdują się adiuwanty, które w miejsce aplikacji szczepionki rekrutują komórki immunologicznie kompetentne (w tym granulocyty) i wzmacniają odpowiedź humoralną. Zdolność wspomagania odpowiedzi humoralnej mają także inne komórki (np. makrofagi),6 dlatego nawet ciężka neutropenia nie jest przyczyną braku odpowiedzi poszczepiennej, choć może ona być słabsza, zwłaszcza w przypadku ciężkiej neutropenii wrodzonej (severe congenital neutropenia – SCN). Brak granulocytów wyłącznie w puli krążącej nie osłabia odpowiedzi na szczepienie. W związku z tym obawy związane z realizacją immunizacji czynnej nie wynikają z ryzyka braku odpowiedzi poszczepiennej u chorych z neutropenią, ale z ryzyka odczynów niepożądanych, zwłaszcza po podaniu szczepionek „żywych”. Należy pamiętać, że granulocyty mają duże znaczenie w zwalczaniu zakażeń bakteryjnych, dlatego zastosowanie atenuowanych, ale żywych szczepów bakteryjnych zwiększa ryzyko powikłań u chorych, którzy nie mają granulocytów w organizmie (nie tylko w puli krążącej). W związku z tym u chorych z SCN zazwyczaj przeciwwskazane są szczepionki „żywe” przeciwbakteryjne (np. przeciwko gruźlicy [BCG] i durowi brzusznemu).7-9 Własne obserwacje oraz dane z piśmiennictwa wskazują jednak, że ryzyko powikłań po podaniu szczepionki „żywej” przeciwbakteryjnej (np. BCG) pacjentom wyłącznie ze zmniejszoną liczbą granulocytów (w tym SCN) jest małe. Inaczej jest u pacjentów z defektem czynności granulocytów (np. przewlekłą chorobą ziarniniakową) lub towarzyszącym defektem limfocytów (np. zespół Griscelliego).10 Wprawdzie „żywe” szczepionki przeciwwirusowe są w tej grupie bezpieczne i można, a nawet trzeba je zalecać, jednak ważny jest optymalny czas ich podania.7-9 Według zaleceń Severe Congenital Neutropenia International Registry (SCNIR) u chorych z przewlekłą neutropenią, w tym SCN, szczepienia należy realizować zgodnie z krajowymi wytycznymi, aczkolwiek w ciężkich postaciach SCN decyzję o podaniu szczepionki „żywej” powinien podją doświadczony specjalista.11
Ostra neutropenia
Z punktu widzenia szczepień ochronnych ostra neutropenia nie stanowi istotnego problemu. Może być powodem jednorazowego, zazwyczaj nieistotnego klinicznie odroczenia szczepienia.
U pacjentów z przypadkowo wykrytym pierwszym epizodem neutropenii nie wiadomo, czy będzie ona miała charakter ostry, czy przewlekły. W pierwszej kolejności należy odpowiedzieć na pytanie, czy pacjent wymaga wyłącznie obserwacji, czy konieczne jest przeprowadzenie badań specjalistycznych. U pacjentów z izolowaną neutropenią, u których nie stwierdza się innych zaburzeń, optymalna jest strategia patrz i czekaj. Na tym etapie nie ma żadnych przeciwwskazań do realizacji szczepień ochronnych szczepionkami inaktywowanymi, mRNA, wektorowymi oraz „żywymi” przeciwwirusowymi. Nie należy zatem odraczać szczepień obowiązkowych ani zalecanych, w tym przeciwko COVID-19. Obecnie w Polsce nie ma „żywych” szczepionek przeciwko COVID-19. U pacjentów z łagodną neutropenią (ANC >1000/µl) można również bezpiecznie stosować szczepionki „żywe” przeciwbakteryjne.
Przewlekła neutropenia
U pacjentów z neutropenią utrzymującą się przez >3 miesiące należy rozważyć jej długotrwałe lub stałe występowanie, dlatego nie można zwlekać z realizacją szczepień ochronnych.
Realizacja szczepień ochronnych u pacjentów z neutropenią przewlekłą zależy od ustalonej etiologii. Pediatrzy najczęściej mają do czynienia z przewlekłą łagodną neutropenią dziecięcą autoimmunizacyjną lub idiopatyczną. Określenie „łagodna” nie odnosi się do liczby bezwzględnej granulocytów, która może być skrajnie mała, ale do przebiegu klinicznego. Typową cechą tego zaburzenia jest przemijający charakter – wyniki badań zwykle wracają do normy w ciągu kilku lub kilkunastu miesięcy.5,8 Wydaje się, że lekarze POZ, którzy opiekują się zdrowymi klinicznie dziećmi z przewlekłą neutropenią jako jedyną nieprawidłowością, mogą sami podjąć decyzję o szczepieniach. Jednak doświadczenie wskazuje, że często w takiej sytuacji kierują swoich pacjentów do hematoonkologów dziecięcych lub immunologów klinicznych w celu potwierdzenia diagnozy i zaplanowania dalszej opieki. Specjaliści zwykle ograniczają diagnostykę do podstawowych badań laboratoryjnych i opracowują zalecenia dotyczące opieki nad dzieckiem. Ważne jest wykonanie morfologii krwi obwodowej na początku ewentualnej banalnej infekcji, aby udokumentować wyrzut granulocytów do wartości >1000/µl i potwierdzić rozpoznanie łagodnej przewlekłej neutropenii dziecięcej. Natomiast nie ma potrzeby oznaczania morfologii bezpośrednio przed szczepieniem.
Immunizacja czynna u pacjentów, u których nie udokumentowano wyrzutu granulocytów do wartości >1000/µl, obejmuje planową realizację szczepień obowiązkowych oraz wszystkich zalecanych, realizowanych szczepionkami inaktywowanymi oraz „żywymi” przeciwwirusowymi, a w przypadku szczepień przeciwko COVID-19 – szczepionkami mRNA. Poniżej podano przykładowe zalecenia dotyczące realizacji szczepień u dziecka w wieku 10 miesięcy, wcześniej szczepionego zgodnie z programem szczepień obowiązkowych:
- w razie infekcji z gorączką wskazane jest oznaczenie morfologii krwi obwodowej z rozmazem w 1.–2. dniu choroby (ocena zdolności do wyrzutu granulocytów w celu potwierdzenia łagodnej przewlekłej neutropenii dziecięcej); po udokumentowaniu wyrzutu granulocytów nie ma potrzeby oznaczania morfologii w przypadku kolejnych banalnych infekcji
- planowa realizacja obowiązkowych szczepień ochronnych, z wyjątkiem szczepionek „żywych” przeciwbakteryjnych, do badań kontrolnych zaplanowanych za 3 miesiące
- poszerzenie immunizacji czynnej o szczepienia
zalecane przeciwko:
– meningokokom grupy B ,A, C, W i Y
– grypie szczepionką inaktywowaną
– COVID-19 zgodnie z aktualizowanymi zaleceniami krajowymi
– ospie wietrznej (jeśli dziecko wcześniej nie chorowało na ospę) - szczepienia należy realizować zgodnie z charakterystyką produktów leczniczych (ChPL).
Przy opracowywaniu zaleceń dla pacjenta, u którego potwierdzono rozpoznanie łagodnej przewlekłej neutropenii dziecięcej, należy uwzględnić wszystkie szczepienia obowiązkowe i zalecane, łącznie ze szczepionkami „żywymi”, także przeciwbakteryjnymi. Bezpieczeństwo „żywych” szczepionek przeciwbakteryjnych w przewlekłej łagodnej neutropenii dziecięcej wynika z faktu, że deficyt granulocytów dotyczy puli krążącej, natomiast są one obecne w tkankach i pulach zapasowych.
Realizacja szczepień u dorosłych z przewlekłą izolowaną neutropenią autoimmunizacyjną lub idiopatyczną o bezobjawowym lub łagodnym przebiegu powinna być priorytetem dla lekarzy POZ i specjalistów zajmujących się takimi chorymi. W zaleceniach należy uwzględnić wcześniej zrealizowane szczepienia. Zaleca się, aby na początku infekcji oznaczyć morfologię krwi z rozmazem w celu oceny zdolności do wyrzutu granulocytów, jako potwierdzenie rozpoznania. Poniżej przedstawiono przykładowe zalecenia dla młodej osoby dorosłej, szczepionej wcześniej zgodnie z programem szczepień, z rozpoznaną przewlekłą neutropenią autoimmunizacyjną, bez poważnych powikłań infekcyjnych i innych konsekwencji zdrowotnych:
- w razie infekcji przebiegającej z gorączką należy zlecić morfologię krwi obwodowej z rozmazem w 1.–2. dniu jej trwania (ocena zdolności do wyrzutu granulocytów); do potwierdzenia rozpoznania wystarczy jednorazowe stwierdzenie wyrzutu neutrofili, nie zaleca się powtarzania morfologii w przypadku kolejnych łagodnych infekcji
- poszerzenie immunizacji czynnej o szczepienia
zalecane przeciwko:
– pneumokokom (PCV-13 lub PCV-15 + po upływie ≥2 mies. PPSV-23 lub wyłącznie PCV-20)
– meningokokom (grupy B, A, C, W i Y)
– grypie
– COVID-19 (zgodnie z aktualnymi zaleceniami krajowymi)
– ospie wietrznej (o ile pacjent wcześniej nie był zakażony wirusem VZV) oraz odrze, śwince i różyczce (osoby nieszczepione – 2 dawki szczepionki MMR w odstępie miesiąca, zaszczepione jednorazowo – 1 dawka) - u pacjentów z potwierdzoną przewlekłą neutropenią autoimmunizacyjną lub idiopatyczną można stosować „żywe” szczepionki przeciwbakteryjne
- szczepienia należy realizować zgodnie z ChPL
- wykonywanie morfologii krwi bezpośrednio przed szczepieniem jest nieuzasadnione.
Szczepienia u pacjentów z SCN
SCN jest chorobą uwarunkowaną genetycznie, prowadzącą do ciężkiej neutropenii, którą stwierdza się w morfologii krwi obwodowej. Od przewlekłej łagodnej neutropenii różni się tym, że granulocytów nie stwierdza się również w pozostałych kompartmentach ciała (tkankach, pulach zapasowych). W przypadku infekcji nie obserwuje się wyrzutu granulocytów. Dojrzałe granulocyty nie są wytwarzane i uwalniane ze szpiku kostnego. W badaniu mielogramu stwierdza się zahamowanie dojrzewania granulocytów obojętnochłonnych. SCN zazwyczaj ujawnia się we wczesnym dzieciństwie i ma charakter trwały. Rzadko obserwuje się neutropenię cykliczną. Stały lub okresowy brak granulocytów prowadzi do poważnych powikłań infekcyjnych lub rozwoju głębokich ropni skóry albo narządów wewnętrznych. Cykliczna neutropenia charakteryzuje się regularnym występowaniem objawów chorobowych: zmniejszeniu ANC towarzyszą objawy kliniczne, które zazwyczaj ustępują po zwiększeniu liczby neutrofili do wartości prawidłowych.5
Zalecenia dotyczące ralizacji szczepień u chorych z SCN opracowują specjaliści immunologii klinicznej, ale ich realizacją zwykle zajmują się lekarze POZ. W leczeniu stosuje się czynnik wzrostu kolonii granulocytów (granulocyte colony-stimulating factor – G-CSF), a u osób opornych na G-CSF i z ciężkim przebiegiem klinicznym wskazane jest przeszczepienie komórek krwiotwórczych. Zdecydowana większość pacjentów wymaga realizacji szczepień obowiązkowych i zalecanych z wykorzystaniem szczepionek inaktywowanych oraz „żywych” przeciwwirusowych. Bardzo ważne są szczepienia przeciwko COVID-19. Wielu autorów uważa, że przeciwwskazana jest immunizacja szczepionkami „żywymi” przeciwbakteryjnymi,7-9 choć nie wszyscy się z tym zgadzają. Na stronach SCNIR nie ma informacji na temat przeciwwskazań do stosowania jakichkolwiek szczepionek „żywych” u chorych z SCN.11 Rozsądne jest przyjęcie zasady, że „żywych” szczepionek przeciwbakteryjnych nie należy stosować u chorych z neutropenią i towarzyszącym niedoborem funkcjonalnym granulocytów lub defektem limfocytów T. „Żywe” szczepionki przeciwbakteryjne są również przeciwwskazane u chorych z dramatycznie ciężkim przebiegiem neutropenii, którzy nie odpowiadają na G-CSF, przygotowywanych do przeszczepienia komórek krwiotwórczych.7-9 U pozostałych chorych z SCN należy przeanalizować bilans ryzyka i korzyści związanych z zastosowaniem „żywych” szczepionek przeciwbakteryjnych.
W praktyce klinicznej większość dzieci w chwili rozpoznania SCN szczepienie BCG ma już za sobą. Zgodnie z obowiązującym w Polsce programem szczepień ochronnych nie zaleca innych „żywych” szczepionek przeciwbakteryjnych, o ile pacjent nie planuje podróży do krajów egzotycznych.
Szczepienia pacjentów z neutropenią towarzyszącą innym chorobom
Neutropenia często towarzyszy zakażeniom (np. HIV). Jest również stałym problemem chorych z nowotworami układu krwiotwórczego, poddanych terapii onkologicznej z powodu nowotworów lub immunosupresyjnej (np. w przebiegu chorób autoimmunizacyjnych). W tej grupie pacjentów, niezależnie od wieku, realizacja szczepień ochronnych zależy nie tylko od ciężkości neutropenii, ale także rodzaju choroby podstawowej i jej leczenia. Zalecenia opracowuje specjalista nadzorujący leczenie pacjenta w porozumieniu z lekarzem POZ. U większości pacjentów zaleca się realizację szczepień szczepionkami inaktywowanymi, a przeciwko COVID-19 – szczepionkami mRNA (u dzieci) lub wektorowymi oraz białkowymi (u dorosłych). Często przeciwwskazane są szczepionki „żywe” zarówno przeciwwirusowe, jak i przeciwbakteryjne, gdyż neutropenii zazwyczaj towarzyszą zaburzenia odporności nabytej komórkowej i humoralnej. Ważny jest wybór optymalnego czasu realizacji szczepień. Należy uwzględnić zdolność do odpowiedzi immunologicznej oraz aktualną sytuację epidemiologiczną. W okresie pandemii szczepienia przeciwko COVID-19 zalecano chorym nawet w okresie intensywnej terapii onkologicznej, mimo udowodnionej słabszej odpowiedzi immunologicznej. Jeśli sytuacja epidemiologiczna nie stwarza zagrożenia, należy rozważyć odroczenie szczepienia do czasu zakończenia leczenia i uzyskania rekonstrukcji immunologicznej, co zwiększa szansę na wytworzenie oczekiwanej odpowiedzi immunologicznej.
Chorzy z tej grupy wymagają indywidualnego podejścia do realizacji szczepień, choć znacznie częściej należy je zalecać (zwłaszcza inaktywowane, mRNA lub wektorowe) niż odraczać. Należy zachować ostrożność w przypadku stosowania szczepionek „żywych”. Wyjątkowo rzadko konieczna jest rezygnacja ze wszystkich szczepień ochronnych.
Piśmiennictwo:
1. Summers C., Rankin S.M., Condliffe A.M. i wsp.: Neutrophil kinetics in health and disease. Trends. Immunol., 2010; 31 (8): 318–3242. Akhtari M., Curtis B., Waller E.K.: Autoimmune neutropenia in adults. Autoimmun. Rev., 2009; 9 (1): 62–66
3. Andersen C.L., Tesfa D., Siersma V.D. i wsp.: Prevalence and clinical significance of neutropenia discovered in routine complete blood cell counts: a longitudinal study. J. Intern. Med., 2016; 279 (6): 566–575
4. Hsieh M.M., Everhart J.E., Byrd-Holt D.D. i wsp.: Prevalence of neutropenia in the U.S. population: age, sex, smoking status, and ethnic differences. Ann. Intern. Med., 2007; 146: 486–492
5. Konieczek J., Bartoszewicz N., Richert-Przygońska M. i wsp.: Clinical spectrum of neutropenia in children – analysis of 109 cases Acta Haematol. Pol., 2021; 52 (6): 558–565
6. Wang Y., Qu K., Lu W. i wsp.: Neutrophils recruited to immunization sites initiating vaccine-induced antibody responses by locally expressing BAFF. iScience, 2022; 25 (6): 104 453
7. Bernatowska E., Pac M., Mikołuć B. i wsp.: Standardy szczepień w pierwotnych niedoborach odporności – rekomendacje Polskiej Grupy Roboczej ds. Pierwotnych Niedoborów Odporności oraz Komitetu Immunologii i Etiologii Zakażeń Człowieka Polskiej Akademii Nauk. Stand. Med. Pediatr., 2021; 18: 403–413
8. Kołtan S., Urbańczyk A., Grześk E. i wsp.: Szczepienia ochronne u dzieci w trakcie i po leczeniu onkologicznym oraz w wybranych chorobach hematologicznych: rekomendacje Polskiego Towarzystwa Onkologii i Hematologii Dziecięcej. Acta Haematol. Pol., 2019; 50 (4): 182–191
9. Janczar S., Zalewska-Szewczyk B., Bąbol-Pokora K. i wsp.: Vaccination in children with chronic severe neutropenia – review of recommendations and a practical approach. Cent. Eur. J. Immunol., 2020; 45 (2): 202–205
10. Soyak Aytekin E., Keskin A., Tan C. i wsp.: Differential diagnosis of primary immunodeficiency in patients with BCGitis and BCGosis: a single-centre study. Scand. J. Immunol., 2021; 94: e13084
11. https://severe-chronic-neutropenia.org/en/handbooks