Czy zespół Gianottiego i Crostiego o łagodnym przebiegu, który wystąpił po szczepieniu przeciwko WZW typu A u 18-miesięcznego dziecka, jest przeciwwskazaniem do podania drugiej dawki szczepionki?
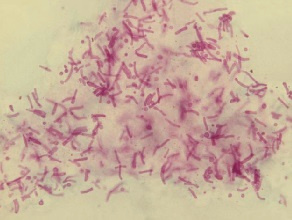
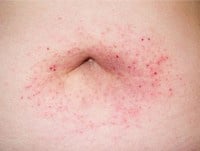
Dziecięce grudkowe zapalenie skóry (papular acrodermatitis of childhood) lub zespół Gianottiego i Crostiego jest łagodną osutką z wykwitami o charakterze grudek zajmujących symetrycznie dystalne części kończyn oraz twarz. Osutka występuje u dzieci w przebiegu różnych zakażeń wirusowych, rzadziej po szczepieniach. Ustępuje samoistnie w ciągu 2–8 tygodni. W przeszłości uważano, że zespół ten jest objawem zakażenia wirusem zapalenia wątroby typu B (HBV). Wykazano jednak, że zwykle pojawia się w przebiegu wielu chorób wirusowych, co sugeruje, że jest to raczej reakcja immunologiczna niż pierwotna manifestacja zakażenia HBV. W Charakterystyce Produktu Leczniczego Havrix Junior nie wymieniono tego zespołu wśród znanych powikłań poszczepiennych, wspomniano jedynie o wysypkach, które występują niezbyt często (od ≥1/1000 do <1/100). W piśmiennictwie dostępne są opisy przypadków zespołu Gianottiego i Crostiego, który wystąpił w związku czasowym z podaniem MMR, DTP, szczepionki przeciwko ospie wietrznej, polio, grypie, japońskiemu zapaleniu mózgu, wirusowemu zapaleniu wątroby (WZW) typu B i A oraz skojarzonej szczepionki Twinrix. Wystąpienie zespołu po szczepieniu jest traktowane jako łagodny, mało istotny klinicznie i przejściowy NOP. Zespół Gianottiego i Crostiego po szczepieniu nie stanowi zatem bezwzględnego przeciwwskazania do podania drugiej dawki szczepionki przeciwko WZW typu A i można kontynuować szczepienia zgodnie ze schematem. Jedynym trwałym i bezwzględnym przeciwskazaniem do szczepienia jest reakcja anafilaktyczna na szczepionkę lub substancję pomocniczą wchodzącą w jej skład.
Po podaniu szczepionki przeciwko WZW typu A zespół występuje bardzo rzadko. Według dostępnych opisów dzieci lepiej tolerują kolejne dawki szczepionki. Pamiętajmy, że wystąpienie NOP może wynikać z koincydencji, czyli zbieżności czasowej. Niektóre opisy wskazują, że ryzyko wystąpienia zespołu zwiększa szczepienie w czasie ostrego zakażenia EBV, które może przebiegać skąpoobjawowo.
Podsumowując, zespół Gianottiego i Crostiego bardzo rzadko występuje po szczepieniu przeciwko WZW typu A. Jest on traktowany jako łagodny odczyn, który nie wymaga rezygnacji z dalszych szczepień, szczególnie że kolejne dawki szczepionki zwykle są lepiej tolerowane.
Piśmiennictwo:
1. Snowden J., Badri T.: Acrodermatitis papular (Gianotti Crosti Syndrome) StatPearls. www.ncbi.nlm.nih.gov/books/NBK441825/2. Robl Imoto R., Uber M., de Carvalho V.O.: Papular crusted rash in a child after immunisation. Arch. Dis. Child., 2019; 104: 706
3. Pedreira R.L., Leal J.M., Silvestre K.J. i wsp.: Gianotti-Crosti syndrome: a case report of a teenager. An. Bras. Dermatol., 2016; 91 (5 suppl 1): 163–165
4. Drago F., Javor S., Ciccarese G. i wsp.: Gianotti-Crosti syndrome as presenting sign of cytomegalovirus infection: A case report and a critical appraisal of its possible cytomegalovirus etiology. J. Clin. Virol., 2016; 78: 120–122
5. Retrouvey M., Koch L.H., Williams J.V.: Gianotti-Crosti syndrome after childhood vaccination. Pediatr. Dermatol., 2012; 29: 666–668
6. Zawar V, Chuh A.: A case-control study on the association of pulse oral poliomyelitis vaccination and Gianotti-Crosti syndrome. Int. J. Dermatol., 2017; 56: 75–79
7. Chuh A., Zawar V., Sciallis G.F. i wsp.: The diagnostic criteria of pityriasis rosea and Gianotti-Crosti syndrome – a protocol to establish diagnostic criteria of skin diseases. J. R. Coll. Physicians Edinb., 2015; 45: 218–225
8. Al Dhaheri H.S., Al Kaabi A., Kara Hamo Y. i wsp.: Unusual presentation of Gianotti-Crosti Syndrome due to Epstein-Barr virus infection. Case Rep. Dermatol. Med., 2016; 2016: 1 017524
9. Taieb A., Plantin P., Du Pasquier P. i wsp.: Gianotti–Crosti syndrome: a study of 26 cases. Br. J. Dermatol., 1986; 115: 49–59
10. Andiran N., Senturk G.B., Bukulmez G.: Combined vaccination by measles and hepatitis B vaccines: a new cause of Gianotti–Crosti syndrome. Dermatology, 2002; 204: 75–76
11. Caputo R., Gelmetti C., Ermacora E. i wsp.: Gianotti–Crosti syndrome: a retrospective analysis of 308 cases. J. Am. Acad. Dermatol., 1992; 1: 207–210
12. Cambiaghi S., Scarabelli G., Pistritto G. i wsp.: Gianotti–Crosti syndrome in an adult after influenza virus vaccination. Dermatology, 1995; 191: 340–341
13. Spear K.L., Winkelmann R.K.: Gianotti–Crosti syndrome. A review of ten cases not associated with hepatitis B. Arch. Dermatol., 1984; 120: 891–896
14. Draelos Z.K., Hansen R.C., James W.D.: Gianotti–Crosti syndrome associated with infections other than hepatitis B. JAMA, 1986; 256: 2386–2388
15. Lacour M., HarmsM.: Gianotti–Crosti syndrome as a result of vaccination and Epstein–Barr virus infection. Eur. J. Pediatr., 1995; 154: 688–689
16. Velangi S.S., Tidman M.J.: Gianotti–Crosti syndrome after measles, mumps and rubella vaccination. Br. J. Dermatol., 1998; 139: 1122–1123
17. Chuh A.A., Chan H.H., Chiu S.S. i wsp.: A prospective case control study of the association of Gianotti–Crosti syndrome with human herpesvirus 6 and human herpesvirus 7 infections. Pediatr. Dermatol., 2002; 19: 492–497
18. Kang N.G., Oh CW.: Gianotti–Crosti syndrome following Japanese encephalitis vaccination. J. Korean. Med. Sci., 2003; 18: 459–461
19. Kolivras A., Andre J.: Gianotti–Crosti syndrome following hepatitis A vaccination. Pediatr. Dermatol., 2008; 25: 650
20. Haug S., Schnopp C., Ring J. i wsp.: Gianotti-Crosti syndrome following immunization. Hautarzt, 2002; 53: 683–685
21. Monastirli A., Varvarigou A., Pasmatzi E. i wsp.: Gianotti-Crosti syndrome after hepatitis A vaccination. Acta Derm. Venereol., 2007; 87: 174–175