Opracowała: Małgorzata Ściubisz, mgr zdrowia publicznego, redaktor „Medycyny Praktycznej – Szczepienia”
Skróty: AIN – śródnabłonkowa neoplazja odbytu, CIN – śródnabłonkowa neoplazja szyjki macicy, ECDC – European Centre for Disease Prevention and Control, HPV – ludzki wirus brodawczaka, HPV-2 – 2-walentna szczepionka przeciwko HPV, HPV-4 – 4-walentna szczepionka przeciwko HPV, HPV-9 – 9-walentna szczepionka przeciwko HPV, VAIN – śródnabłonkowa neoplazja pochwy, VIN – śródnabłonkowa neoplazja sromu
- skuteczność i efektywność 9-walentnej szczepionki przeciwko HPV (HPV-9)
- skuteczność i efektywność szczepionek przeciwko HPV u osób zakażonych HIV
- skuteczność i efektywność szczepionek przeciwko HPV u chłopców i mężczyzn
- efektywność kosztowa programów szczepień obejmujących również mężczyzn.
Wprowadzenie
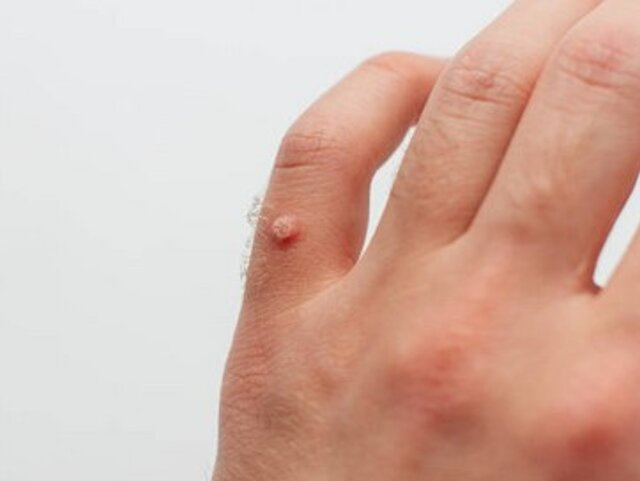
Zakażenie ludzkim wirusem brodawczaka (HPV) jest jednym z najczęstszych zakażeń przenoszonych drogą kontaktów seksualnych na świecie. Do zakażenia dochodzi w krótkim czasie po rozpoczęciu aktywności seksualnej. Uznanie kluczowej roli HPV w etiologii praktycznie wszystkich nowotworów szyjki macicy radykalnie zmieniło podejście do rozpoznawania i zapobiegania tej chorobie. HPV jest także przyczyną innych, rzadziej występujących nowotworów okolicy anogenitalnej i zlokalizowanych poza nią, także u mężczyzn, oraz praktycznie wszystkich brodawek płciowych (kłykcin kończystych). Chorobami związanymi z HPV są zatem obarczone obie płcie. Mimo sukcesu programów przesiewowych badań cytologicznych w kierunku raka szyjki macicy, choroba ta jest nadal ważną przyczyną zachorowalności i umieralności kobiet w Europie. Nie dysponujemy natomiast wysokiej jakości programem badań przesiewowych w kierunku zapobiegania innym niż rak szyjki macicy chorobom związanym z HPV u kobiet ani w kierunku nowotworów związanych z HPV u mężczyzn. W związku z tym szczepienie przeciwko HPV może zapewnić znaczącą, dodatkową korzyść w zapobieganiu wszystkim chorobom związanym z HPV u obu płci.
Obciążenie chorobami związanymi z HPV w Europie
Częstość zakażeń HPV w populacji ogólnej europejskich kobiet szacuje się na 14%, przy czym zależy ona od wieku, a szczyt zachorowań przypada na pierwsze lata od rozpoczęcia aktywności seksualnej (w okresie dojrzewania i wczesnej dorosłości). W populacji mężczyzn częstość zakażeń HPV jest większa niż u kobiet i utrzymuje się na podobnym poziomie, niezależnie od wieku. Tylko niewielki odsetek zakażeń przechodzi w zakażenie przetrwałe, które może prowadzić do rozwoju zmian przedrakowych i raka. Praktycznie za wszystkie przypadki raka szyjki macicy, ale także za znaczący odsetek innych nowotworów okolicy anogenitalnej (sromu, pochwy, prącia i odbytu) oraz zlokalizowanych poza nią (głowy i szyi, w szczególności jamy ustanej i gardła), odpowiadają onkogenne typy HPV (głównie 16 i 18, ale także 31, 33, 35, 39, 45, 51, 52, 56, 58 i 59). Natomiast główną przyczyną brodawek płciowych (kłykcin kończystych) jest HPV typu 6 i 11.
Szacuje się, że w krajach Unii Europejskiej/Europejskiego Obszaru Gospodarczego (UE/EOG) każdego roku rozpoznaje się 33 987 przypadków raka szyjki macicy i 13 239 zgonów z jego powodu, 14 700 przypadków innych nowotworów okolicy anogenitalnej, w tym 5400 wśród mężczyzn (głównie rak odbytu i prącia) i 9300 u kobiet (głównie rak odbytu, pochwy i sromu), 13 997–27 773 przypadków śródnabłonkowej neoplazji sromu (VIN) drugiego lub trzeciego stopnia, 596–4751 przypadków śródnabłonkowej neoplazji pochwy (VAIN) drugiego lub trzeciego stopnia, 2646 przypadków śródnabłonkowej neoplazji odbytu (AIN) drugiego lub trzeciego stopnia, w tym 1549 przypadków wśród kobiet i 1097 wśród mężczyzn, 13 800 przypadków nowotworów okolicy głowy i szyi, głównie u mężczyzn (w ostatnich latach obserwuje się zwiększenie częstości nowotworów głowy i szyi, a zwłaszcza raka jamy ustanej, przy jednoczesnym zmniejszeniu częstości spożycia tytoniu).
Standaryzowane wskaźniki zachorowalności i umieralności z powodu raka szyjki macicy i innych nowotworów związanych z HPV w populacji europejskiej są zróżnicowane. Szacuje się, że:
- zachorowalność na raka szyjki macicy wynosi od 4,1/100 000 na Cyprze do 28,6/100 000 w Rumunii
- umieralność z powodu raka szyjki macicy wynosi od 0,4/100 000 w Islandii do 10,8/100 000 w Rumunii
- zachorowalność na inne nowotwory okolicy anogenitalnej waha się od 0,72/100 000 w Polsce do 2,16/100 000 w Danii
- zachorowalność na nowotwory głowy i szyi waha się od 0,18/100 000 na Cyprze do 3,04/100 000 na Węgrzech
- w Polsce wskaźnik zachorowalności i umieralności z powodu raka szyjki macicy wynosi odpowiednio 12,2/100 000 i 5,4/100 000, a zachorowalność na nowotwory głowy i szyi 1,27/100 000.
Szczególną grupę ryzyka chorób związanych z HPV stanowią osoby zakażone HIV. Dostępne dane wskazują, że częstość zakażeń HPV wśród osób zakażonych HIV jest większa niż u osób niezakażonych. Dodatkowo, związana z HIV immunosupresja może zwiększać ryzyko progresji zakażenia HPV do raka.
Szczepionki przeciwko HPV
Aktualnie w Europie zarejestrowano 3 szczepionki przeciwko HPV (p. tab.), które zasadniczo różnią się liczbą typów HPV uwzględnionych w składzie, nieco wskazaniami do stosowania i zakresem rejestracji (tylko u kobiet lub u mężczyzn i kobiet). Wszystkie 3 szczepionki zawierają cząstki wirusopodobne (virus-like-particles – VLP) HPV typu 16 i 18, które odpowiadają za 71% przypadków raka szyjki macicy.
| Tabela. Charakterystyka szczepionek przeciwko HPV dostępnych w Europie | |||
|---|---|---|---|
| HPV-2 | HPV-4 | HPV-9 | |
| skład antygenowy | białko L1 HPV typu 16, 18 | białko L1 HPV typu 6, 11, 16, 18 | białko L1 HPV typu 6, 11, 16, 18, 31, 33, 45, 52, 58 |
| wskazania | zapobieganie: – nowotworom szyjki macicy lub odbytu – zmianom przednowotworowym narządów płciowych (szyjki macicy, sromu i pochwy) – preparat jest zarejestrowany do stosowania u kobiet |
zapobieganie: – zmianom przednowotworowym narządów płciowych (szyjki macicy, sromu i pochwy) – zmianom przednowotworowym odbytnicy, raka szyjki macicy oraz raka odbytnicy, związanym przyczynowo z zakażeniem pewnymi onkogennymi typami HPV – brodawkom narządów płciowych (kłykcin kończystych) związanych przyczynowo z zakażeniem określonymi typami HPV – preparat jest zarejestrowany do stosowania u obu płci |
zapobieganie: – zmianom przednowotworowym oraz rakowi szyjki macicy, sromu, pochwy i odbytnicy, wywoływanym przez szczepionkowe typy HPV – brodawkom narządów płciowych (kłykcin kończystych) wywoływanych przez określone typy wirusa HPV – preparat jest zarejestrowany do stosowania u obu płci |
| schemat szczepienia | – u osób w wieku 9–14 lat 2 dawki
po 0,5 ml w schemacie 0, 5–13 mies. – u osób w wieku ≥15 lat 3 dawki po 0,5 ml w schemacie 0, 1, 6 mies. |
– u osób wieku 9–13 lat 2 dawki po 0,5 ml w schemacie 0, 6 mies. – u osób w wieku ≥14 lat 3 dawki po 0,5 ml w schemacie 0, 2, 6 mies. |
– u osób w wieku 9–14 lat 2 dawki po 0,5 ml w schemacie 0, 5–13 mies. lub 3 dawki w schemacie 0, 2, 6 mies. – u osób w wieku ≥15 lat 3 dawki po 0,5 ml w schemacie 0, 2, 6 mies. |
| HPV – ludzki wirus brodawczaka, HPV-2 – 2-walentna szczepionka przeciwko HPV, HPV-4 – 4-walentna szczepionka przeciwko HPV, HPV-9 – 9-walentna szczepionka przeciwko HPV | |||
Programy powszechnych szczepień przeciwko HPV w Europie
Do 2019 roku niemal wszystkie kraje UE/EOG wprowadziły szczepienie przeciwko HPV do krajowych programów powszechnych szczepień. Programy powszechnych szczepień dziewcząt prowadzi 30 z 31 krajów (wszystkie oprócz Polski), a w 11 z nich realizowane są także programy szczepień wychwytujących w starszych grupach wiekowych. W 14 z 30 krajów programy powszechnych szczepień rozszerzono na populację chłopców (Austria, Belgia, Chorwacja, Czechy, Dania, Finlandia, Niemcy, Irlandia, Włochy, Holandia, Norwegia, Szwecja, Wielka Brytania), a wiele innych krajów planuje to zrobić w najbliższej przyszłości. W jednym kraju (Lichtenstein) prowadzone są także szczepienia wychwytujące wśród starszych chłopców. W większości krajów szczepienia są w całości finansowane ze środków publicznych, a w kilku krajach pacjent pokrywa część kosztów (głównie dotyczy to szczepień wychwytujących). Różnice w programach w poszczególnych krajach dotyczą przede wszystkim wieku docelowych populacji, który wynosi 9–14 lat w przypadku dziewcząt i chłopców oraz 10–26 lat w programach szczepień wychwytujących dziewcząt i 10–18 lat w programach szczepień wychwytujących chłopców.
Autorzy stanowiska zwracają uwagę na duże różnice w odsetkach docelowych populacji zaszczepionych w ramach programów nie tylko między krajami, ale także w regionach poszczególnych państw. W 2019 roku w Finlandii, na Węgrzech, Islandii, Malcie, Norwegii, Portugalii, Hiszpanii, Szwecji i Wielkiej Brytanii odsetek ten wyniósł >70%, choć w niektórych krajach nadal utrzymuje się <50% (Francja, Niemcy). W ostatnich latach w Danii i Irlandii obserwowano słabszą realizację programów szczepień przeciwko HPV i istotne zmniejszenie wyszczepialności, którą sukcesywnie odbudowują dzięki skutecznym kampaniom promującym szczepienia. Do 2015 roku w krajach UE/ EOG wszystkie należne dawki szczepionki przeciwko HPV otrzymało 14 mln kobiet, a ≥1 dawkę szczepionki 17 mln. W przyszłości może to zapobiec 76 000 zachorowań na raka szyjki macicy u zaszczepionych dziewcząt.
Zgodnie z polskim Programem Szczepień Ochronnych szczepienie przeciwko HPV zaleca się dziewczętom w wieku 11–12 lat, ale nie jest finansowane (koszt zakupu szczepionki pokrywa pacjent). Polskie Towarzystwo Pediatryczne zaleca także szczepienie przeciwko HPV wcześniej nieszczepionym dziewczętom w wieku 13–14 lat. Bezpłatne programy szczepień realizują niektóre samorządy terytorialnego. Szacuje się, że wyszczepialność polskich nastolatek wobec HPV wynosi 7,5–10%.
Bezpieczeństwo i nadzór nad szczepionkami przeciwko HPV
Bardzo dobry profil bezpieczeństwa wszystkich 3 dostępnych aktualnie szczepionek przeciwko HPV potwierdzono w badaniach przedrejestracyjnych. Dalszy ciągły nadzór prowadzi European Medicines Agency (EMA) oraz inne międzynarodowe i krajowe agencje regulacyjne monitorujące bezpieczeństwo szczepionek.
Zgromadzone dotąd dane dotyczące bezpieczeństwa szczepionek przeciwko HPV nie wykazują niepokojących sygnałów. W analizie przeprowadzonej przez Global Advisory Committee for Vaccine Safety (GACVS) działający przy Światowej Organizacji Zdrowia (WHO) nie potwierdzono, aby szczepienie przeciwko HPV było związane przyczynowo z występowaniem chorób autoimmunizacyjnych (w tym zespołu Guillaina i Barrégo oraz stwardnienia rozsianego), żylnej choroby zakrzepowo-zatorowej, udaru mózgu, zespołu bólu regionalnego, zespołu posturalnej tachykardii ortostatycznej (p. Szczepienie przeciwko HPV a zespół bólu regionalnego i posturalnej tachykardii ortostatycznej – przyp. red.), przedwczesnej niewydolności jajników (p. Szczepienia a pierwotna niewydolność jajników – czy istnieje związek? - przyp. red.), czy niepomyślnymi następstwami dla ciąży (p. Dwie dawki 4-walentnej szczepionki przeciwko HPV były skuteczne w zapobieganiu występowania brodawek narządów płciowych u kobiet, Podanie szczepionki przeciwko HPV w okresie okołokoncepcyjnym nie wpłynęło na przebieg ciąży, Szczepienie przeciwko HPV a ryzyko powikłań ciąży, Przypadkowe zaszczepienie ciężarnej przeciwko HPV – przyp. red.). Bezpieczeństwo szczepienia przeciwko HPV w odniesieniu do występowania zespołu bólu regionalnego i zespołu posturalnej tachykardii ortostatycznej potwierdziła także EMA w przeglądzie z 2015 roku. Ryzyko anafilaksji po szczepieniu przeciwko HPV jest bardzo małe i podobne do ryzyka obserwowanego po podaniu innych szczepionek (1,7 przypadków/1 000 000 dawek). Również ryzyko omdlenia związanego z lękiem i stresem towarzyszącym wstrzyknięciu, które obserwuje się głównie u nastolatków, jest podobne do ryzyka obserwowanego przy podawaniu innych szczepionek.
Skuteczność szczepionek przeciwko HPV i efekty programów szczepień
Populacyjne efekty programów szczepień przeciwko HPV
Od czasu zarejestrowania pierwszej szczepionki przeciwko HPV (2006 r.) zgromadzono wiele danych dotyczących efektów programów powszechnych szczepień przeciwko HPV (p. Co wiadomo o populacyjnych efektach szczepień przeciwko HPV?– przyp. red.). W 2019 roku opublikowano metaanalizę obejmującą 40 badań obserwacyjnych przeprowadzonych w 14 krajach (p. Jak powszechne szczepienia przeciwko HPV wpłynęły na epidemiologię zakażeń oraz chorób związanych z tym wirusem? – przyp. red.), w której wykazano, że powszechne szczepienie dziewcząt przeciwko HPV szczepionką 2- lub 4-walentną istotnie zmniejszyło częstość wykrywania CIN co najmniej średniego stopnia, brodawek płciowych i zakażenia HPV typu 16, 18, 31, 33 i 45 u płci żeńskiej. Stwierdzono także wytworzenie efektu odporności zbiorowiskowej w populacjach nieuprawnionych do powszechnych szczepień (płeć męska, kobiety w starszych grupach wiekowych). Korzystny wpływ programów powszechnych szczepień przeciwko HPV na częstość zakażeń tym wirusem w populacji szczepionych kobiet potwierdzono także w badaniach przeprowadzonych w Australii, Belgii, Finlandii, Francji, Niemczech, Holandii, Hiszpanii, Szwecji i Wielkiej Brytanii, w populacji szczepionych kobiet i mężczyzn w Stanach Zjednoczonych, w populacji nieszczepionych kobiet w Wielkiej Brytanii oraz nieszczepionych mężczyzn w Australii. Dane z Australii, Belgii, Kanady, Danii, Niemiec, Izraela, Włoch, Nowej Zelandii, Hiszpanii, Szwecji, Wielkiej Brytanii oraz Stanów Zjednoczonych potwierdzają także korzystny wpływ programów powszechnych szczepień na częstość CIN dużego stopnia w populacji szczepionych kobiet. W Australii efekt ten obserwowano wśród kobiet w wieku do 30 lat.Dane dotyczące skuteczności HPV-9
Skuteczność HPV-9 u dziewcząt i kobiet
Dane dotyczące skuteczności HPV-9 w zapobieganiu istotnym klinicznie punktom końcowym związanym z HPV u dziewcząt i kobiet w wieku 16–26 lat pochodzą z dużego badania z randomizacją (p. Skuteczność 9-walentnej szczepionki przeciwko HPV u kobiet w wieku 16-26 lat – przyp. red.). Wykazano w nim, że HPV-9, w porównaniu z HPV-4, zmniejsza ryzyko przetrwałego zakażeniu HPV o 96% (95% CI: 94,6–97,1), CIN, VIN, VAIN co najmniej wysokiego stopnia o 97,4% (95% CI: 85–99,9), CIN co najmniej wysokiego stopnia o 97,1% (95% CI: 83,5–99,9), VIN, VAIN co najmniej wysokiego stopnia o 100% (95% CI: 71,5–100) wywołanych przez typy wirusa uwzględnione wyłącznie w składzie HPV-9 (typ 31, 33, 45, 52, 58) oraz przez HPV typu 6, 11, 16 i 18 (skuteczność nie gorsza niż HPV-4). Dodatkowo w badaniach oceniających immunogenność wykazano, że w odniesieniu do HPV typu 6, 11, 16 i 18 serokonwersję obserwowano u podobnego odsetka kobiet w wieku 16–26 lat szczepionych HPV-4 i HPV-9. U dziewcząt w wieku 9–15 lat badania immunogenności wskazują na brak przewagi HPV-4 nad HPV-9 w odniesieniu do typów 6, 11, 16 i 18 oraz na silniejszą odpowiedź immunologiczną na dodatkowe typy HPV (31, 33, 45, 52 i 58) uwzględnione w składzie HPV-9. Serokonwersję po szczepieniu HPV-9 obserwowano u podobnego odsetka kobiet w wieku 9–15 lat i 16–26 lat.
Skuteczność HPV-9 u chłopców i mężczyzn
Nie dysponujemy bezpośrednimi danymi potwierdzającymi skuteczność HPV-9 w zapobieganiu przetrwałemu zakażeniu HPV i związanym z nim chorobom u chłopców i mężczyzn. Badania oceniające immunogenność HPV-9 sugerują brak przewagi HPV-4 nad HPV-9 w odniesieniu do typów 6, 11, 16 i 18 oraz silniejszą odpowiedź immunologiczną na dodatkowe typy HPV 31, 33, 45, 52 i 58 uwzględnione w składzie HPV-9. Na tej podstawie o skuteczności HPV-9 w zapobieganiu przetrwałym zakażeniom i chorobom wywołanym HPV typu 6, 11, 16 i 18 możemy wnioskować z badań dotyczących HPV-4 (p. dalej „Skuteczność HPV-4 i HPV-2 u chłopców i mężczyzn” – przyp. red.). Wykazano również większą immunogenność HPV-9 u chłopców w wieku 9–15 lat niż u kobiet w wieku 16–26 lat.
Skuteczność HPV-4 i HPV-2 u chłopców i mężczyzn
Aktualnie dowody na skuteczność HPV-4 i HPV-2 w zapobieganiu przetrwałemu zakażeniu HPV i związanym z nim chorobom u chłopców i mężczyzn są ograniczone. W badaniach dotyczących immunogenności wykazano, że u chłopców w wieku 9–15 lat immunogenność HPV-4 jest nie gorsza niż u dziewczynek w tym samym wieku i większa niż u kobiet w wieku 16–23 lat. Po szczepieniu HPV-2 serokonwersja utrzymywała się przez ≥42 miesiące u wszystkich chłopców w wieku 9–15 lat, a immunogenność była większa niż u kobiet w wieku 16–26 lat. W 1 badaniu z randomizacją wykazano, że u mężczyzn w wieku 16–26 lat (również u mężczyzn utrzymujących kontakty homoseksualne) HPV-4, w porównaniu z placebo, zmniejszała ryzyko przetrwałego zakażenia HPV o 85,6% (95% CI: 73,4–92,9), brodawek płciowych o 89,4% (95% CI: 65,5–97,9), AIN drugiego lub trzeciego stopnia o 74,9% (95% CI: 8,8–95,4) i śródnabłonkowej neoplazji prącia (PeIN) o 100% (od -3788,2 do 100.0). Natomiast nie znaleziono danych na temat skuteczności szczepionki 2-walentnej (HPV-2) w zapobieganiu zakażeniu HPV i związanym z nim chorobom u mężczyzn.
Skuteczność szczepionek przeciwko HPV u osób zakażonych HIV
Nie ma bezpośrednich dowodów na skuteczność szczepienia przeciwko HPV w zapobieganiu klinicznym punktom końcowym związanym z HPV u osób zakażonych HIV, choć w 2018 i 2019 roku pojawiły się niskiej jakości dane wskazujące na skuteczność HPV-4 w zapobieganiu przetrwałemu zakażeniu HPV i zakażeniu HPV w obrębie jamy ustnej. Badania dotyczące immunogenności wskazują, że po szczepieniu HPV-4 i HPV-2 serokonwersję obserwowano u dużego odsetka osób zakażonych HIV, ale niższe miana przeciwciał niż u osób niezakażonych HIV.
Efektywność kosztowa rozszerzenia programów szczepień na populację mężczyzn
W odniesieniu do efektywności kosztowej, na podstawie analizy badań modelowych stwierdzono, że jeżeli priorytetem jest zapobieganie chorobom szyjki macicy, rozszerzenie aktualnych programów szczepień na mężczyzn będzie coraz bardziej efektywne kosztowo w przypadku utrzymywania się mniejszej wyszczepialności wśród kobiet oraz mniejszego kosztu szczepionek. Jednak skupienie się na zwiększeniu odsetka zaszczepionych dziewcząt może mieć nadal przewagę w odniesieniu do efektywności kosztowej. Jeżeli celem programu szczepień przeciwko HPV jest zapobieganie chorobom związanym z zakażeniem HPV, efektywniejsze kosztowo mogą być powszechne szczepienia dla obu płci.
Implikacje dla zdrowia publicznego
Implikacje dla aktualnie prowadzonych programów powszechnych szczepień
Większe korzyści i efekt ochronny można uzyskać, szczepiąc osoby przed okresem pokwitania, ponieważ szczepienie jest skuteczniejsze u osób niezakażonych typami HPV uwzględnionymi w szczepionce. Szczepionki są również bardziej immunogenne u młodszych osób. Choć przy aktualnych kosztach szczepionek, szczepienia przeznaczone wyłącznie dla płci żeńskiej, w której grupą docelową są dziewczynki przed okresem pokwitania, są prawdopodobnie efektywniejsze kosztowo, to nie zapewniają wystarczającej ochrony mężczyznom utrzymującym kontakty homoseksualne. Strategia taka jest również bardziej wrażliwa na nagłe zmniejszanie się wskaźników wyszczepialności. Rozszerzenie programów powszechnych szczepień na nastolatki obojga płci może również zapewnić lepszą odporność zbiorowiskową przy mniejszych wskaźnikach wyszczepialności. Wydaje się, że programy powszechnych szczepień realizowane z użyciem HPV-9 mogą być szczególnie korzystne dla dorosłych już zakażonych jakimś typem HPV, na przykład dla osób zakażonych HIV, mężczyzn utrzymujących kontakty homoseksualne i kobiet w wieku >25 lat.
Aspekty społeczne
Zaobserwowano, że kobiety o niższym statusie społeczno-ekonomicznym częściej chorują na raka szyjki macicy, jednocześnie rzadziej korzystają z przesiewowych badań cytologicznych. Dane z niektórych krajów europejskich wskazują, że dostęp do szczepienia przeciwko HPV jest podobny we wszystkich grupach społecznych. Utrzymanie dużego wskaźnika wyszczepialności nie tylko w całej populacji, ale również we wszystkich subpopulacjach (np. w zależności od regionu, pochodzenia etnicznego, statusu społeczno-ekonomicznego), jest kluczowe w ograniczaniu nierówności w zdrowiu. Zatem jeżeli wskaźniki wyszczepialności są mniejsze w konkretnych subpopulacjach, wskazane może być skierowanie działań i zasobów na poprawienie wyszczepialności w tych niedostatecznie zaszczepionych grupach.
Względy etyczne
Mężczyźni utrzymujący kontakty homoseksualne są narażeni na większe ryzyko zakażenia HPV, przy czym nie odnoszą oni korzyści z programów powszechnych szczepień obejmujących tylko dziewczęta. Rozszerzenie programów powszechnych szczepień tylko o tę grupę ryzyka może stanowić duże wyzwanie, ponieważ identyfikacja w tak młodym wieku mężczyzn utrzymujących kontakty homoseksualne jest właściwie niemożliwa, co będzie skutkowało suboptymalną wyszczepialnością. Wydaje się zatem, że program powszechnych szczepień przeciwko HPV nastolatków obojga płci zapewniałby bezpośrednią ochronę przed chorobami związanymi z HPV również u mężczyzn utrzymujących kontakty homoseksualne. W przypadku ograniczonego dostępu szczepionek przeciwko HPV w pierwszej kolejności preferuje się realizację programów powszechnych szczepień dziewcząt.
Możliwe implikacje dotyczące szczepienia osób zakażonych HIV
Aktualnie dysponujemy ograniczonymi dowodami na skuteczność szczepienia w zapobieganiu klinicznym punktom końcowym związanym z HPV u osób zakażonych HIV. Dane dotyczące immunogenności sugerują jednak, że serokonwersję po szczepieniu przeciwko HPV obserwuje się u większości osób zakażonych HIV (choć immunogenność szczepionek może zależeć od statusu immunologicznego, np. liczby limfocytów CD4). Nie ma też żadnych niepokojących sygnałów dotyczących bezpieczeństwa szczepienia przeciwko HPV w tej grupie. Korzyści ze szczepienia mogą zatem odnieść także osoby zakażone HIV. Ogólna zasada, że szczepienie w młodszym wieku wiąże się z lepszą odpowiedzią immunologiczną, powinna dotyczyć także osób zakażonych HIV, zwłaszcza że są one obciążone większym ryzykiem zakażenia HPV (co może dodatkowo zmniejszać korzyści ze szczepienia).
Możliwe implikacje dotyczące zjawiska niepewności wobec szczepień
Kluczowe znaczenie dla zwiększenia i utrzymania dużego odsetka dziewcząt korzystających z programów powszechnych szczepień przeciwko HPV ma wiedza i postawa personelu medycznego placówek ochrony zdrowia. Personel medyczny postrzegany jest jako najbardziej zaufane źródło informacji na temat szczepień ochronnych i ma największy wpływ na decyzje o szczepieniu podejmowane przez pacjentów. Zatem stanowisko personelu medycznego wobec szczepień przeciwko HPV może mieć istotny wpływ na zachowanie pacjentów, a tym samym na niepewność wobec szczepień (vaccine hesitancy) i ich ogólną akceptację.
Zagadnienia wymagające dalszych badań
Po dokonaniu przeglądu i omówieniu zebranych danych grupa ekspertów zidentyfikowała obszary wymagające dalszych badań. Są to m.in.:
- skuteczność i efektywność wszystkich dostępnych szczepionek przeciwko HPV u mężczyzn
- ochrona krzyżowa wszystkich dostępnych szczepionek przeciwko HPV
- czas utrzymywania się ochrony po szczepieniu przeciwko HPV i jej jakości
- wzorce transmisji HPV pomiędzy płciami, wewnątrz tej samej płci i w zależności od wieku
- efekty szczepienia przeciwko HPV w zależności od wzorców transmisji (np. w zależności od liczby partnerów seksualnych, dróg transmisji zakażenia i wskaźników wyszczepialności)
- skuteczność jednej dawki szczepionki przeciwko HPV u osób, które nie ukończyły pełnego schematu
- dodatkowe korzyści ze szczepienia HPV-9 u kobiet i mężczyzn w wieku >25 lat
- skuteczność i efektywność HPV-2 u mężczyzn
- skuteczność szczepionek przeciwko HPV i kinetyka powstawania swoistych przeciwciał u osób zakażonych HIV
- skuteczność szczepionek przeciwko HPV w zapobieganiu brodawkom płciowych i AIN u mężczyzn utrzymujących kontakty homoseksualne
- częstość zakażeń HPV w obrębie jamy ustnej w zależności od wieku
- skuteczność szczepionek przeciwko HPV w zapobieganiu zakażeniu w obrębie jamy ustnej u mężczyzn
- skuteczność szczepionek przeciwko HPV u osób z niedoborami odporności (w tym u osób zakażonych HIV)
- immunologiczne korelaty ochrony oraz możliwość ich wykorzystania w nadzorze epidemiologicznym
- wpływ szczepień przeciwko HPV na wykonywanie przesiewowych badań cytologicznych w kierunku raka szyjki macicy
- możliwy związek przyczynowy między zakażeniem HPV a innymi chorobami
- ciągłe monitorowanie zjawiska zastępowalności serotypów HPV, niepowodzenia szczepienia przeciwko HPV
- czynniki mające wpływ na wskaźniki wyszczepialności i ich nagłe zmniejszenie.
Kolejne kroki
Aktualnie trwają badania w kilku obszarach będących przedmiotem niniejszego opracowania. Dotyczą one m.in. skuteczności rzeczywistej (efektywności) szczepionek w zapobieganiu chorobom związanym z HPV, rozpowszechnienia zakażeń HPV w obrębie jamy ustanej i gardła, skuteczności 1-dawkowego schematu szczepienia przeciwko HPV oraz populacyjnych efektów programów powszechnych szczepień. Istotne znaczenia dla zwiększenia skuteczności interwencji i poprawienia jej wydajności będą mieć także dodatkowe dane z bezpośrednich porównań (head to head) aktualnie dostępnych szczepionek przeciwko HPV oraz dotyczące stosowania mieszanych schematów szczepienia (tj. z użyciem różnych preparatów).
Badania przesiewowe w erze szczepień przeciwko HPV
Pierwsze kohorty dziewcząt szczepionych przeciwko HPV w ramach krajowych programów szczepień zaczynają wchodzić w wiek należny dla rozpoczęcia przesiewowych badań cytologicznych w kierunku raka szyjki macicy. Badania opublikowane w latach 2016–2018 sugerują, że w populacjach częściowo szczepionych przeciwko HPV mniej intensywne programy badań przesiewowych w kierunku raka szyjki macicy, tj. rozpoczynane w późniejszym wieku, wykonywane rzadziej, wyjściowo mniej inwazyjnymi metodami, mogą przynieść podobne, a nawet większe korzyści (przy jednocześnie mniejszych kosztach), niż utrzymanie aktualnie obowiązujących zaleceń.
(W oryginale 205 pozycji piśmiennictwa.)