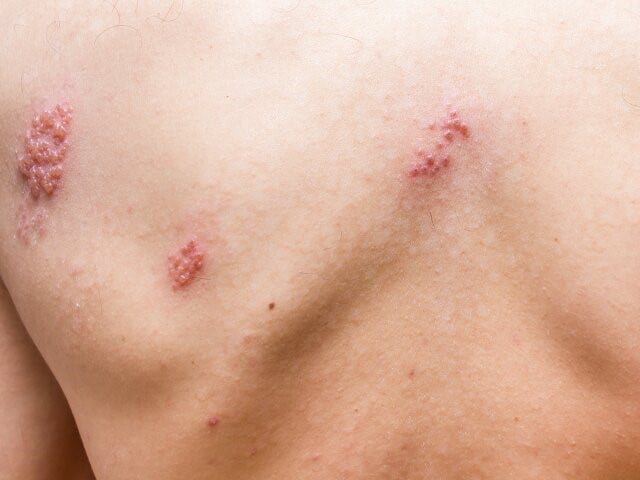
Jakie informacje dotyczące bezpieczeństwa i ewentualnych niepożądanych odczynów poszczepiennych (NOP) należy przekazać pacjentowi przed szczepieniem przeciwko półpaścowi? Czy istnieje ryzyko zespołu Guillaina i Barrégo (ZGB) po szczepieniu?
Rekombinowana szczepionka przeciwko półpaścowi (RZV) zawiera adiuwant AS01B, który wzmacnia odpowiedź immunologiczną na szczepionkę, ale jednocześnie nieco zwiększa jej reaktogenność, czyli ryzyko typowych miejscowych i ogólnoustrojowych NOP. Zatem przed szczepieniem przeciwko półpaścowi należy o tym poinformować pacjenta. Tolerancję i bezpieczeństwo RZV potwierdzono w 2 głównych badaniach z randomizacją (RCT) przeprowadzonych w populacji osób w wieku ≥50 lat i ≥70 lat. W badaniu obejmującym dorosłych w wieku ≥50 lat wykazano, że w grupie szczepionej, w porównaniu z grupą placebo, znacznie częściej obserwowano typowe miejscowe (81,5 vs 11,9%) i ogólnoustrojowe (66,1 vs 29,5%) NOP. Reakcje miejscowe o nasileniu utrudniającym codzienną aktywność zgłosiło odpowiednio 9,5 vs 0,4% uczestników, a ogólnoustrojowe – 11,4 vs 2,4%. Podobne obserwacje płyną z badania obejmującego starszych dorosłych w wieku ≥70 lat. W grupie szczepionej, w porównaniu z grupą placebo, znacznie częściej obserwowano typowe miejscowe (74,1 vs 9,9%) i ogólnoustrojowe (53 vs 25,1%) NOP. Natomiast reakcje miejscowe o nasileniu utrudniającym codzienną aktywność zgłosiło odpowiednio 8,5 vs 0,2% uczestników, a ogólnoustrojowe – 6 vs 2%. Najczęściej zgłaszanym NOP był ból w miejscu wstrzyknięcia i zmęczenie. Pacjenta warto jednak uspokoić, że reakcje te miały samoograniczający się charakter i ustępowały w ciągu 1–2 dni, oraz poinformować, że w razie pojawienia się uciążliwych objawów można zastosować leki przeciwgorączkowe lub przeciwbólowe. Warto również wyjaśnić, że miejscowe i ogólnoustrojowe NOP, nawet o większym nasileniu, nie są przeciwwskazaniem do przyjęcia drugiej dawki szczepionki.
Niepokój pacjenta może wzbudzić informacja w ulotce dołączonej do szczepionki dotycząca zwiększonego ryzyka ZGB po podaniu RZV. W piśmiennictwie medycznym można znaleźć liczne doniesienia o związku czasowym szczepień z występowaniem chorób autoimmunizacyjnych, a za związkiem przyczynowo-skutkowym przemawiają tylko pojedyncze doniesienia. Nie istnieją jednoznaczne kryteria, które pozwoliłyby stwierdzić, kiedy przyczyna? choroby autoimmunizacyjnej było szczepienie. Każdy przypadek należy analizować indywidualnie. World Health Organization (WHO) zaproponowała następujące wskazówki, które pomagają ocenić, czy taka zależność jest prawdopodobna: (1) zgodność danych (consistency) i siła związku (strength) – takie samo zdarzenie obserwuje się po podaniu tej samej szczepionki w różnych grupach, przez różnych badaczy, (2) swoistość – związek powinien być dla określonej szczepionki i choroby, (3) związek czasowy – udokumentowany związek czasowy między szczepieniem a wystąpieniem choroby autoimmunizacyjnej lub zaostrzeniem już istniejącej. Podanie szczepionki powinno wyprzedzać najwcześniejsze objawy choroby.
W latach 1976–1977 ZGB występował u osób szczepionych przeciwko grypie preparatem zawierającym szczep A/New Jersey/8/76 wirusa grypy. Szacowane ryzyko wyniosło wówczas 1/100 000 szczepionych i było największe w okresie 5 tygodni po szczepieniu (ryzyko względne [RR]: 7,60). Obecnie szczep ten nie jest używany do produkcji szczepionek, a ryzyko ZGB ocenia się na bardzo małe – 1 przypadek/milion podanych dawek. Jest ono znacznie mniejsze od ryzyka związanego z zachorowaniem na grypę i rozwoju jej powikłań, do których należy również ZGB. Dane dotyczące bezpieczeństwa z RCT, które były podstawą rejestracji szczepionki przeciwko półpaścowi, zasadniczo nie wzbudziły obaw związanych z autoimmunizacją. Jednak niedawno, już po wprowadzeniu RZV do stosowania w praktyce, amerykański Food and Drug Administration (FDA) zgłosił potencjalne zwiększenie ryzyka ZGB na podstawie wyników badania obserwacyjnego, w którym uwzględniono populację osób w wieku ≥65 lat objętych ubezpieczeniem Medicare. Wykazano jednak, że szacowane ryzyko, które można przypisać RZV, było niewielkie i wyniosło około 3 przypadków/milion podanych dawek tej szczepionki (p. Czy szczepienie przeciwko półpaścowi wpływa na ryzyko wystąpienia zespołu Guillaina i Barrégo? – przyp. red.). W związku z tym w ramach aktywnego populacyjnego nadzoru nad bezpieczeństwem szczepień przeprowadzono prospektywną analizę (niemal w czasie rzeczywistym) danych z dużych baz danych opieki zdrowotnej w USA w celu oceny bezpieczeństwa RZV. Badanie przeprowadzono w ramach projektu Vaccine Safety Datalink (VSD) nadzorowanego przez Centers for Disease Control and Prevention (CDC). W analizie uwzględniono 647 833 dawek szczepionki RZV podanych osobom w wieku ≥50 lat w latach 2018–2019 i porównano z historyczną grupą kontrolną osób, którym podano „żywą” szczepionkę przeciwko półpaścowi (ZVL). W analizowanym okresie odnotowano 6 prawdopodobnych przypadków ZGB w okresie do 42 dni po podaniu RZV, w porównaniu z oczekiwanymi 5 przypadkami (na podstawie liczby zdarzeń po podaniu ZVL). Wszystkie prawdopodobne przypadki ZGB po podaniu RZV i ZVL poddano dodatkowej ocenie i weryfikacji rozpoznania na podstawie dokumentacji medycznej. Spośród 6 potencjalnych przypadków ZGB w okresie po podaniu RZV, 3 uznano za ZGB, a 3 kolejne przeklasyfikowano, ponieważ pierwsze objawy choroby pojawiły się już przed szczepieniem. Z kolei spośród 5 potencjalnych przypadków ZGB w okresie po podaniu ZVL, 2 przypadki potwierdzono, 2 kolejne wykluczono, a w przypadku 1 zachorowania dane medyczne nie były dostępne. Autorzy analizy – przyjmując ostrożnie, że przypadek w grupie kontrolnej, dla którego dane nie były dostępne, w rzeczywistości nie był ZGB – nie stwierdzili istotnie statystycznie zwiększonego ryzyka ZGB w okresie do 42 dni po podaniu RZV (RR: 1,56 [95% CI: 0,18–18,62]). Zwrócili jednak uwagę, że liczba przypadków ZGB była mała, co sprawia, że precyzja oszacowania jest mała i z pewnością należy przeprowadzić kolejne badania. W razie wątpliwości pacjenta należy poinformować, że dostępne dane wskazują na związek RZV z występowaniem ZGB (dlatego takie ostrzeżenie zamieszczono w ulotce), ale nie ma dowodów, że ma on charakter przyczynowy. Zakładając jednak, że taki związek istnieje, ryzyko ZGB po podaniu RZV jest ekstremalnie małe i wynosi około 3 przypadki/milion podanych dawek. Warto dodać, że razie wystąpienia niepokojących objawów (osłabienie siły mięśni lub uczucie mrowienia [zwłaszcza w kończynach dolnych lub górnych], nasilające się i stopniowo obejmujące inne części ciała, trudności w chodzeniu, problemów z mówieniem, żuciem lub połykaniem, podwójne widzenie lub zaburzenia ruchomości gałek ocznych, trudności z trzymaniem moczu lub zaburzenia czynności jelit) pacjent powinien zgłosić się do lekarza. Pacjenta warto również uświadomić, że ZGB jest chorobą, która w populacji częściej występuje bez związku ze szczepieniem, na przykład jako powikłanie infekcji wirusowych.
Piśmiennictwo:
1. Lal H., Cunningham A.L., Godeaux O. i wsp.: Efficacy of an adjuvanted herpes zoster subunit vaccine in older adults. N. Engl. J. Med., 2015; 372 (22): 2087–20962. Cunningham A.L., Lal H., Kovac M. i wsp.: Efficacy of the herpes zoster subunit vaccine in adults 70 years of age or older. N. Engl. J. Med., 2016; 375 (11): 1019–1032
3. Anderson T.C., Masters N.B., Guo A. i wsp.: Use of recombinant zoster vaccine in immunocompromised adults aged ≥19 years: recommendations of the Advisory Committee on Immunization Practices – United States, 2022. MMWR, 2022; 71 (3): 80–84
4. Więsik-Szewczyk E., Jahnz-Różyk K.: Autoimmunizacyjne układowe choroby tkanki łącznej a szczepienia ochronne. Postępy Hig. Med. Dosw., 2015; 69: 1530–1538
5. Causality assessment of adverse events following immunization. Wkly. Epidemiol. Rec., 2001; 76: 85–89
6. Lasky T., Terracciano G.J., Magder L. i wsp.: The Guillain-Barré syndrome and the 1993–1993 and 1993–1994 influenza vaccines. N. Engl. J. Med., 1998; 339: 1797–1802
7. Nelson J.C., Ulloa-Pérez E., Yu O. i wsp.: Active postlicensure safety surveillance for recombinant zoster vaccine using electronic health record data. Am. J. Epidemiol., 2023; 192 (2): 205–216