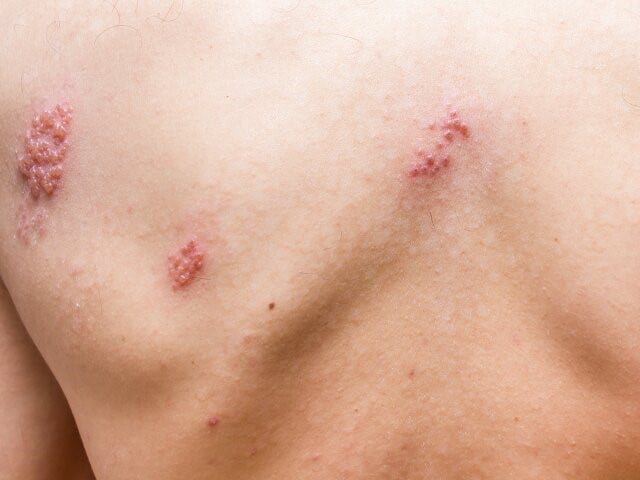
Aktualnie nie ma silnych zaleceń dotyczących podawania dawek przypominających zarówno po szczepieniu „żywą” szczepionką przeciwko półpaścowi (ZLV), jak i szczepionką rekombinowaną (RZV). W przypadku ZLV zaobserwowano stopniowe zmniejszanie się skuteczności w miarę upływu czasu. Stwierdzono, że już rok po szczepieniu jego skuteczność istotnie się zmniejsza, a po 6 latach wynosiła <35%. W jak dotąd najdłuższym badaniu obserwacyjnym stwierdzono, że skuteczność szczepionki zmniejsza się przez 9–11 lat po szczepieniu, po tym okresie nie obserwowano już istotnych różnic. W Niemczech w 2017 roku Stały Komitet ds. Szczepień Ochronnych (STIKO) podjął decyzję przeciwko zalecaniu rutynowego szczepienia preparatem ZLV. Od 18 listopada 2020 roku ZLV nie jest też dostępna w USA, gdzie zgodnie z zaleceniami amerykańskiego Advisory Committee on Immunization Practices (ACIP) szczepienie z użyciem RZV jest preferowane względem ZLV.
Obecnie trwa badanie obserwacyjne ZOE-LTFU, które ma na celu długoterminową ocenę jej skuteczności, immunogenności i bezpieczeństwa RZV. Jest to badanie obserwacyjne, będące kontynuacją RCT III fazy ZOE-50 i ZOE-70, w których oceniono skuteczność i bezpieczeństwo tego preparatu u osób w wieku ≥50 lat i ≥70 lat (p. Skuteczność i bezpieczeństwo szczepionek przeciwko półpaścowi – przyp. red.). W październiku 2022 roku opublikowano wstępne wyniki badania ZOE-LTFU, w ramach którego uczestników RCT ZOE-50 i ZOE-70 obserwowano przez okres do 10 lat. Wykazano, że skuteczność RZV w zapobieganiu zachorowaniom na półpasiec nieco się zmniejszyła, jednak w przeciwieństwie do ZLV, po 10 latach nadal była duża i wyniosła 73,2%. U osób w wieku ≥50 lat zapadalność na półpasiec zwiększyła się z 0,2/1000 osobodni w 1. roku po szczepieniu do 2,3/1000 osobodni po 10 latach od szczepienia, zaś w grupie otrzymującej placebo utrzymywała się na średnim poziomie około 8,7/1000 osobodni. W badaniu wykazano też utrzymującą się dużą immunogenność zarówno w zakresie odpowiedzi humoralnej, jak i komórkowej. Dane te wskazują, że około 10 lat po szczepieniu przeciwko półpaścowi preparatem RZV jego skuteczność nadal jest duża.
Różnice w skuteczności RZV i ZLV są szczególnie widoczne u osób starszych (>70. rż.). U osób w wieku 70–79 lat oraz ≥90 lat po 3 latach od szczepienia ZLV skuteczność wynosiła odpowiednio 41 i 18%. Ze względu na zmniejszanie się skuteczności ZLV, u pacjenta zaszczepionego uprzednio tym preparatem można rozważyć podanie RZV, zwłaszcza jeśli ma >70 lat. Należy jednak uwzględnić wiek pacjenta oraz datę otrzymania ZLV. W badaniu RCT III fazy oceniono bezpieczeństwo i immunogenność szczepionki RZV podanej ≥5 lat po ZVL. Nie stwierdzono, aby wcześniejsze podanie ZLV miało wpływ na odpowiedź immunologiczną po podaniu RZV. Nie oceniono krótszych przedziałów czasu. Jednak według ACIP nie ma danych ani teoretycznych przesłanek, aby krótszy odstęp między ZVL i RZV był mniej skuteczny lub bezpieczny. Eksperci ACIP zalecają skrócenie tego okresu, zwłaszcza u pacjentów ≥70. roku życia, jednak nie powinien on być krótszy niż 2 miesiące.
Czy jednak warto w ogóle opóźniać szczepienie i zrealizować je u pacjenta w późniejszym okresie życia? Odpowiedź brzmi – nie warto. Aktualnie dostępne dane naukowe potwierdzają, że bardzo dobra skuteczność RZV utrzymuje się przez 10 lat (póki co nie prowadzono dłuższej obserwacji), to jednak należy mieć na uwadze starzenie się układu odpornościowego. Jest to proces postępujący i nieodwracalny, w efekcie którego zmniejsza się zdolność do „uczenia się” nowych antygenów. Jest to skutkiem m.in. zmniejszania się liczby dziewiczych limfocytów T i B. W przeciwieństwie do dzieci, osoby starsze mają dużo komórek pamięci i mało dziewiczych limfocytów, które nie zetknęły się jeszcze z antygenem. To przekłada się na słabszą odpowiedź na pierwotne szczepienie, ale zazwyczaj dobrą na dawki przypominające. Gorszą zdolność do odpowiedzi na nowe antygeny widać też w przypadku szczepionki RZV. Choć w obu badaniach ZOE-50 i ZOE-70 skuteczność i immunogenność szczepionki była bardzo duża, to i tak mniejsza u osób ≥70. roku życia. Poza tym, choć ryzyko półpaśca zwiększa się wraz z wiekiem, to jednak choroba ta i jej powikłania mogą też wystąpić u 50-latków. Szczepienie w młodszym wieku ma również wymiar ekonomiczny z punktu widzenia zdrowia publicznego. Ryzyko rozwoju półpaśca w ciągu całego życia szacuje się na około 30%. W Niemczech obciążenie systemu opieki zdrowotnej w związku z półpaścem oszacowano na >400 000 przypadków/rok, a całkowity koszt opieki związanej z tą chorobą wynosi około 182 mln euro. Curran i wsp. oszacowali, że aby zapobiec 1 przypadkowi półpaśca u osób w wieku 50–69 lat, trzeba zaszczepić 6 osób, a neuralgii popółpaścowej – 34–36 osób. W populacji osób >70. roku życia wskaźniki te są większe i wynoszą odpowiednio 10 i 48 osób. Badacze wykazali również, że szczepienie osób >50. roku życia jest bardziej opłacalne dla systemu niż szczepienie >60. roku życia.
Piśmiennictwo:
1. Tseng H.F., Harpaz R., Luo Y. i wsp.: Declining effectiveness of herpes zoster vaccine in adults aged ?60 years. J. Infect. Dis., 2016; 213: 1872–18752. Morrison V.A., Johnson G.R., Schmader K.E. i wsp.: Shingles Prevention Study Group. Long-term persistence of zoster vaccine efficacy. Clin. Infect. Dis., 2015; 60: 900–909
3. Curran D., Van Oorschot D., Matthews S. i wsp.: Long-term efficacy data for the recombinant zoster vaccine: impact on public health and cost effectiveness in Germany. Hum. Vaccin. Immunother., 2021; 17 (12): 5296–5303
4. CDC. Vaccines and Preventable Diseases. Shingrix Recommendations. www.cdc.gov/vaccines/vpd/shingles/hcp/shingrix/recommendations.html (dostęp: 6.10.2023)
5. Dooling K.L., Guo A., Patel M. i wsp.: Recommendations of the Advisory Committee on Immunization Practices for use of herpes zoster vaccines. MMWR, 2018; 67: 103–108
6. Strezova A., Diez-Domingo J., Al Shawafi K. i wsp.: Zoster-049 Study Group. Long-term protection against herpes zoster by the adjuvanted recombinant zoster vaccine: interim efficacy, immunogenicity, and safety results up to 10 years after initial vaccination. Open Forum Infect. Dis., 2022; 9 (10): ofac485
7. Grupping K., Campora L., Douha M. i wsp.: Immunogenicity and safety of an adjuvanted herpes zoster subunit vaccine in older adults previously vaccinated with a live-attenuated herpes zoster vaccine: a phase III, group-matched, clinical trial. Open Forum Infect. Dis., 2017; 4: S414
8. Dooling K.L., Guo A., Patel M. i wsp.: Recommendations of the Advisory Committee on Immunization Practices for use of herpes zoster vaccines. MMWR, 2018; 67: 103–108
9. Tylutka A., Zembroń-Łacny A.: Starzenie się układu immunologicznego i jego konsekwencje dla zdrowia. Postepy Hig. Med. Dosw, 2020; 74: 259–270
10. Lal H., Cunningham A.L., Godeaux O. i wsp.: ZOE-50 Study Group. Efficacy of an adjuvanted herpes zoster subunit vaccine in older adults. N. Engl. J. Med., 2015; 372: 2087–2096
11. Cunningham A.L., Lal H., Kovac M. i wsp.: ZOE-70 Study Group. Efficacy of the herpes zoster subunit vaccine in adults 70 years of age or older. N. Engl. J. Med., 2016; 375: 1019–1032